I. Tổng quan về glycosaminoglycan
Glycosaminoglycans (GAGs) là các phức hợp lớn của các chuỗi heteropolysaccharide tích điện âm. Chúng thường liên quan với một lượng nhỏ protein, hình thành nên các cấu trúc được gọi là proteoglycans, các cấu trúc này thường chứa đến 95% carbohydrate. GAGs có khả năng đặc biệt là liên kết với lượng nước lớn, tạo thành chất nền dạng gel mà hình thành nên phần nền tảng của chất nền cơ thể, là thành phần mà cùng với các protein cấu trúc dạng sợi như collagen, elastin và fibrillin-1 và các proteins kết dính như fibronectin, hình thành nên chất nền ngoại bào (extracellular matrix – ECM). GAGs hydrate hóa đóng vai trò như là một sự nâng đỡ linh động cho ECM, tương tác với các protein cấu trúc và các proteins bám dính, và đóng vai trò như là một sàng phân tử (molecular sieve), tác động đến chuyển động của các chất qua ECM. Các thuộc tính nhớt và bôi trơn của các sự bài tiết chất nhầy cũng là nhờ sự có mặt của GAGs, điều mà dẫn đến việc đặt tên trước đây cho các hợp chất này là mucopolysaccharides.
II. Cấu trúc
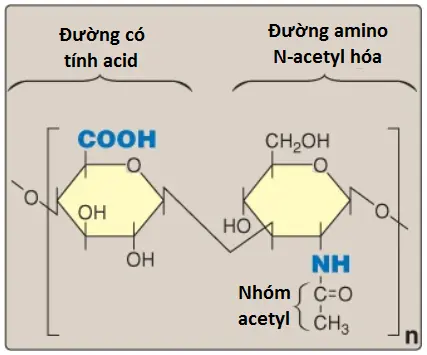
GAGs là các heteropolysaccharide dài, không phân nhánh được tạo thành từ các chuỗi disaccharide lặp đi lặp lại mà trong mỗi disaccharide sẽ có một trong số các đường là đường amino N-acetyl hóa (N-acetylated amino sugar), là N-acetylglucosamine (GlcNAc) hoặc N-acetylgalactosamine (GalNAc) (Hình 1) và đường còn lại là đường có tính acid (acidic sugar). Một ngoại trừ duy nhất là keratan sulfate, chứa galactose chứ không phải là đường acid. Đường amino là D-glucosamine hoặc D-galactosamine, trong đó nhóm amino thường được acetyl hóa, làm mất đi tích điện dương của nó. Đường amino cũng có thể được sulfate hóa trên carbon thứ 4 hoặc thứ 6 hoặc trên một nitrogen không được acetyl hóa. Đường acid thì là D-glucuronic acid hoặc là epimer C-5 của nó là L-iduronic acid (Hình 2). Các đường uronic này chứa các nhóm carboxyl mà tích điện âm ở pH sinh lý và cùng với các nhóm sulfate (-SO42-), tạo thành bản chất tích điện âm mạnh của GAGs.

A. Mối liên hệ cấu trúc – chức năng
Do nồng độ cao của các điện tích âm nên các chuỗi disaccharide lặp đi lặp lại này có khuynh hướng mở rộng trong dung dịch. Chúng đẩy nhau và được bao quanh bởi một vỏ phân tử nước. Khi chúng lại gần nhau, chúng trượt qua nhau, giống như hai nam châm cùng cực sẽ trượt qua nhau. Điều này tạo ra sự đặc sệt trơn trượt của các dịch niêm mạc và dịch khớp. Khi một dung dịch chứa GAGs bị nén lại, nước bị đẩy ra và GAGs được ép lại thành một thể tích nhỏ hơn. Khi sức ép mất đi, GAGs quay trở lại thể tích hydrate hóa ban đầu do sự đẩy các điện tích âm của chúng. Thuộc tính này đóng góp vào khả năng phục hồi của sụn, dịch khớp và dịch thủy tinh của mắt (Hình 3).

B. Phân loại
6 loại GAGs chính được phân chia theo thành phần monomer, loại liên kết glycoside và số lượng và vị trí của các đơn vị sulfate. Cấu trúc của GAGs và sự phân bố của chúng trong cơ thể thì được minh họa trong Hình 4. Tất cả các GAGs, trừ hyaluronic acid, thì được sulfate hóa và được phát hiện có liên kết một cách cộng hóa trị với protein, hình thành nên các monomer proteoglycans.

C. Proteoglycans
Proteoglycans được tìm thấy trong ECM trên mặt ngoài của các tế bào.
1. Cấu trúc monomer: Một monomer proteoglycans được tìm thấy trong sụn bao gồm một protein lõi mà đến 100 chuỗi GAGs thẳng kết nối cộng hóa trị với nó. Các chuỗi này, mỗi chuỗi có thể bao gồm lên đến 200 đơn vị disaccharide, mở ra từ protein lõi và vẫn phân tách với nhau do sự đẩy điện tích. Cấu trúc hình thành thì giống với bàn chải cọ chai lọ (bottle brush) (Hình 5). Trong proteoglycans sụn thì chondroitin sulfate và keratin sulfate là các loại GAGs chính. Chú ý rằng proteoglycans thì được phân nhóm theo các họ gene mà mã hóa cho các proteins lõi có các đặc điểm cấu trúc chung. Họ aggrecan (aggrecan, varsican, neurocan và brevican), có nhiều trong sụn, là một ví dụ.

2. Liên kết GAGs-protein: GAGs nối với protein lõi thông qua liên kết cộng hóa trị thì thường gặp nhất là qua một trihexoside (galactose-galactose-xylose) và một gốc serine trong protein. Một liên kết O-glycoside được hình thành giữa xylose và nhóm hydroxyl của serine (Hình 6).

Ứng dụng lâm sàng 14.1: Proteoglycans, sụn và viêm xương khớp
Viêm xương khớp ảnh hưởng đến hàng triệu người trên khắp thế giới. Trong bệnh này, sụn khớp bị thoái hóa và proteoglycans mà bình thường giúp cung cấp một đệm cho khớp bị mất đi. Nếu như không có khả năng hồi phục của sụn giúp bảo vệ khớp thì sẽ xuất hiện đau, cứng khớp và sưng với các sự nặng lên dần dần của các dấu hiệu và các triệu chứng. Glucosamine và chondroitin đã được ghi nhận là sẽ có cả tác dụng giảm đau và ngừng sự tiến triển của viêm xương khớp. Các hợp chất này thì hoàn toàn có sẵn trong các thực phẩm bổ sung mua qua quầy thuốc ở Hoa kỳ. Dựa trên một số nghiên cứu lâm sàng, người ta đã thấy rằng glucosamine sulfate (không phải glucosamine hydrochloride) và chondroitin sulfate có thể có tác động ít đến trung bình trong việc làm giảm các triệu chứng của viêm xương khớp.
3. Sự hình thành tập hợp: Nhiều monomer proteoglycans có thể liên kết với một phân tử hyaluronic acid để hình thành nên các tập hợp proteoglycans. Sự liên kết thì không phải là cộng hóa trị và xảy ra chủ yếu qua các tương tác ion giữa protein lõi và hyaluronic acid. Sự liên kết được ổn định thêm bởi các protein nhỏ được gọi là các protein liên kết (Hình 7).

III. Sự tổng hợp
Các chuỗi heteropolysaccharide thì được kéo dài bởi sự thêm vào tuần tự luân phiên của các đường acid và đường amino, chủ yếu đến từ các dẫn xuất uridine diphosphate của chúng (UDP). Các phản ứng được xúc tác bởi một họ các glycosyltransferases đặc hiệu. Bởi vì GAGs được sản xuất để bài tiết khỏi tế bào nên sự tổng hợp của chúng xảy ra chủ yếu trong bộ máy Golgi.
A. Sự tổng hợp đường amino
Các đường amino là các thành phần thiết yếu của glycoconjugates như proteoglycans, glycoproteins và glycolipids. Con đường tổng hợp các đường amino (hexosamines) thì diễn ra rất mạnh trong các mô liên kết, nơi mà đến 20% glucose đi theo con đường chuyển hóa này.
1. N-acetylglucosamine và N-acetylgalactosamine: Monosaccharide fructose 6-phosphate là tiền thân của GlcNAc và GalNAc. Một nhóm hydroxyl trên fructose thì bị thay thế bởi nitrogen amide của một glutamine và sản phẩm glucosamine 6-phosphate bị acetyl hóa, isomer hóa và hoạt hóa, tạo thành đường nucleotide UDP-GlcNAc (Hình 8). UDP-GalNAc được tạo thành bởi sự epimer hóa của UDP-GlcNAc. Chính các đường nucleotide này giúp hình thành nên các đường amino mà được sử dụng để kéo dài các chuỗi carbohydrate.

2. N-acetylneuraminic acid: NANA, một monosaccharide 9 carbon có tính acid, là một thành viên của họ các sialic acids, mỗi trong số các acid này được acetyl hóa ở các vị trí khác nhau. Các hợp chất này thường được tìm thấy như là các gốc carbohydrate tận cùng của các chuỗi bên oliosaccharide của các glycoproteins, của các glycolipids hay ít gặp hơn là của các GAGs. N-acetylmannosamine 6-phosphate (có nguồn gốc từ fructose 6-phosphate) và phosphoenolpyruvate (một trung gian trong quá trình đường phân) là các nguồn carbon và nitrogen ngay lập tức cho sự tổng hợp NANA (xem Hình 8). Trước khi NANA có thể được thêm vào một oliosaccharide đang phát triển thì nó phải được hoạt hóa thành cytidine monophosphate (CMP) – NANA bằng cách phản ứng với cytidine triphosphate (CTP). CMP-NANA synthetase xúc tác phản ứng này. CMP-NANA là đường nucleotide duy nhất trong chuyển hóa ở người mà trong đó chất mang nucleotide là một monophosphate chứ không phải là một diphosphate.
B. Sự tổng hợp đường có tính acid
D-glucuronic acid, mà cấu trúc của nó là glucose với một carbon thứ 6 được oxy hóa (-CH2OH → -COOH) và epimer C-5 của nó, L-iduronic acid, là các thành phần thiết yếu của GAGs. Glucuronic acid cũng cần cho sự giải độc các hợp chất ưa lipid, như bilirubin, steroids và nhiều thuốc, bao gồm statins, bởi vì sự liên hợp với glucuronate (sự glucuronide hóa) làm tăng tính tan trong nước của các hợp chất trên. Ở các thực vật và các động vật có vú (ngoài chuột lang và linh trưởng, bao gồm cả con người), glucuronic acid là một tiền thân của ascorbic acid (vitamin C) như được thể hiện trong Hình 9 (trong hình có chữ “di truyền trội” là mình ghi nhầm nhé, “di truyền lặn” nha). Con đường uronic acid này cũng cung cấp một cơ chế mà bằng cách đó D-xylulose trong chế độ ăn có thể đi vào trong các con đường chuyển hóa trung tâm.

1. Glucuronic acid: Glucuronic acid có thể thu được với các lượng nhỏ từ chế độ ăn và từ sự thoái hóa lysosome của GAGs. Nó có thể được tổng hợp bởi con đường uronic acid, mà trong đó glucose 1-phosphate phản ứng với uridine triphosphate (UTP) và được chuyển thành UDP-glucose. Sự oxy hóa của UDP-glucose tạo ra UDP-glucuronic acid, dạng mà cung cấp glucuronic acid cho sự tổng hợp GAGs và sự glucuronide hóa (Hình 10). Sản phẩm cuối cùng của sự chuyển hóa glucuronic acid ở người là D-xylulose 5-phosphate, thành phần mà có thể đi vào con đường pentose phosphate và tạo ra các trung gian đường phân glyceraldehyde 3-phosphate và fructose 6-phosphate (xem Hình 9; cũng xem thêm Hình 2 trong một bài viết trước).

2. L-iduronic acid: Sự tổng hợp của L-iduronic acid diễn ra sau khi D-glucuronic acid được tích hợp vào trong chuỗi carbohydrate. Uronosyl 5-epimerase gây ra sự epimer hóa của dạng đường D thành dạng đường L.
C. Sự tổng hợp của protein lõi
Protein lõi được tạo thành bởi các ribosomes trên lưới nội chất hạt (RER), đi vào trong lòng lưới nội chất hạt và sau đó di chuyển đến bộ máy Golgi, nơi mà nó được glycosyl hóa bởi glycosyltransferases liên kết màng.
D. Sự tổng hợp chuỗi carbohydrate
Sự hình thành chuỗi carbohydrate được khởi động bởi sự tổng hợp của một thành phần liên kết ngắn trên protein lõi mà trên đó sự tổng hợp chuỗi carbohydrate sẽ xảy ra. Thành phần liên kết thường gặp nhất là một trihexoside được hình thành bởi sự chuyển của một xylose từ UDP-xylose đến nhóm hydroxyl của một serine (hay threonine) xúc tác bởi xylosyltransferase. Hai phân tử galactose sau đó được thêm vào, hoàn thành trihexoside. Chuỗi này được tiếp tục sau đó bởi sự thêm vào tuần tự luân phiên các đường có tính acid và các đường amino (Hình 11) và sự epimer hóa của một số gốc D-glucuronyl thành các gốc L-iduronyl.

E. Sự thêm nhóm sulfate
Sự sulfate hóa của một GAG xảy ra sau khi monosaccharide được sulfate hóa được tích hợp vào chuỗi carbohydrate đang phát triển. Nguồn sulfate là từ 3′-phosphoadenosyl-5′-phosphosulfate (PAPS), một phân tử adenosine monophosphate có một nhóm sulfate liên kết với 5’-phosphate. Phản ứng sulfate hóa được xúc tác bởi sulfotransferases. Sự tổng hợp GAG sulfate hóa của chondroitin sulfate được thể hiện trong Hình 11. Chú ý rằng PAPS cũng là chất cho lưu huỳnh trong sự tổng hợp glycosphingolipid.
Các bạn có thể xem bài viết mới trên Facebook tại đây: https://www.facebook.com/profile.php?id=61550892771585
Các bạn có thể xem bài viết trước tại đây: https://docsachxyz.com/con-duong-pentose-phosphate-va-nicotinamide-adenine-dinucleotide-phosphate-phan-2/
Cảm ơn các bạn đã theo dõi bài viết. Hẹn gặp lại các bạn trong các bài viết tiếp theo nhé !!!