VI. Độ thanh thải thuốc bởi thận
Thuốc phải đủ phân cực mới có thể đào thải khỏi cơ thể. Việc đào thải thuốc khỏi cơ thể diễn ra thông qua một số con đường; quan trọng nhất là đào thải qua thận vào nước tiểu. Bệnh nhân suy thận có thể không bài tiết được thuốc và có nguy cơ tích tụ thuốc và tác dụng phụ.
A. Đào thải thuốc qua thận
Một loại thuốc phải trải qua một số quá trình ở thận trước khi đào thải: lọc cầu thận, bài tiết chủ động ở ống thận và tái hấp thu thụ động ở ống thận.
1. Lọc cầu thận
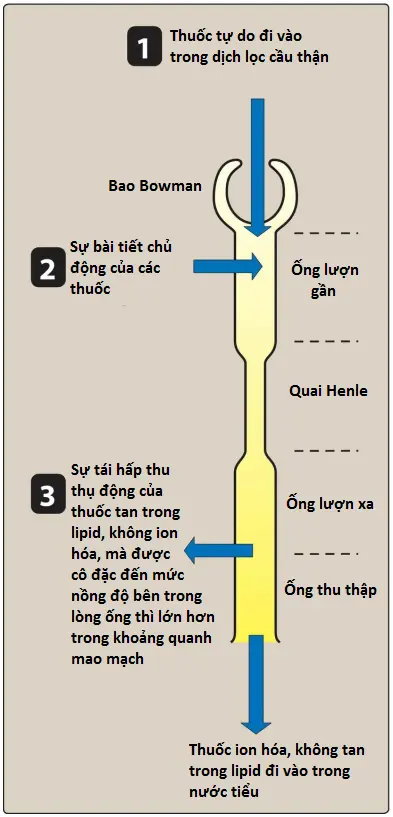
Thuốc đi vào thận qua động mạch thận, phân chia để tạo thành đám rối mao mạch cầu thận. Thuốc tự do (không liên kết với albumin) chảy qua các khe mao mạch vào khoang Bowman như một phần của dịch lọc cầu thận (Hình 1). Tốc độ lọc cầu thận (GFR) bình thường là khoảng 120 mL/phút/1.73m2 nhưng có thể giảm đáng kể ở bệnh thận. Độ hòa tan lipid và độ pH không ảnh hưởng đến quá trình thuốc đi vào dịch lọc cầu thận. Tuy nhiên, sự thay đổi trong GFR và khả năng liên kết protein của thuốc lại ảnh hưởng đến quá trình này.
2. Sự bài tiết ở ống lượn gần
Thuốc không được chuyển vào dịch lọc cầu thận khỏi cầu thận qua các tiểu động mạch ra mà phân chia để tạo thành đám rối mao mạch bao quanh lòng ống thận ở ống thận gần. Sự bài tiết chủ yếu xảy ra ở ống lượn gần thông qua hai hệ thống vận chuyển tích cực đòi hỏi năng lượng: một hệ thống cho anion (ví dụ, các dạng khử proton của axit yếu) và một hệ thống cho cation (ví dụ, các dạng proton của bazơ yếu). Mỗi hệ thống vận chuyển này đều có độ đặc hiệu thấp và có thể vận chuyển nhiều hợp chất. Do đó, sự cạnh tranh giữa các thuốc để giành các chất mang này có thể xảy ra trong mỗi hệ thống vận chuyển. [Lưu ý: Trẻ sinh non và trẻ sơ sinh có cơ chế bài tiết ở ống thận chưa phát triển hoàn chỉnh và do đó, có thể giữ lại một số loại thuốc trong máu.]
3. Tái hấp thu ở ống thận xa
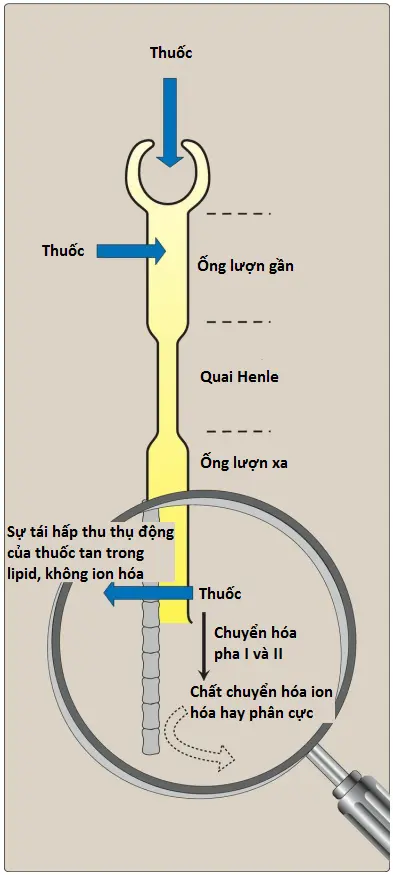
Khi thuốc di chuyển về phía ống lượn xa, nồng độ của thuốc tăng lên và vượt quá nồng độ của không gian quanh mạch máu. Thuốc, nếu không được tích điện, có thể khuếch tán ra khỏi lòng thận, trở lại tuần hoàn toàn thân (Hình 2). Có thể điều chỉnh độ pH của nước tiểu để tăng tỷ lệ thuốc ion hóa trong lòng thận để giảm thiểu lượng khuếch tán ngược và tăng độ thanh thải của thuốc không mong muốn. Nhìn chung, axit yếu có thể được loại bỏ bằng cách kiềm hóa nước tiểu, trong khi việc loại bỏ các bazơ yếu có thể được tăng cường bằng cách axit hóa nước tiểu. Quá trình này được gọi là “bẫy ion”. Ví dụ, một bệnh nhân bị quá liều phenobarbital (axit yếu) có thể được dùng bicarbonate, chất này sẽ kiềm hóa nước tiểu và giữ thuốc ở trạng thái ion hóa, do đó làm giảm sự tái hấp thu thuốc.
VII. Sự bài tiết bởi các con đường khác
Bài tiết thuốc cũng có thể xảy ra qua ruột, mật, phổi và sữa mẹ, ngoài những con đường khác. Thuốc không được hấp thu sau khi uống hoặc thuốc được tiết trực tiếp vào ruột hoặc vào mật được bài tiết qua phân. Phổi chủ yếu tham gia vào quá trình đào thải khí gây mê (ví dụ, desflurane). Việc đào thải thuốc qua sữa mẹ có thể khiến trẻ sơ sinh bú mẹ tiếp xúc với thuốc và/hoặc chất chuyển hóa mà người mẹ đang dùng và là nguồn tiềm ẩn gây ra các tác dụng phụ không mong muốn cho trẻ sơ sinh. Bài tiết hầu hết các loại thuốc qua mồ hôi, nước bọt, nước mắt, tóc và da chỉ xảy ra ở mức độ nhỏ. Độ thanh thải cơ thể toàn phần và thời gian bán thải của thuốc là các phương pháp quan trọng để thanh thải thuốc được sử dụng để tối ưu hóa liệu pháp thuốc và giảm thiểu độc tính.
A. Độ thanh thải cơ thể toàn phần
Độ thanh thải cơ thể (hệ thống) toàn phần, CLtotal, là tổng của tất cả các độ thanh thải từ các cơ quan chuyển hóa thuốc và đào thải thuốc. Thận thường là cơ quan bài tiết chính. Gan cũng góp phần thanh thải thuốc thông qua quá trình chuyển hóa và/hoặc bài tiết vào mật. Độ thanh thải toàn phần được tính theo công thức sau:
CLtoàn phần = CLgan + CLthận + CLphổi + CLkhác
trong đó CLgan + CLthận thường là quan trọng nhất.
B. Các tình huống lâm sàng dẫn đến thay đổi thời gian bán thải của thuốc
Khi bệnh nhân có bất thường làm thay đổi thời gian bán thải của thuốc, cần phải điều chỉnh liều dùng. Những bệnh nhân có thể có thời gian bán thải của thuốc tăng bao gồm những bệnh nhân có 1) lưu lượng máu thận hoặc gan giảm, ví dụ như trong tình trạng sốc tim, suy tim hoặc xuất huyết; 2) khả năng lọc thuốc từ huyết tương giảm, ví dụ như trong bệnh thận; và 3) chuyển hóa giảm, ví dụ như khi thuốc dùng đồng thời ức chế chuyển hóa hoặc trong tình trạng suy gan, như trong bệnh xơ gan. Những bệnh nhân này có thể cần giảm liều dùng hoặc giảm tần suất dùng thuốc. Ngược lại, thời gian bán thải của thuốc có thể giảm do lưu lượng máu gan tăng, giảm liên kết protein hoặc tăng chuyển hóa. Điều này có thể cần liều cao hơn hoặc tăng tần suất dùng thuốc.
VIII. Thiết kế và tối ưu hóa phác đồ liều lượng
Để bắt đầu liệu pháp dùng thuốc, bác sĩ lâm sàng phải chọn đường dùng, liều lượng và khoảng thời gian thuốc phù hợp. Việc lựa chọn phác đồ phụ thuộc vào nhiều yếu tố của bệnh nhân và thuốc, bao gồm tốc độ đạt được nồng độ điều trị của thuốc. Liệu pháp điều trị có thể bao gồm một liều thuốc duy nhất, ví dụ, thuốc gây ngủ, chẳng hạn như zolpidem. Thông thường hơn, thuốc được dùng liên tục, dưới dạng truyền tĩnh mạch hoặc theo phác đồ liều cố định/khoảng cách thời gian cố định qua đường tĩnh mạch hoặc đường uống (ví dụ, “một viên sau mỗi 4 giờ”). Việc dùng liên tục hoặc lặp lại sẽ dẫn đến tích tụ thuốc cho đến khi đạt trạng thái ổn định. Nồng độ ở trạng thái ổn định đạt được khi tốc độ đào thải thuốc bằng với tốc độ dùng thuốc, sao cho nồng độ thuốc trong huyết tương và mô vẫn tương đối ổn định.
A. Phác đồ truyền thuốc liên tục
Với truyền tĩnh mạch liên tục, tốc độ thuốc đi vào cơ thể là hằng số. Hầu hết các loại thuốc đều có quá trình đào thải bậc nhất, nghĩa là, một phần thuốc không đổi được đào thải trên một đơn vị thời gian. Do đó, tốc độ đào thải thuốc tăng theo tỷ lệ thuận với nồng độ trong huyết tương tăng.
1. Nồng độ thuốc trong huyết tương sau khi truyền tĩnh mạch liên tục
Sau khi bắt đầu truyền tĩnh mạch liên tục, nồng độ thuốc trong huyết tương tăng cho đến khi đạt trạng thái ổn định (tốc độ đào thải thuốc bằng tốc độ đưa thuốc vào cơ thể), tại thời điểm đó, nồng độ thuốc trong huyết tương vẫn không đổi.
a. Ảnh hưởng của tốc độ truyền đến nồng độ ở trạng thái ổn định
Nồng độ trong huyết tương ở trạng thái ổn định (Css) tỷ lệ thuận với tốc độ truyền. Ví dụ, nếu tốc độ truyền tăng gấp đôi, Css cũng tăng gấp đôi (Hình 3). Hơn nữa, Css tỷ lệ nghịch với độ thanh thải của thuốc. Do đó, bất kỳ yếu tố nào làm giảm độ thanh thải, chẳng hạn như bệnh gan hoặc thận, đều làm tăng Css của thuốc được truyền (giả sử Vd không đổi). Các yếu tố làm tăng độ thanh thải, chẳng hạn như tăng chuyển hóa, đều làm giảm Css.

b. Thời gian đạt nồng độ thuốc ở trạng thái ổn định
Nồng độ thuốc tăng từ 0 khi bắt đầu truyền đến mức trạng thái ổn định cuối cùng, Css (Hình 3). Hằng số tốc độ đạt trạng thái ổn định là hằng số tốc độ đào thải thuốc toàn phần khỏi cơ thể. Do đó, 50% Css của một thuốc được quan sát thấy sau thời gian t trôi qua, kể từ khi truyền thuốc, bằng t1/2, trong đó t1/2 (hoặc thời gian bán thải) là thời gian cần thiết để nồng độ thuốc thay đổi 50%. Sau một thời gian bán thải khác, nồng độ thuốc đạt tới 75% Css (Hình 4). Nồng độ thuốc là 87.5% Css ở 3 thời gian bán thải và 90% ở 3.3 thời gian bán thải. Do đó, một thuốc đạt trạng thái ổn định trong khoảng 4 đến 5 thời gian bán thải.

Yếu tố duy nhất quyết định tốc độ thuốc đạt trạng thái ổn định là thời gian bán thải (t1/2) của thuốc và tốc độ này chỉ bị ảnh hưởng bởi các yếu tố ảnh hưởng đến thời gian bán thải. Tốc độ tiệm cận trạng thái ổn định không bị ảnh hưởng bởi tốc độ truyền. Khi ngừng truyền, nồng độ thuốc trong huyết tương giảm xuống bằng không với cùng thời gian quan sát được khi tiệm cận trạng thái ổn định (Hình 4).
B. Phác đồ liều cố định/thời gian cố định
Việc dùng thuốc theo liều cố định thay vì truyền liên tục thường thuận tiện hơn. Tuy nhiên, liều cố định của thuốc tiêm tĩnh mạch hoặc uống được dùng theo các khoảng thời gian cố định sẽ dẫn đến sự dao động theo thời gian trong nồng độ thuốc lưu thông, trái ngược với sự gia tăng đều đặn của nồng độ thuốc khi truyền liên tục.
1. Tiêm tĩnh mạch nhiều lần
Khi một loại thuốc được dùng nhiều lần theo các khoảng thời gian đều đặn, nồng độ trong huyết tương sẽ tăng cho đến khi đạt trạng thái ổn định (Hình 5). Vì hầu hết các loại thuốc được dùng theo các khoảng thời gian ngắn hơn 5 thời gian bán thải và bị đào thải theo cấp số nhân theo thời gian, nên một ít thuốc từ liều đầu tiên vẫn còn trong cơ thể khi dùng liều thứ hai, một số thuốc từ liều thứ hai vẫn còn khi dùng liều thứ ba, v.v. Do đó, thuốc tích lũy cho đến khi, trong khoảng thời gian dùng thuốc, tốc độ đào thải thuốc bằng với tốc độ dùng thuốc và đạt được trạng thái ổn định.
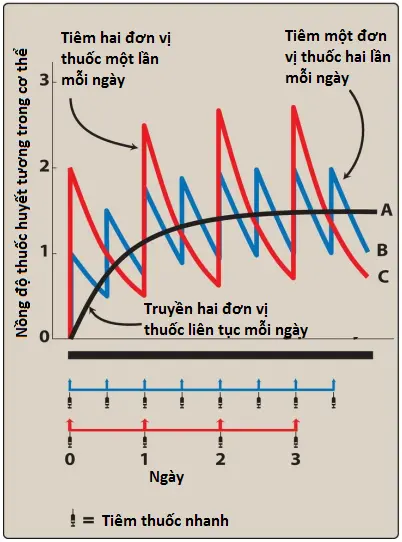
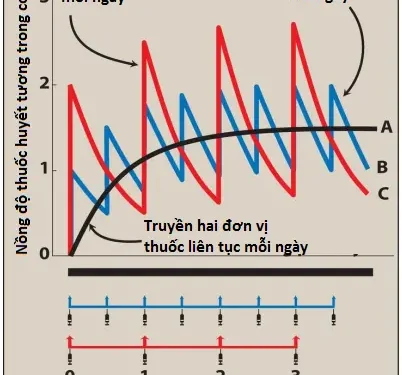
a. Ảnh hưởng của tần suất dùng thuốc
Khi dùng lặp lại ở các khoảng thời gian đều đặn, nồng độ thuốc trong huyết tương dao động quanh một giá trị trung bình. Sử dụng liều thấp hơn ở các khoảng thời gian ngắn hơn làm giảm biên độ dao động nồng độ thuốc. Tuy nhiên, tần suất dùng thuốc không làm thay đổi độ lớn của Css cũng như tốc độ đạt được Css.
b. Ví dụ về việc đạt được trạng thái ổn định khi sử dụng các phác đồ liều khác nhau
Đường cong B của Hình 5 cho thấy lượng thuốc trong cơ thể khi dùng 1 đơn vị thuốc qua đường tĩnh mạch và lặp lại ở các khoảng thời gian dùng thuốc tương ứng với thời gian bán thải của thuốc. Vào cuối khoảng thời gian dùng thuốc đầu tiên, còn lại 0.50 đơn vị thuốc từ liều đầu tiên khi dùng liều thứ hai. Vào cuối khoảng thời gian dùng thuốc thứ hai, còn lại 0.75 đơn vị khi dùng liều thứ ba. Lượng thuốc tối thiểu còn lại trong khoảng thời gian dùng thuốc dần dần đạt giá trị 1.00 đơn vị, trong khi giá trị tối đa ngay sau khi dùng thuốc dần dần đạt giá trị 2.00 đơn vị. Do đó, ở trạng thái ổn định, 1.00 đơn vị thuốc bị mất trong khoảng cách thời gian dùng thuốc, hoàn toàn khớp với tốc độ dùng thuốc. Nghĩa là, “tốc độ vào” bằng “tốc độ ra”. Giống như trường hợp truyền tĩnh mạch, 90% giá trị trạng thái ổn định đạt được trong 3.3 thời gian bán thải.
2. Nhiều lần dùng thuốc qua đường uống
Hầu hết các loại thuốc được dùng cho bệnh nhân ngoại trú là thuốc uống với liều lượng cụ thể một, hai hoặc nhiều lần mỗi ngày. Ngược lại với tiêm tĩnh mạch, thuốc dùng qua đường uống có thể được hấp thụ chậm và nồng độ thuốc trong huyết tương bị ảnh hưởng bởi cả tốc độ hấp thụ và tốc độ đào thải (Hình 6).

C. Tối ưu hóa liều dùng
Mục tiêu của liệu pháp dùng thuốc là đạt được và duy trì nồng độ trong một cửa sổ đáp ứng điều trị đồng thời giảm thiểu độc tính và/hoặc tác dụng phụ. Với việc chuẩn độ cẩn thận, hầu hết các loại thuốc đều có thể đạt được mục tiêu này. Nếu cửa sổ điều trị (xem loạt bài viết sau) của thuốc nhỏ (ví dụ, digoxin hoặc lithium), cần hết sức thận trọng khi lựa chọn phác đồ liều dùng và cần theo dõi nồng độ thuốc để đảm bảo đạt được khoảng điều trị. Phác đồ sử dụng thuốc được dùng dưới dạng một liều duy trì và có thể cần liều nạp nếu cần tác dụng nhanh.
1. Liều duy trì
Thuốc thường được dùng để duy trì Css trong cửa sổ điều trị. Một loại thuốc cần 4 đến 5 chu kỳ bán thải để đạt được Css. Để đạt được nồng độ cho trước, tốc độ dùng thuốc và tốc độ đào thải thuốc là rất quan trọng. Tốc độ liều có thể được xác định bằng cách biết nồng độ mục tiêu trong huyết tương (Cp), độ thanh thải (CL) của thuốc khỏi tuần hoàn hệ thống và phần thuốc (F) được hấp thu (sinh khả dụng):
Tốc độ liều = (Chuyết tương mục tiêu) (CL)/F
2. Liều nạp
Đôi khi cần đạt được nhanh chóng nồng độ mong muốn trong huyết tương (ví dụ, trong các trường hợp nhiễm trùng nghiêm trọng hoặc loạn nhịp tim). Do đó, “liều nạp” thuốc được dùng để đạt được nồng độ mong muốn trong huyết tương nhanh chóng, sau đó là liều duy trì để duy trì trạng thái ổn định (Hình 7). Nhìn chung, liều nạp có thể được tính như sau:

Liều nạp = (Vd) × (nồng độ huyết tương ở trạng thái ổn định mong muốn)/F
Nhược điểm của liều nạp bao gồm tăng nguy cơ độc tính của thuốc và thời gian giảm nồng độ trong huyết tương lâu hơn nếu xảy ra tình trạng dư thừa.
3. Điều chỉnh liều
Lượng thuốc dùng cho một tình trạng nhất định được ước tính dựa trên “bệnh nhân trung bình”. Cách tiếp cận này bỏ qua sự thay đổi giữa các bệnh nhân về các thông số dược động học như độ thanh thải và Vd, mà trong một số trường hợp, chúng khá đáng kể. Kiến thức về các nguyên tắc dược động học rất hữu ích trong việc điều chỉnh liều lượng để tối ưu hóa liệu pháp điều trị cho một bệnh nhân nhất định. Theo dõi liệu pháp dùng thuốc và liên hệ liệu pháp này với các lợi ích lâm sàng cung cấp một công cụ khác để cá nhân hóa liệu pháp điều trị.
Đối với các loại thuốc có khoảng điều trị xác định, nồng độ thuốc được đo và liều lượng và tần suất được điều chỉnh để đạt được mức mong muốn. Khi xác định sự điều chỉnh liều lượng, Vd có thể được sử dụng để tính toán lượng thuốc cần thiết để đạt được nồng độ mong muốn trong huyết tương. Ví dụ, giả sử một bệnh nhân suy tim không được kiểm soát tốt do nồng độ digoxin trong huyết tương không đủ. Giả sử nồng độ digoxin trong huyết tương là C1 và nồng độ mục tiêu mong muốn là C2, nồng độ cao hơn. Có thể sử dụng phép tính sau để xác định lượng digoxin bổ sung cần dùng để đưa nồng độ từ C1 lên C2.
(Vd)(C1) = Lượng thuốc ban đầu trong cơ thể
(Vd)(C2) = Lượng thuốc trong cơ thể cần thiết để đạt được nồng độ mong muốn trong huyết tương
Sự chênh lệch giữa hai giá trị là liều bổ sung cần thiết, bằng Vd (C2 − C1).
Hình 8 cho thấy diễn biến theo thời gian của nồng độ thuốc khi bắt đầu điều trị hoặc thay đổi liều dùng.

Các bạn có thể xem bài viết mới trên Facebook tại đây: https://www.facebook.com/profile.php?id=61550892771585
Các bạn có thể xem bài viết trước tại đây: https://docsachxyz.com/duoc-dong-hoc-pharmacokinetics-phan-3/
Cảm ơn các bạn đã theo dõi bài viết. Hẹn gặp lại các bạn trong các bài viết tiếp theo nhé !!!