IV. Các tác dụng của NADPH
D. Sự thực bào và tiêu diệt vi sinh vật của tế bào bạch cầu
Sự thực bào là sự tiêu hóa bằng sự nhập bào qua trung gian thụ cảm thể (receptor) các vi sinh vật, các phần tử ngoại lai và mảnh tế bào bởi các tế bào bạch cầu như bạch cầu trung tính (neutrophils) hay các đại thực bào (macrophages). Nó là một cơ chế phòng thủ quan trọng, đặc biệt là trong các sự nhiễm khuẩn. Bạch cầu trung tính và bạch cầu đơn nhân (monocytes) thì được trang bị các cơ chế không phụ thuộc oxygen và phụ thuộc oxygen (oxygen-independent and oxygendependent mechanisms) để tiêu diệt vi khuẩn.
1. Không phụ thuộc oxygen: Các cơ chế không phụ thuộc oxygen sử dụng các sự thay đổi pH trong các thể tự thực bào (phagolysosomes) và các enzyme lysosome để phá hủy bệnh nguyên.
2. Phụ thuộc oxygen: Các cơ chế phụ thuộc oxygen bao gồm các enzymes NADPH oxidase và myeloperoxidase (MPO) mà hoạt động cùng với nhau để giết chết vi khuẩn (Hình 8). Nhìn chung, hệ thống MPO là hệ thống mạnh mẽ nhất trong các cơ chế diệt khuẩn. Một vi khuẩn xâm nhập thì được nhận ra bởi hệ thống miễn dịch và bị tấn công bởi các kháng thể mà liên kết nó với một thụ cảm thể trên một tế bào thực bào. Sau khi sự nội hóa (internalization) vi sinh vật diễn ra, NADPH oxidase, bên trong màng tế bào bạch cầu, được hoạt hóa và khử O2 từ mô xung quanh thành superoxide (O2•−), một gốc tự do ROS, khi mà NADPH bị oxy hóa. Sự tiêu thụ nhanh O2 mà kèm theo sự hình thành O2•− được gọi là sự bùng nổ hô hấp (respiratory burst). (Chú ý: NADPH oxidase hoạt hóa là một phức hợp liên kết với màng gồm một flavocytochrome cùng với các peptides mà di chuyển từ bào tương đến nhờ sự hoạt hóa của tế bào bạch cầu. Các electrons di chuyển từ NADPH đến O2 thông qua flavin adenine nucleotide [FAD] và heme, tạo thành O2•−).
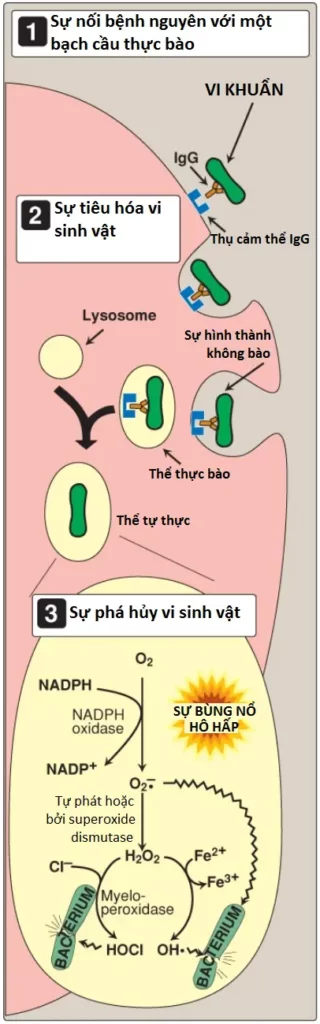
Các sự thiếu hụt di truyền hiếm trong NADPH oxidase gây ra bệnh u hạt mạn tính (chronic granulomatous disease – CGD) được đặc trưng bởi các nhiễm khuẩn dai dẳng, nặng nề và sự hình thành của các u hạt (các vùng viêm dạng hạt) mà cô lập vi khuẩn chưa bị phá hủy. Tiếp theo, O2•− được chuyển thành H2O2 (cũng là một ROS), hoặc tự phát hoặc được xúc tác bởi superoxide dismutase. Trong sự có mặt của MPO, một enzyme lysosome chứa heme xuất hiện trong thể tự thực (phagolysosome), peroxide cùng với các ion chloride được chuyển thành hypochlorus acid, HOCl, thành phần chính của thuốc tẩy gia dụng, chất này sẽ giết chết vi khuẩn. Peroxide cũng có thể bị khử một phần thành gốc hydroxyl (OH•), một ROS, hoặc vị khử hoàn toàn thành H2O bởi catalase hay glutathione peroxidase. Các sự thiếu hụt trong MPO không làm tăng khả năng mắc nhiễm khuẩn bởi vì peroxide từ NADPH oxidase có tính diệt khuẩn.
E. Sự tổng hợp nitric oxide
Nitric oxide (NO) được công nhận là một chất trung gian trong nhiều hệ thống sinh học. NO là một yếu tố gây giãn có nguồn gốc từ nội mô mà gây ra sự giãn mạch bằng cách làm giãn cơ trơn mạch máu. Nó cũng đóng vai trò như là một chất dẫn truyền thần kinh, ngăn cản sự kết tập tiểu cầu và đóng một vai trò thiết yếu trong chức năng đại thực bào. Nó có một thời gian bán hủy rất ngắn trong các mô (3 đến 10 giây) bởi vì nó phản ứng với O2 và O2•− và được chuyển thành nitrates và nitrites kể cả peroxynitrite (O=NOO-), một gốc nitrogen phản ứng (reactive nitrogen species – RNS). Chú ý rằng NO là một khí gốc tự do (free radical gas) mà thường nhầm lẫn với nitrous oxide (N2O), “khí cười” mà được sử dụng như là một chất gây tê và ổn định về mặt hóa học.
1. Sự tổng hợp nitric oxide: Arginine, O2 và NADPH là các cơ chất cho NO synthase bào tương ([NOS], Hình 9). Flavin mononucleotide (FMN), FAD, heme và tetrahydrobiopterin (xem các bài viết sau của mình) là các coenzymes và NO và citrulline là các sản phẩm của phản ứng. Ba isoenzymes NOS, mỗi trong số đó là sản phẩm của một gene khác nhau, đã được xác định. Hai trong số đó là các enzymes phụ thuộc calcium (Ca2+)-calmodulin (CaM) cơ bản (được tổng hợp ở một tốc độ hằng định) (xem bài viết trước của mình). Chúng được tìm thấy chủ yếu trong nội mô mạch máu (eNOS) và mô thần kinh (nNOS) và sản xuất liên tục các mức NO rất thấp để giãn mạch và cho sự dẫn truyền thần kinh. Một enzyme không phụ thuộc Ca2+ cảm ứng có thể được biểu hiện trong nhiều tế bào, bao gồm các đại thực bào và các bạch cầu trung tính, như là một sự phòng thủ sớm chống lại các bệnh nguyên. Các chất cảm ứng đặc hiệu đối với iNOS thay đổi theo loại tế bào và bao gồm các cytokines gây viêm, như yếu tố hoại tử u α (TNF-α) và interferon-γ (IFN-γ) và các nội độc tố của vi khuẩn như lipopolysaccharide (LPS). Các hợp chất này tăng cường sự tổng hợp của iNOS, thành phần mà có thể sản xuất ra các lượng lớn NO trong nhiều giờ hay thậm chí nhiều ngày.
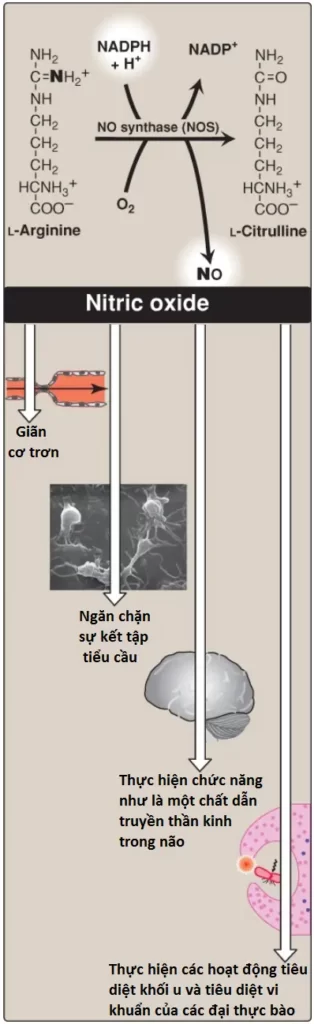
2. Nitric oxide và nội mô mạch máu: NO là một chất điều hòa quan trọng trong sự kiểm soát trương lực cơ trơn của mạch máu. NO được tổng hợp bởi eNOS trong các tế bào nội mô và khuếch tán đến cơ trơn của mạch máu, nơi mà nó hoạt hóa dạng bào tương của guanylyl cyclase (hay guanylate cyclase) để hình thành nên guanosine monophosphate vòng (cyclic adenosine monophosphate – cGMP). Phản ứng này thì tương tự với sự hình thành của adenosine monophosphate vòng (cyclic adenosine monophosphate – cAMP) bởi adenylyl cyclase (xem bài viết trước của mình nhé). Sự tăng lên kết quả trong cGMP gây ra sự hoạt hóa của protein kinase G, thành phần mà sẽ phosphoryl hóa các kênh Ca2+, gây ra sự giảm đi vào của Ca2+ vào trong các tế bào cơ trơn. Điều này làm giảm sự hoạt hóa Ca2+-CaM của kinase chuỗi nhẹ myosin (myosin light-chain kinase), bằng cách đó, làm giảm sự co cơ trơn và tạo điều kiện cho sự giãn cơ trơn.
Các nitrates giãn mạch như nitroglycerin, được chuyển hóa thành NO, chất này sẽ gây ra sự giãn của cơ trơn mạch máu và do đó, làm giảm huyết áp. Vì thế, NO có thể được hình dung như là một nitro giãn mạch nội sinh (endogenous nitrovasodilator). Chú ý rằng dưới các tình trạng thiếu oxygen, nitrite (NO2–) có thể được khử thành NO, chất mà liên kết với deoxyhemoglobin. NO được giải phóng vào trong máu, gây ra sự giãn mạch và tăng lưu lượng máu.
3. Nitric oxide và hoạt động tiêu diệt vi khuẩn của đại thực bào: Trong các đại thực bào, hoạt động của iNOS bình thường thì sẽ thấp nhưng sự tổng hợp của enzyme thì được kích thích một cách đáng kể bởi LPS của vi khuẩn và bởi sự giải phóng IFN-γ và TNF-α trong đáp ứng với nhiễm khuẩn. Các đại thực bào hoạt hóa hình thành nên các gốc O2•− mà kết hợp với NO để hình thành nên các trung gian mà phân ly, tạo thành gốc OH• có tính diệt khuẩn mạnh.
4. Các chức năng khác: NO là một chất ức chế mạnh mẽ sự bám và kết tập của tiểu cầu (bằng cách hoạt hóa con đường cGMP). Nó cũng có vai trò như là một chất dẫn truyền thần kinh trong các hệ thống thần kinh trung ương và ngoại vi.
V. Sự thiếu hụt G6PD
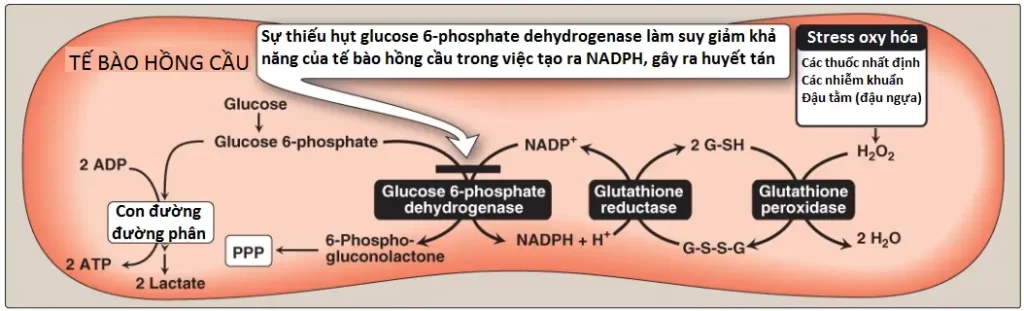
Sự thiếu hụt G6PD (G6PD deficiency), một tình trạng di truyền mà ảnh hưởng chủ yếu đến nam giới, được đặc trưng bởi thiếu máu huyết tán khi những người bị ảnh hưởng trải qua một stress oxy hóa. Thiếu máu được gây ra bởi sự mất khả năng của các tế bào hồng cầu (erythrocytes) trong việc giải độc các tác nhân oxy hóa. Với sự thiếu hụt G6PD, ít NADPH có sẵn hơn để duy trì một sự dự trữ glutathione khử mà giúp giải độc H2O2 tạo ra trong đáp ứng với stress oxy hóa.
A. Vai trò của G6PD trong các tế bào hồng cầu
Hoạt động đầy đủ của G6PD là cần thiết cho các tế bào trong việc hình thành nên NADPH cần cho sự duy trì của tích trữ G-SH. Mặc dù sự thiếu hụt G6PD xảy ra trong tất cả các tế bào của những người bị ảnh hưởng nhưng nó nặng nhất là trong các tế bào hồng cầu, nơi mà chỉ con đường pentose phosphate cung cấp các phương tiện để tạo ra NADPH. Ngoài ra, bởi vì các tế bào hồng cầu không có nhân hay các ribosomes nên chúng không thể khôi phục nguồn cung cấp enzyme của chúng, làm cho các tế bào hồng cầu đặc biệt dễ tổn thương với các dạng enzyme có tính ổn định suy giảm. Các mô khác có một con đường khác để sản xuất NADPH (thông qua malate dehydrogenase phụ thuộc NADP+ [malic enzyme]; xem các bài viết tiếp theo của mình nhé).
Ứng dụng lâm sàng 1: Các đặc điểm của sự thiếu hụt G6PD
Di truyền với đặc điểm liên kết với nhiễm sắc thể X nên G6PD ảnh hưởng chủ yếu đến nam giới và là sự bất thường enzyme gây bệnh thường gặp nhất ở con người. Hơn 400 triệu người bị ảnh hưởng trên khắp thế giới. Sự thiếu hụt enzyme này có tỷ lệ cao nhất ở những người mà có gốc Trung Đông, vùng nhiệt đới châu Á và châu Phi và các vùng của Địa Trung Hải. Sự thiếu hụt G6PD thực sự là một họ các tình trạng thiếu hụt được gây ra bởi một số các đột biến khác nhau trong các genes G6PD. Chỉ một số trong các biến thể protein kết quả là gây ra các triệu chứng lâm sàng.
Ngoài các cơn bệnh thiếu máu huyết tán định kỳ trong đáp ứng với stress oxy hóa, một biểu hiện lâm sàng thường gặp của thiếu hụt G6PD là vàng da sơ sinh xuất hiện 1 đến 4 ngày sau khi sinh. Vàng da, có thể nghiêm trọng, thường do sự tăng sản xuất bilirubin không liên hợp (unconjugated bilirubin) (xem các bài viết sau của mình nhé). Đời sống của những người mắc thể nghiêm trọng của thiếu hụt G6PD có thể giảm đi phần nào đó do các biến chứng từ huyết tán mạn tính. Tác động xấu của thiếu hụt G6PD được cân bằng trong quá trình tiến hóa bởi sự tăng đề kháng với sốt rét được gây ra bởi Plasmodium falciparum. Sự nhiễm của các tế bào hồng cầu bởi ký sinh trùng sẽ thúc đẩy stress oxy hóa và gây ra sự phân giải của các tế bào hồng cầu và bảo vệ vật chủ khỏi sự phát triển của sốt rét.
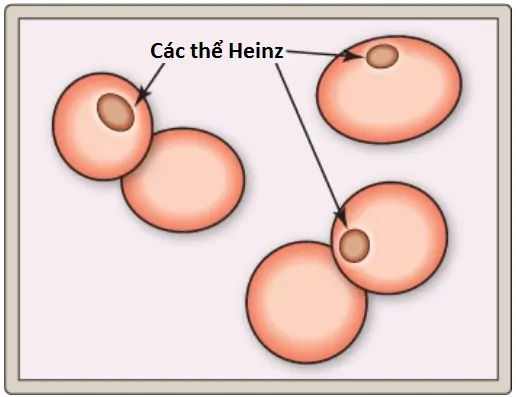
Sự thiếu hụt của G6PD làm giảm quá trình giải độc các gốc tự do và peroxides được hình thành bên trong tế bào (Hình 10). G-SH cũng giúp duy trì các trạng thái khử của các nhóm sulfhydryl trong các proteins, bao gồm hemoglobin. Sự oxy hóa của các nhóm sulfhydryl đó dẫn đến sự hình thành của các proteins biến tính mà tạo nên các khối không tan được gọi là các thể Heinz (Heinz bodies) bám vào các màng tế bào hồng cầu (Hình 11). Sự oxy hóa tiếp các proteins màng làm cho các màng hồng cầu trở nên cứng (ít có khả năng biến dạng hơn) và chúng bị loại bỏ khỏi hệ thống tuần hoàn bởi các đại thực bào trong lách và gan.
B. Các yếu tố khơi mào trong sự thiếu hụt G6PD
Những người nam mà di truyền một đột biến G6PD trên nhiễm sắc thể X duy nhất của họ thì được xem như là có đặc điểm bán hợp tử (hemizygous) đối với sự thiếu hụt G6PD bởi vì họ chỉ có một nhiễm sắc thể X. Những người bị ảnh hưởng sẽ vẫn không có triệu chứng một cách bình thường trừ khi hoặc cho đến khi họ trải qua một stress oxy hóa mạnh, điều mà có thể đến từ sự điều trị với một thuốc oxy hóa, sự tiêu hóa đậu răng ngựa (đậu tằm) hay một nhiễm khuẩn nặng. Sự phân giải của các tế bào hồng cầu và thiếu máu huyết tán xuất hiện ở những người có sự thiếu hụt G6PD trong đáp ứng với các chất thúc đẩy stress oxy hóa.
1. Các thuốc oxy hóa: Các thuốc mà có thể gây ra stress oxy hóa và gây ra thiếu máu huyết tán ở những bệnh nhân mắc thiếu hụt G6PD thường là thuộc các loại thuốc bắt đầu bằng chữ A: một số kháng sinh (antibiotics) (đặc biệt là các thuốc kháng sinh sulfonamides), một số thuốc chống sốt rét (antimalarials), một số thuốc giảm đau (analgesics) và một số thuốc hạ sốt (antipyretics). Chỉ các thuốc nhất định trong mỗi loại là có tác động. Danh sách thuốc có sẵn cho người kê đơn thường bao gồm các thuốc an toàn và các thuốc tốt nhất nên tránh cho những người mắc tình trạng thiếu hụt G6PD.
2. Thiếu máu tán huyết do ăn đậu tằm (favism): Những người mắc một số dạng thiếu hụt G6PD, đặc biệt là biến thể Địa Trung Hải (Mediterranean variant) thì đặc biệt dễ mắc tác động huyết tán của đậu tằm (fava bean hay broad bean), một thực phẩm phổ biến trong chế độ ăn ở vùng Địa Trung Hải. Tác động huyết tán do ăn đậu tằm thì không được quan sát thấy trong tất cả những người mắc thiếu hụt G6PD nhưng tất cả những bệnh nhân mắc thiếu máu tán huyết do ăn đậu tằm thì đều có thiếu hụt G6PD.
3. Nhiễm khuẩn: Sự nhiễm khuẩn là một yếu tố khơi mào thường gặp của huyết tán ở những người mắc thiếu hụt G6PD. Đáp ứng viêm với nhiễm khuẩn gây ra sự hình thành của các gốc tự do trong các đại thực bào. Các gốc tự do có thể khuếch tán vào bên trong các tế bào hồng cầu và gây ra tổn thương oxy hóa.
C. Các biến thể của gene G6PD
Sự nhân bản và phân tích trình tự của gene G6PD (xem các bài viết sau này của mình) đưa đến sự xác định của hơn 400 biến thể G6PD khác nhau mà gây ra sự thiếu hụt enzyme G6PD. Một số đột biến không ảnh hưởng đến hoạt động của enzyme. Hầu hết các đột biến mà gây ra giảm chức năng của enzyme G6PD là các đột biến điểm sai nghĩa (missense point mutations) (xem các bài viết sau của mình); một số gây ra sự giảm hoạt động xúc tác, các số khác gây ra sự giảm tính ổn định trong khi các đột biến G6PD khác làm thay đổi ái tính liên kết đối với NADP+ hay glucose 6-phosphate. Enzyme G6PD hoạt động tồn tại dưới dạng homodimer hay tetramer. Các đột biến ở giao diện giữa các tiểu đơn vị có thể ảnh hướng đến tính ổn định của enzyme.
Mức độ nghiêm trọng của thiếu máu huyết tán ở những người bị thiếu hụt G6PD thường liên quan với mức độ hoạt động của enzyme trong các tế bào hồng cầu của bệnh nhân. Các biến thể G6PD có thể được phân loại như được thể hiện trên Hình 12. G6PD A- là nguyên mẫu của thể trung bình của bệnh (loại III). Các tế bào hồng cầu chứa một G6PD không ổn định nhưng bình thường về mặt động lực học, với hầu hết hoạt động của enzyme hiện diện trong tế bào hồng cầu lưới (reticulocytes) và các tế bào hồng cầu trẻ (Hình 13). Các tế bào hồng cầu già nhất có mức độ hoạt động của G6PD thấp nhất và được ưu tiên loại bỏ trong cơn huyết tán. Bởi vì huyết tán không ảnh hưởng đến các tế bào trẻ hơn nên các cơn huyết tán sẽ tự giới hạn. G6PD Địa Trung Hải là nguyên mẫu của một sự thiếu hụt nghiêm trọng hơn (loại II). Các đột biến loại I (hiếm) là dạng nặng nhất và liên quan với thiếu máu huyết tán không có hồng cầu hình cầu mạn tính, ngay cả khi không có stress oxy hóa.
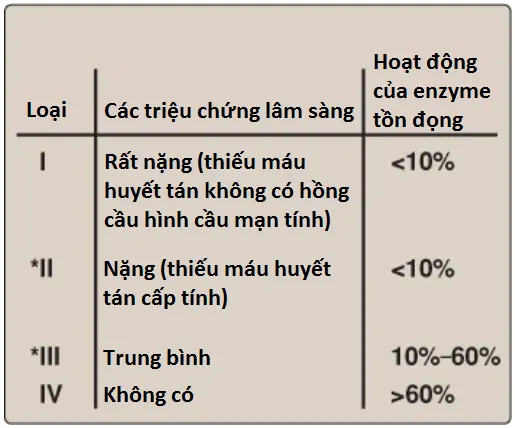
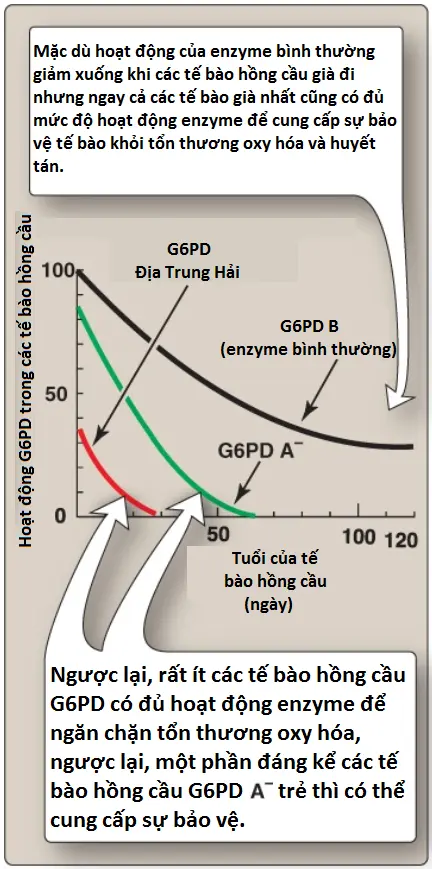
Cả các proteins G6PD A- và G6PD Địa Trung Hải đều đại diện cho các enzymes đột biến mà khác so với các biến thể bình thường tương ứng bởi một amino acid. Các đột biến mất hay dịch khung (deletions or frameshift mutations) lớn thì chưa xác định được, cho thấy rằng sự vắng mặt hoàn toàn hoạt động của enzyme G6PD thì có khả năng cao là gây tử vong.
VI. Tổng hợp bài viết
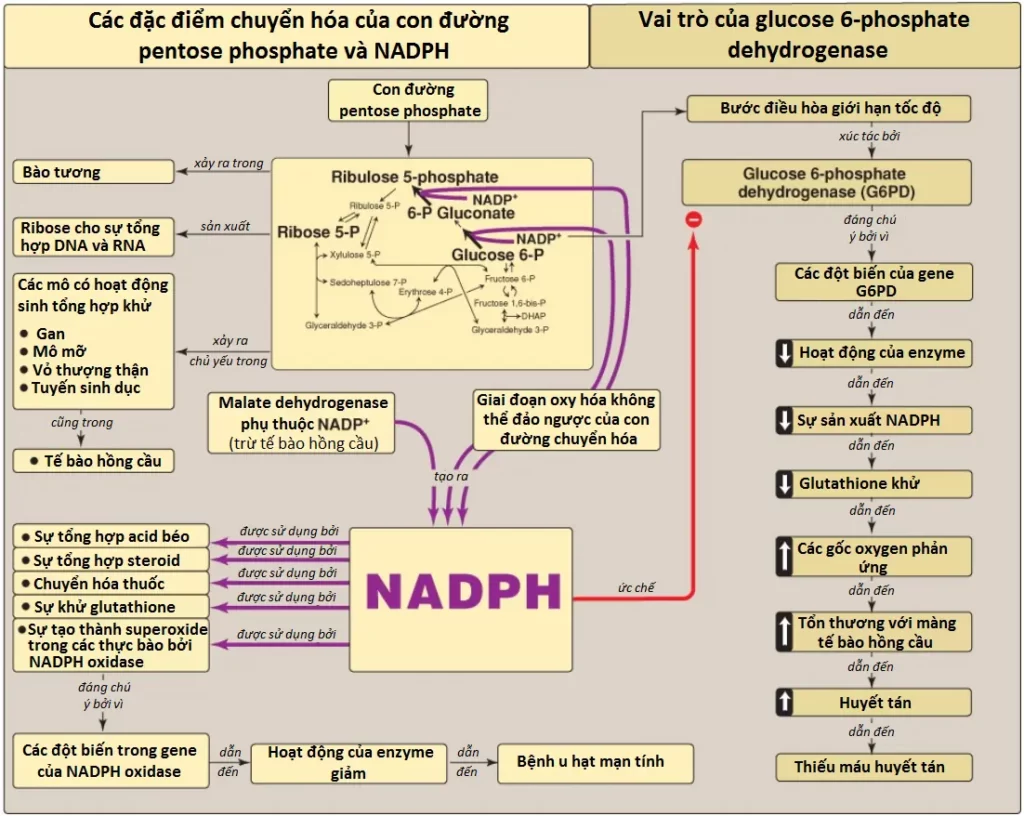
- Con đường pentose phosphate (pentose phosphate pathway) là con đường sản xuất NADPH chính trong cơ thể (Hình 14).
- Không có ATP được sử dụng hay tiêu thụ trong con đường này.
- Con đường này bao gồm một giai đoạn oxy hóa không thể đảo ngược, theo sau bởi một chuỗi các sự chuyển đổi có thể đảo ngược của đường-phosphate.
- Các phản ứng không phải oxy hóa có thể đảo ngược (reversible nonoxidative reactions) sẽ chuyển đổi qua lại giữa các đường. Ribulose 5-phosphate được chuyển thành ribose 5-phosphate, cần cho sự tổng hợp nucleotide và nucleic acid, hoặc thành fructose 6-phosphate và glyceraldehyde 3-phosphate (các trung gian đường phân).
- Phần oxy hóa tạo ra NADPH (NADPH-producing oxidative portion) của con đường cung cấp các đương lượng khử cho sự sinh tổng hợp khử và các phản ứng khử độc.
- Trong phần này của con đường, glucose 6-phosphate được chuyển đổi một cách không thể đảo ngược thành ribulose 5-phosphate và 2 NADPHs được tạo ra. Bước điều hòa được xúc tác bởi G6PD, thành phần bị ức chế mạnh bởi sự tăng lên trong tỷ số NADPH/NADP+.
- NADPH là một nguồn của các đương lượng khử (reducing equivalents) trong quá trình sinh tổng hợp khử (reductive biosynthesis) như sự sản xuất các acid béo trong gan, mô mỡ và tuyến vú; cholesterol trong gan và các hormones steroid trong nhau thai, buồng trứng, tinh hoàn và vỏ thượng thận.
- NADPH cũng được cần bởi các tế bào hồng cầu cho sự khử H2O2 được tạo ra như là kết quả của quá trình chuyển hóa hiếu khí.
- G-SH được sử dụng bởi glutathione peroxidase để khử peroxide thành nước. Glutathione oxy hóa (oxidized glutathione) (G-S-S-G) tạo ra được khử bởi glutathione reductase, sử dụng NADPH như là nguồn các electrons.
- NADPH cung cấp các đương lượng khử cho hệ thống cytochrome P450 monooxygenase của ty thể (mitochondrial cytochrome P450 monooxygenase system), hệ thống được sử dụng trong sự tổng hợp hormone steroid (steroid hormone synthesis) trong mô tạo hormone steroid (steroidogenic tissue), sự tổng hợp acid mật (bile acid synthesis) trong gan và sự hoạt hóa vitamin D (vitamin D activation) trong gan và các thận.
- Hệ thống tiểu thể (microsomal system) sử dụng NADPH để khử độc các chất ngoại lai (xenobiotics) như các thuốc và nhiều chất gây ô nhiễm. NADPH cung cấp các đương lượng khử cho các tế bào thực bào liên quan đến sự loại bỏ các vi sinh vật xâm nhập. NADPH oxidase sử dụng phân tử oxygen (O2) và các electrons từ NADPH để sản xuất các gốc superoxide (superoxide radicals), thành phần mà cuối cùng sẽ được chuyển thành peroxide bởi superoxide dismutase.
- Sự thiếu hụt G6PD (G6PD deficiency), một bệnh liên kết với nhiễm sắc thể X mà ảnh hưởng chủ yếu đến nam giới, làm suy giảm khả năng của tế bào hồng cầu (erythrocyte) trong việc hình thành NADPH cần cho sự duy trì việc tích trữ G-SH. Các tế bào hồng cầu thì bị ảnh hưởng nhiều nhất bởi vì chúng không có thêm các nguồn NADPH. Bệnh được đặc trưng bởi thiếu máu huyết tán (hemolytic anemia) gây ra bởi sự sản xuất các gốc tự do và các peroxides sau khi trải qua stress oxy hóa, bao gồm nhiễm khuẩn nặng; các thuốc oxy hóa (oxidant drugs) hay đậu ngựa (đậu tằm) (fava beans). Mức độ của thiếu máu phụ thuộc vào mức độ hoạt động của enzyme tồn đọng. Những đứa trẻ mới sinh mà có suy giảm G6PD có thể sẽ trải qua vàng da sơ sinh (neonatal jaundice) kéo dài.
Các bạn có thể xem bài viết mới trên Facebook tại đây: https://www.facebook.com/profile.php?id=61550892771585
Các bạn có thể xem bài viết trước tại đây: https://docsachxyz.com/con-duong-pentose-phosphate-va-nicotinamide-adenine-dinucleotide-phosphate-phan-1/
Cảm ơn các bạn đã theo dõi bài viết. Hẹn gặp lại các bạn trong các bài viết tiếp theo nhé !!!





































