I. Tổng quan
Ribonucleoside và deoxyribonucleoside phosphates (nucleotides) có vai trò thiết yếu đối với tất cả các tế bào. Nếu như không có chúng, cả ribonucleic acid (RNA) và deoxyribonucleic acid (DNA) đều không thể được sản xuất được, và vì thế, các proteins không thể được tổng hợp và các tế bào cũng không thể tăng sinh. Các nucleotides cũng đóng vai trò như là các chất mang cho các trung gian hoạt hóa trong sự tổng hợp của một số carbohydrates, lipids và proteins liên hợp (như uridine diphosphate [UDP]-glucose và cytidine diphosphate [CDP]-choline) và là các thành phần cấu trúc cho một số coenzyme thiết yếu, như coenzyme A, flavin adenine dinucleotide (FAD[H2]), nicotinamide adenine dinucleotide (NAD[H]) và nicotinamide adenine dinucleotide phosphate (NADP[H]). Các nucleotides, như adenosine monophosphate vòng (cAMP) và guanosine monophosphate vòng (cGMP), đóng vai trò như là các chất truyền tin thứ hai trong các con đường truyền tín hiệu. Ngoài ra, các nucleotides đóng một vai trò quan trọng như là các nguồn năng lượng trong tế bào. Cuối cùng, các nucleotides là các hợp chất điều hòa quan trọng đối với nhiều con đường chuyển hóa trung gian, ức chế hoặc hoạt hóa các enzyme quan trọng. Các bases purine và pyrimidine được tìm thấy trong các nucleotides có thể được tổng hợp mới hoặc có thể thu được thông qua các con đường thu hồi mà cho phép sự sử dụng lại các bases đã được hình thành trước đó do sự thay thế bình thường của tế bào. (Chú ý: Một ít purine và pyrimidine được cung cấp bởi chế độ ăn là được sử dụng; ngược lại, gần như tất cả các nucleic acids mà đi vào trong đường tiêu hóa [GI] là bị thoái hóa).
II. Cấu trúc
Các nucleotides bao gồm một base nitrogen; một monosaccharide pentose; và một, hai hoặc ba nhóm phosphate. Các bases chứa nitrogen thuộc về hai họ hợp chất: purines và pyrimidines.
A. Các base purine và pyrimidine
Purines là các cấu trúc vòng kép, ngược lại, pyrimidines chỉ có một vòng đơn. Cả DNA và RNA đều chứa cùng các base purine: adenine (A) và guanine (G). Cả DNA và RNA đều chứa pyrimidine cytosine (C), nhưng chúng lại khác nhau trong base pyrimidine thứ hai: DNA chứa thymine (T), ngược lại, RNA chứa uracil (U). T và U khác nhau chỉ ở việc T có một nhóm methyl (Hình 1). Các base không thường gặp (đã chỉnh sửa) thì đôi khi được tìm thấy trong một số loại DNA (như trong một số DNA của virus) và RNA (như trong RNA vận chuyển [tRNA]). Các sự chỉnh sửa base bao gồm sự methyl hóa, sự glycosyl hóa, sự acetyl hóa và sự khử. Một số ví dụ của các base không thường gặp được thể hiện trong Hình 2. (Chú ý: Sự có mặt của các base không thường gặp trong một trình tự nucleotides có thể hỗ trợ trong khả năng nhận diện nó của các enzyme chuyên biệt hoặc bảo vệ nó khỏi bị thoái hóa bởi các nucleases).
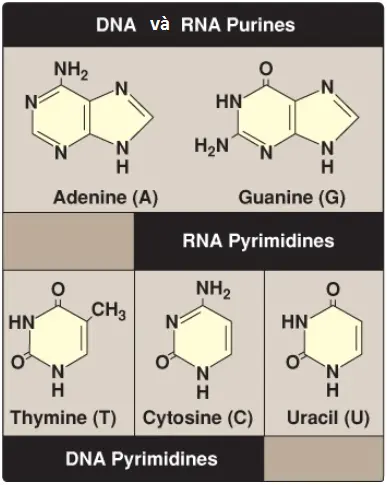
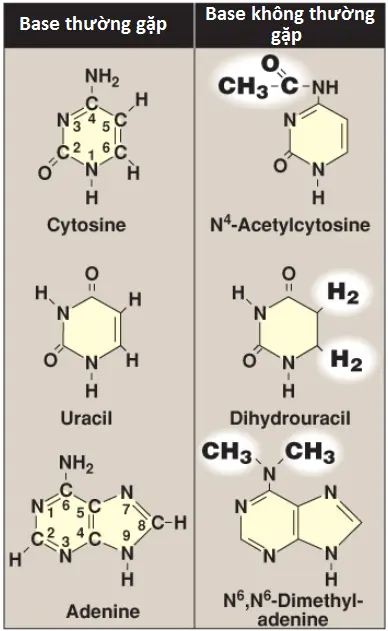
B. Nucleosides
Sự bổ sung một đường pentose vào một base thông qua một liên kết N-glycoside tạo ra một nucleoside. Nếu như đường là ribose, một ribonucleoside được tạo ra và nếu như đường là 2-deoxyribose thì một deoxyribonucleoside được tạo ra (Hình 3A). Các ribonucleosides là A, G, C và U được đặt tên lần lượt cho adenosine, guanosine, cytidine và uridine. Các deoxyribonucleoside là A, G, C và T thì có thêm tiền tố deoxy- (như deoxyadenosine). (Chú ý: Hợp chất deoxythymidine thường được gọi đơn giản là thymidine, với tiền tố deoxy- đã được ngầm hiểu, bởi vì nó chỉ được tích hợp vào trong DNA). Các nguyên tử carbon và nitrogen trong các vòng base và đường được đánh số riêng rẽ (xem Hình 3B). (Chú ý: Carbons trong pentose được đánh số 1’ đến 5’. Vì thế, khi 5’-carbon của nucleoside [hay nucleotides] được nhắc đến thì một nguyên tử carbon trong pentose, chứ không phải một nguyên tử trong base, sẽ được nghĩ đến).
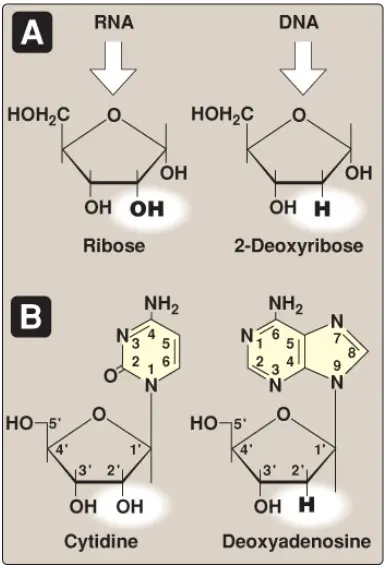
C. Nucleotides
Sự bổ sung của một hoặc nhiều nhóm phosphate vào một nucleoside tạo ra một nucleotide. Nhóm phosphate đầu tiên được nối bởi một liên kết ester vào 5’-OH của pentose, hình thành nên một nucleoside 5’-phosphate hay 5’-nucleotide. Loại pentose được phản ánh bởi tiền tố trong các tên 5’-ribonucleotide và 5’-deoxyribonucleotide. Nếu như một nhóm phosphate được nối với 5’-carbon của pentose thì cấu trúc là một nucleoside monophosphate, như adenosine monophosphate (AMP, hay adenylate). Nếu như một nhóm phosphate thứ hai hoặc thứ ba được thêm vào trong nucleoside thì một nucleoside diphosphate (như adenosine diphosphate [ADP] hoặc triphosphate, như ATP) sẽ được tạo ra (Hình 4). Các phosphate thứ hai và thứ ba sẽ kết nối với nucleotides bởi một “liên kết cao năng” (một liên kết với một sự biến đổi âm lớn của năng lượng tự do [-ΔG] trong sự thủy phân). (Chú ý: Các nhóm phosphate chịu trách nhiệm cho các sự tích điện âm liên quan với các nucleotides và làm cho DNA và RNA được gọi là các nucleic acids).
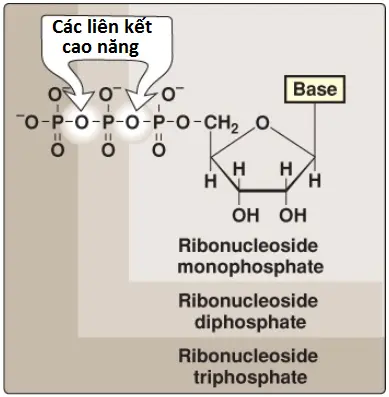
III. Sự tổng hợp nucleotide purine
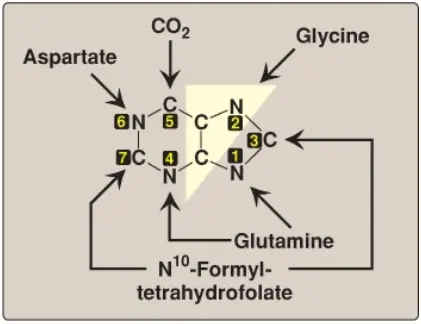
Các nguyên tử của vòng purine được đóng góp bởi một số hợp chất, bao gồm các amino acids (aspartate, glycine và glutamine), carbon dioxide (CO2) và N10-formyltetrahydrofolate (N10-formyl-THF), như được thể hiện trong Hình 5. Vòng purine được cấu trúc chủ yếu trong gan bởi một chuỗi các phản ứng mà thêm các carbons và các nitrogens được cho bởi các hợp chất vào trong một ribose 5-phosphate được hình thành từ trước. (Chú ý: Sự tổng hợp của ribose 5-phosphate từ glucose 6-phosphate bởi con đường pentose phosphate được nói đến trên trong bài viết trước).
A. Sự tổng hợp 5-Phosphoribosyl-1-pyrophosphate
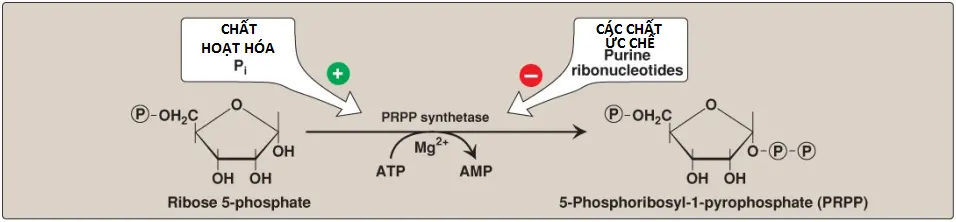
5-Phosphoribosyl-1-pyrophosphate (PRPP) là một pentose hoạt hóa mà tham gia vào trong sự tổng hợp và sự thu hồi các purine và pyrimidine. Sự tổng hợp của PRPP từ ATP và ribose 5-phosphate được xúc tác bởi PRPP synthetase (Hình 6). Enzyme liên kết NST X này được hoạt hóa bởi phosphate vô cơ và bị ức chế bởi các nucleotides purine (sự ức chế của sản phẩm cuối cùng). (Chú ý: Bởi vì gốc đường của PRPP là ribose nên ribonucleotides là các sản phẩm cuối cùng của sự tổng hợp purine mới. Khi deoxyribonucleotide được cần cho sự tổng hợp DNA, gốc đường ribose sẽ được khử).
B. Sự tổng hợp 5-Phosphoribosylamine
Sự tổng hợp của 5-phosphoribosylamine từ PRPP và glutamine được thể hiện trong Hình 7. Nhóm amide của glutamine thay thế nhóm pyrophosphate nối vào carbon 1 của PRPP. Đây là bước cam kết trong quá trình sinh tổng hợp nucleotide purine. Enzyme mà xúc tác cho phản ứng, là glutamine:phosphoribosylpyrophosphate amidotransferase (GPAT), được ức chế bởi purine 5’-nucleotides AMP và guanosine monophosphate (GMP, hay guanylate), các sản phẩm cuối cùng của con đường. Tốc độ phản ứng cũng được kiểm soát bởi nồng độ PRPP nội bào. (Chú ý: Nồng độ của PRPP bình thường rất thấp so với hằng số Michaelis [Km] đối với GPAT. Vì thế, bất cứ sự thay đổi nhỏ nào trong nồng độ PRPP sẽ gây ra một sự thay đổi tỷ lệ thuận trong tốc độ phản ứng).
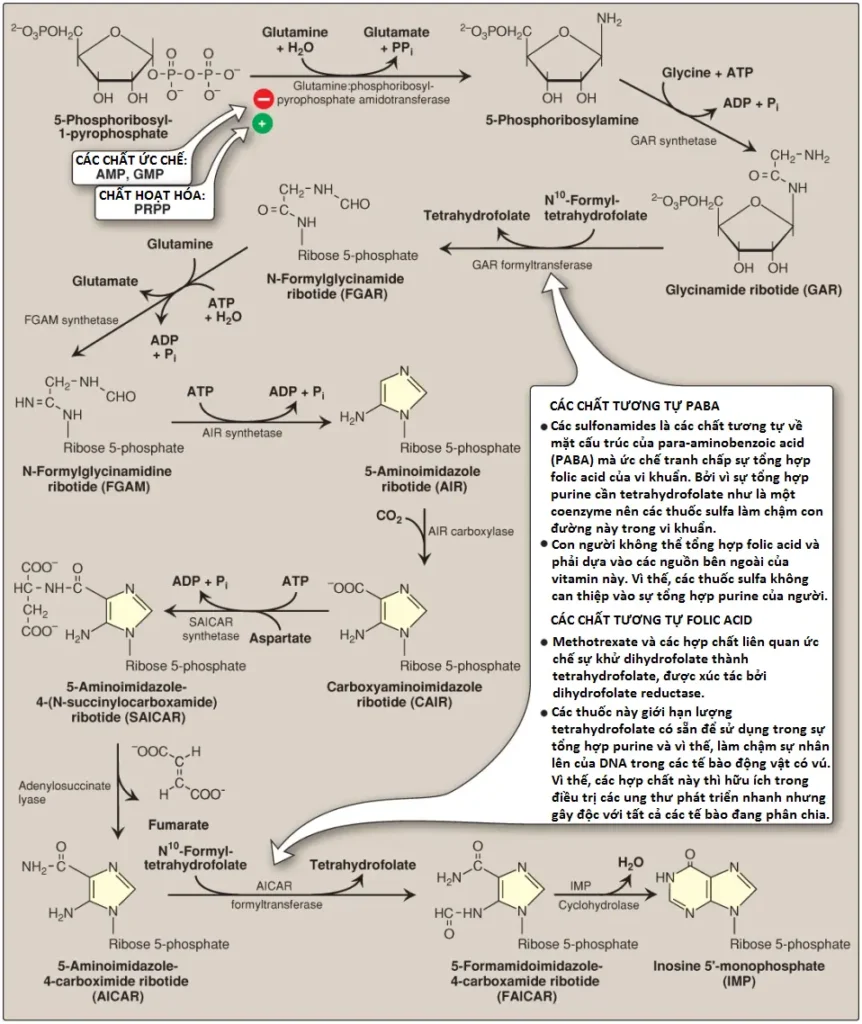
C. Sự tổng hợp inosine monophosphate
9 bước tiếp theo trong quá trình sinh tổng hợp nucleotide purine sẽ dẫn đến sự tổng hợp của inosine monophosphate ([IMP] mà base của nó là hypoxanthine) được minh họa trong Hình 7. IMP là nucleotide purine cha cho AMP và GMP. 4 bước trong con đường này cần ATP như là một nguồn năng lượng và 2 bước trong con đường cần N10-formyl-THF như là một chất cho một carbon. (Chú ý: Hypoxanthine được tìm thấy trong tRNA).
D. Các chất ức chế tổng hợp
Một số chất ức chế tổng hợp của sự tổng hợp purine (như sulfonamides) là có tác dụng ức chế sự phát triển của các vi sinh vật đang phân chia nhanh mà không can thiệp vào chức năng của tế bào người (xem Hình 7). Các chất ức chế tổng hợp purine khác, như các chất tương tự về mặt cấu trúc với folic acid (như methotrexate), được sử dụng về mặt dược lý để kiểm soát sự lan rộng của ung thư bằng cách can thiệp vào sự tổng hợp của nucleotides và vì thế, cả của DNA và RNA (xem Hình 7).
Các chất ức chế sự tổng hợp purine ở người thì cực kỳ độc với các mô, đặc biệt là với các cấu trúc đang phát triển như các cấu trúc trong một thai nhi hoặc với các loại tế bào mà bình thường nhân đôi nhanh, bao gồm các tế bào tủy xương, da, đường tiêu hóa, hệ miễn dịch hoặc nang tóc. Kết quả, những người sử dụng các thuốc chống ung thư như vậy có thể trải qua các tác dụng phụ, bao gồm thiếu máu, da có vảy, rối loạn đường tiêu hóa, suy giảm miễn dịch và rụng tóc.
E. Sự tổng hợp adenosine và guanosine monophosphate
Sự chuyển đổi của IMP thành AMP hoặc GMP sử dụng một con đường hai bước, cần năng lượng và nitrogen (Hình 8). (Chú ý: Sự tổng hợp AMP cần guanosine triphosphate [GTP] như là một nguồn năng lượng và aspartate như là một nguồn nitrogen, ngược lại, sự tổng hợp GMP cần ATP và glutamine). Ngoài ra, phản ứng đầu tiên trong mỗi con đường bị ức chế bởi sản phẩm cuối cùng của con đường đó. Điều này cung cấp một cơ chế để điều hướng IMP trong việc tổng hợp purine có lượng ít hơn. Nếu như cả AMP và GMP xuất hiện với các lượng đủ thì con đường tổng hợp mới của sự tổng hợp nucleotide purine bị ức chế ở bước GPAT.
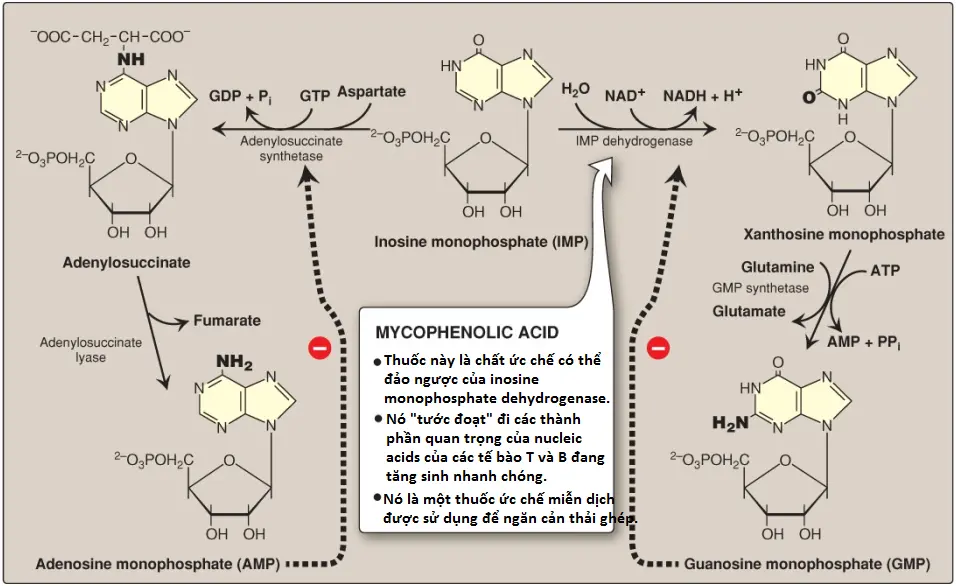
Mycophenolic acid là một chất ức chế có thể đảo ngược của IMP dehydrogenase, enzyme được sử dụng để tạo GMP. Các tế bào lympho T và B đang tăng sinh dễ chịu tổn thương với các mức thấp của nucleotide purine quan trọng này, vì thế mycophenolic acid là một chất ức chế miễn dịch hiệu quả để ngăn cản tình trạng thải ghép cơ quan (thận, tim và gan), cũng như là các rối loạn miễn dịch nhất định như bệnh lupus hay bệnh Crohn.
F. Sự tổng hợp nucleoside di- và triphosphate
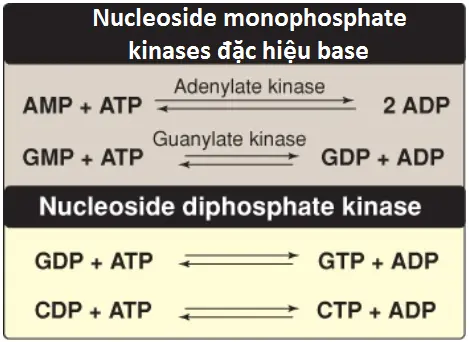
Nucleoside diphosphate được tổng hợp từ nucleoside monophosphates tương ứng bởi các nucleoside monophosphate kinases đặc hiệu base (Hình 9). (Chú ý: Các kinases này không phân biệt giữa ribose và deoxyribose trong cơ chất). ATP nhìn chung là nguồn phosphate được chuyển bởi vì nó xuất hiện với các nồng độ cao hơn các nucleoside triphosphates khác. Adenylate kinase thì đặc biệt hoạt động trong gan và trong cơ, nơi mà sự chuyển đổi năng lượng từ ATP thì cao. Chức năng của nó là duy trì cân bằng giữa các adenine nucleotide (AMP, ADP và ATP). Nucleoside diphosphates và triphosphates được chuyển đổi qua lại bởi nucleoside diphosphate kinase, một enzyme mà không giống như monophosphate kinases, có tính đặc hiệu cơ chất rộng.
G. Con đường thu hồi purine (purine salvage pathway)
Purines mà do sự thay thế bình thường của các nucleic acids của tế bào, hoặc các lượng nhỏ thu được từ chế độ ăn và không bị thoái hóa, có thể được chuyển thành nucleoside triphosphates và được sử dụng bởi cơ thể. Điều này đề cập đến con đường thu hồi đối với purines. (Chú ý: Sự thu hồi này thì cực kỳ quan trọng trong não).
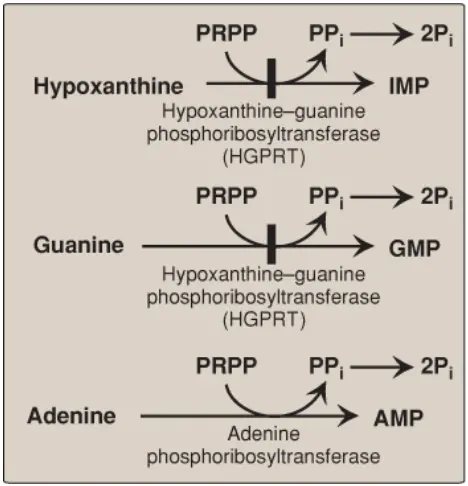
1. Sự thu hồi base purine thành nucleotides: Hai enzymes liên quan là: adenine phosphoribosyltransferase (APRT) và hypoxanthine-guanine phosphoribosyltransferase (HGPRT). Cả hai đều sử dụng PRPP như là một nguồn của nhóm ribose 5-phosphate (Hình 10). Sự giải phóng của pyrophosphate và sự thủy phân tiếp theo của nó khiến cho các phản ứng này không thể đảo ngược. (Chú ý: Adenosine là nucleoside purine duy nhất được thu hồi. Nó được phosphoryl hóa thành AMP bởi adenosine kinase).
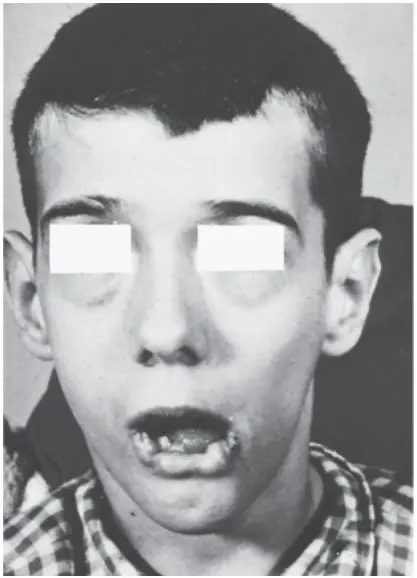
2. Hội chứng Lesch-Nyhan: Đây là một rối loạn lặn, liên kết NST X hiếm gặp liên quan với một sự thiếu hụt gần như hoàn toàn của HGPRT. Sự thiếu hụt gây ra một sự mất khả năng thu hồi hypoxanthine hay G, từ đó, các lượng dư của của uric acid, sản phẩm cuối cùng của sự thoái hóa purine, sau đó được tạo thành. Ngoài ta, sự thiếu hụt của con đường thu hồi này gây ra một sự tăng lên trong các mức PRPP và sự giảm trong các mức IMP và GMP. Kết quả, GPAT (bước điều hòa trong sự tổng hợp purine) có dư thừa cơ chất và giảm các chất ức chế có sẵn, và sự tổng hợp purine mới được tăng lên. Sự kết hợp của giảm tái sử dụng purine và tăng sự tổng hợp purine gây ra sự tăng thoái hóa của purines và sự sản xuất của các lượng lớn uric acid, khiến cho sự thiếu hụt HGPRT là một nguyên nhân di truyền của tăng uric acid máu. Ở những bệnh nhân mắc hội chứng Lesch-Nyhan, tăng uric acid máu thường gây ra sự hình thành của sỏi uric acid trong các thận (sỏi tiết niệu) và sự lắng đọng của các tinh thể urate trong các khớp (viêm khớp do gout) và các mô mềm. Ngoài ra, hội chứng được đặc trưng bởi rối loạn chức năng vận động, các sự suy giảm nhận thức và các rối loạn hành vi mà bao gồm cả cố gây thương tích cho bản thân (self-mutilation) (như cắn môi và các ngón tay), như được thể hiện trong Hình 11.
IV. Sự tổng hợp deoxyribonucleotide
Các nucleotides đã mô tả đều chứa ribose (ribonucleotides). Tuy nhiên, sự tổng hợp DNA cần 2’-deoxyribonucleotides, là thành phần được sản xuất từ ribonucleoside diphosphate bởi enzyme ribonucleotide reductase trong suốt pha S của chu kỳ tế bào. (Chú ý: Cùng enzyme tác động lên ribonucleotides pyrimidine).
A. Ribonucleotide reductase
Ribonucleotide reductase (ribonucleoside diphosphate reductase) là một dimer bao gồm hai tiểu đơn vị không giống nhau, R1 (hay α) và R2 nhỏ hơn (hay β) và đặc hiệu cho sự khử của purine nucleoside diphosphates (ADP và GDP) và pyrimidine nucleoside diphosphates (CDP và UDP) thành các dạng deoxy của chúng (dADP, dGDP, dCDP và dUDP). Các chất cho ngay lập tức các nguyên tử hydrogen cần cho sự khử của nhóm 2’-hydroxyl là hai nhóm sulfhydryl (-SH) trên chính enzyme (tiểu đơn vị R1), giúp hình thành nên một liên kết disulfide trong suốt phản ứng. (Chú ý: R2 chứa gốc tyrosyl ổn định cần cho sự xúc tác ở R1).
1. Sự tái tạo enzyme khử: Để ribonucleotide reductase tiếp tục sản xuất deoxyribonucleotides ở R1 thì liên kết disulfide được tạo ra trong suốt sự sản xuất của 2′-deoxy carbon phải được khử. Nguồn của các đương lượng khử là thioredoxin, một protein coenzyme của ribonucleotide reductase. Thioredoxin chứa hai gốc cysteine được phân tách bởi hai amino acids trong chuỗi peptide. Hai nhóm -SH của thioredoxin cho các nguyên tử hydrogen của chúng đến ribonucleotide reductase, hình thành nên một liên kết disulfide trong quá trình này (Hình 12).
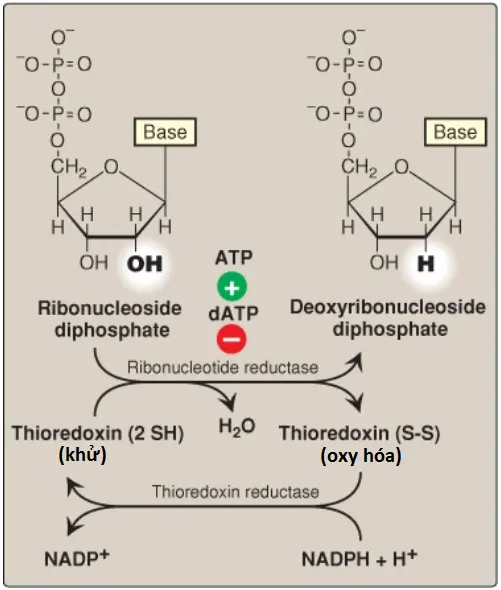
2. Sự tái tạo thioredoxin khử: Thioredoxin phải được chuyển trở lại dạng khử để tiếp tục thực hiện chức năng của nó. Các đương lượng khử được cung cấp bởi NADPH + H+ và phản ứng được xúc tác bởi thioredoxin reductase, một selenoprotein.
B. Sự điều hòa tổng hợp deoxyribonucleotide
Ribonucleotide reductase chịu trách nhiệm cho sự duy trì một sự cung cấp cân bằng của deoxyribonucleotides cần cho sự tổng hợp DNA. Kết quả, sự điều hòa của enzyme thì sẽ phức tạp. Ngoài vị trí xúc tác (đây là vị trí liên kết cơ chất nhé), R1 còn chứa hai vị trí dị lập thể riêng biệt liên quan đến việc điều hòa hoạt động enzyme (Hình 13).
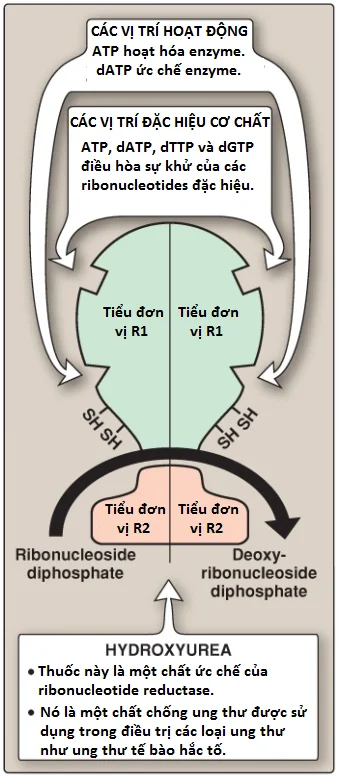
Áp dụng lâm sàng 1: Hydroxyurea
Thuốc hydroxyurea (hydroxycarbamide) ức chế ribonucleotide reductase, bằng cách đó, ức chế sự hình thành của các cơ chất cho sự tổng hợp DNA. Thuốc này là một thuốc chống ung thư và được sử dụng trong điều trị các ung thư như ung thư tế bào hắc tố da. Hydroxyurea cũng được sử dụng trong điều trị bệnh thiếu máu hồng cầu hình liềm. Tuy nhiên, sự tăng lên trong hemoglobin thai nhi được quan sát thấy với hydroxyurea là bởi vì các sự thay đổi trong sự biểu hiện gen và không phải do sự ức chế ribonucleotide reductase.
1. Các vị trí hoạt động (activity sites – không phải vị trí liên kết cơ chất nhé, cẩn thần nhầm): Sự liên kết của deoxyadenosine triphosphate (dATP) với các vị trí dị lập thể (được gọi là các vị trí hoạt động) trên R1 sẽ ức chế hoạt động xúc tác tổng quan của enzyme và, vì thế, ngăn cản sự khử của bất cứ một trong bốn nucleoside diphosphates. Điều này ngăn cản hiệu quả sự tổng hợp DNA và giải thích độc tính của các mức dATP tăng lên được quan sát thấy trong các tình trạng như thiếu hụt adenosine deaminase (ADA). Ngược lại, ATP liên kết với các vị trí này sẽ làm hoạt hóa enzyme.
2. Các vị trí đặc hiệu cơ chất (substrate specificity sites): Sự liên kết của nucleoside triphosphates với các vị trí dị lập thể khác (được gọi là các vị trí đặc hiệu cơ chất) trên R1 điều hòa tính đặc hiệu cơ chất, gây ra một sự tăng lên trong sự chuyển đổi của các loại ribonucleotides khác nhau thành deoxyribonucleotides khi chúng được cần cho sự tổng hợp DNA. Ví dụ, deoxythymidine triphosphate liên kết ở vị trí đặc hiệu gây ra một sự thay đổi cấu hình mà cho phép sự khử của GDP thành dGDP ở vị trí xúc tác khi ATP ở vị trí hoạt động.
Các bạn có thể xem bài viết mới trên Facebook tại đây: https://www.facebook.com/profile.php?id=61550892771585
Các bạn có thể xem bài viết trước tại đây: https://docsachxyz.com/amino-acids-su-chuyen-doi-thanh-cac-san-pham-chuyen-biet-phan-3/
Cảm ơn các bạn đã theo dõi bài viết. Hẹn gặp lại các bạn trong các bài viết tiếp theo nhé !!!





































