I. Tổng quan
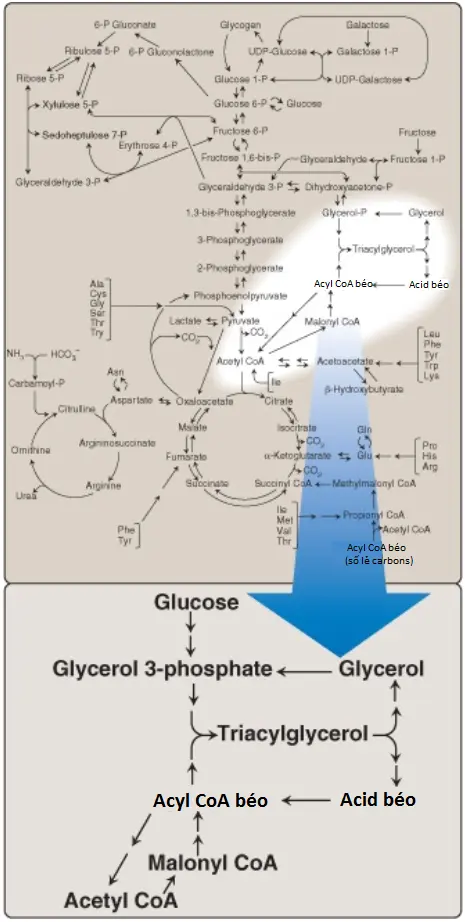
Các acids béo tồn tại ở dạng tự do trong cơ thể (nghĩa là chúng không được ester hóa) và dưới dạng các acyl esters béo (fatty acyl esters) trong các phân tử phức tạp hơn như triacylglycerol (TAGs). Các mức thấp của các acids béo tự do (free fatty acids – FFA) xuất hiện trong tất cả các mô, nhưng các lượng đáng kể đôi khi có thể được tìm thấy trong huyết tương, đặc biệt là trong suốt quá trình đói. FFA huyết tương (được vận chuyển trên albumin huyết thanh) thì đi theo một chặng từ nguồn gốc ban đầu (TAG của các mô mỡ hoặc các lipoproteins tuần hoàn) đến vị trí tiêu thụ của nó (hầu hết các mô). FFA có thể bị oxy hóa bởi nhiều mô, đặc biệt là gan và cơ, để cung cấp năng lượng và, trong gan, để cung cấp cơ chất cho sự tổng hợp thể ketone. Các acids béo cũng là các thành phần cấu trúc của các lipids màng, như phospholipids và glycolipids (xem các bài viết sau). Các acids béo nối với các proteins nhất định làm tăng cường khả năng của các proteins đó trong việc liên kết với màng. Các acids béo cũng là các tiền thân của prostaglandins giống hormone (hormone-like) (xem các bài viết tiếp theo). Các acids béo được ester hóa, ở dạng TAG được tích trữ trong mô mỡ trắng (white adipose tissue – WAT), đóng vai trò như là nguồn tích trữ năng lượng chính của cơ thể. Các sự thay đổi trong sự chuyển hóa acid béo thì có liên quan với béo phì và đái tháo đường. Hình 1 minh họa các con đường chuyển hóa của sự tổng hợp và thoái hóa acid béo và mối liên hệ của chúng với sự chuyển hóa carbohydrate.
II. Cấu trúc acid béo
Một acid béo chứa một chuỗi hydrocarbon kỵ nước với một nhóm carboxyl tận mà có pKa là khoảng 4.8 (Hình 2). Ở pH sinh lý, nhóm carboxyl tận cùng (-COOH) ion hóa, trở thành -COO–. (Chú ý: Khi pH lớn hơn pK thì dạng deproton hóa sẽ chiếm ưu thế). Nhóm anion này có một ái tính với nước, tạo ra bản chất lưỡng tính của acid béo (có cả một vùng ưa nước và kỵ nước). Tuy nhiên, đối với các acid béo chuỗi dài (long-chain-length fatty acids – LCFA), phần kỵ nước thì sẽ chiếm ưu thế. Các phân tử này thì rất không tan trong nước và phải được vận chuyển trong hệ thống tuần hoàn trong mối liên hệ với protein. Hơn 90% các acids béo được tìm thấy trong huyết tương là ở dạng các esters của acid béo (chủ yếu là TAG, cholesteryl esters và phospholipids) chứa trong các phần tử lipoprotein tuần hoàn (xem các bài viết tiếp theo). FFA được vận chuyển trong hệ thống tuần hoàn trong mối liên hệ với albumin, protein nhiều nhất trong huyết thanh.

A. Sự bão hòa của acid béo
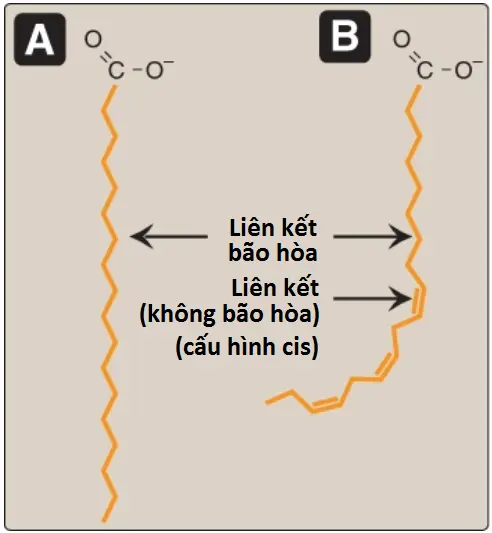
Các chuỗi acid béo có thể không chứa liên kết đôi (nghĩa là bão hòa [saturated]) hoặc chứa một hoặc nhiều liên kết đôi (nghĩa là không bão hòa đơn hoặc đa [monounsaturated or polyunsaturated]). Ở người, phần lớn là ở dạng bão hòa hoặc không bão hòa đơn. Khi các liên kết đôi xuất hiện, chúng thì gần như luôn luôn ở cấu hình dạng cis chứ không ở dạng trans. Sự xuất hiện của một liên kết đôi dạng cis làm cho acid béo bị gập ở vị trí đó (Hình 3). Nếu như acid béo có hai hoặc nhiều liên kết đôi, chúng luôn luôn cách nhau ở một khoảng cách 3 carbons. (Chú ý: Nhìn chung, việc thêm vào các liên kết đôi làm giảm nhiệt độ nóng chảy [Tm] của một acid béo, ngược lại, tăng chiều dài chuỗi sẽ làm tăng Tm. Bởi vì các lipids của màng nhìn chung là thường chứa LCFA nên sự xuất hiện của các liên kết đôi trong một số acid béo giúp duy trì bản chất dạng lỏng của các lipids đó. Xem các bài viết sau để bàn luận về việc xuất hiện trong chế độ ăn của các acids béo không bão hòa dạng cis và dạng trans).
B. Chiều dài chuỗi acid béo và các vị trí liên kết đôi
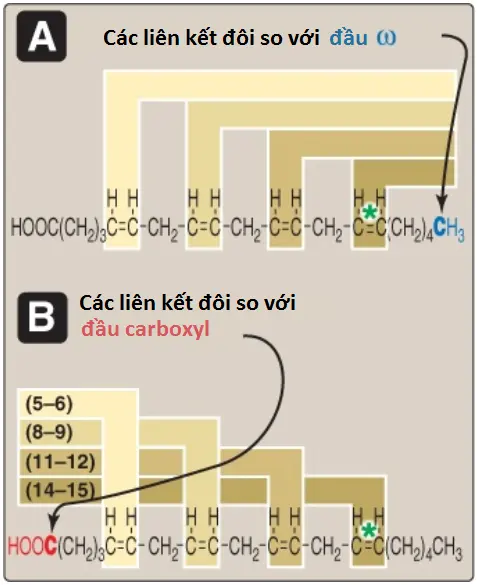
Các tên và các cấu trúc thông thường của một số acids béo có tầm quan trọng sinh lý được liệt kê trong Hình 4. Ở người, các acids béo có một số chẵn nguyên tử carbon (16, 18 hay 20) chiếm ưu thế, với các acids béo dài hơn (>22 carbons) được tìm thấy trong não bộ. Các nguyên tử carbon được đánh số, bắt đầu với carbon của carbonyl là carbon số 1. Số trước dấu hai chấm chỉ số carbons trong chuỗi và các số sau dấu hai chấm chỉ số lượng và vị trí (so với đầu carboxyl) của các liên kết đôi. Ví dụ, như được phản ánh trong Hình 4, arachidonic acid, 20:4(5,8,11,14), thì dài 20 carbons và có 4 liên kết đôi (giữa các carbons 5-6, 8-9, 11-12 và 14-15). (Chú ý: Carbon thứ hai, carbon mà nhóm carboxyl liên kết vào, cũng được gọi là α-carbon, carbon thứ 3 là β-carbon và carbon thứ 4 là γ-carbon. Carbon của nhóm methyl tận cùng được gọi là ω-carbon bất kể chiều dài của chuỗi). Các liên kết đôi trong một acid béo cũng có thể được tham chiếu so với đầu omega (methyl) của chuỗi. Arachidonic acid thì được gọi là một acid béo ω-6 bởi vì liên kết đôi tận cùng cách 6 liên kết tính từ đầu ω (Hình 5A). (Chú ý: Việc ký hiệu tương đương là n-6 cũng có thể được sử dụng [Hình 5B]). Một acid béo ω-6 khác là linoleic acid thiết yếu 18:2(9,12). Ngược lại, alpha-linolenic acid, 18:3(9,12,15), là một acid béo ω-3 thiết yếu.

C. Các acids béo thiết yếu
Linoleic acid, tiền thân của arachidonic acid ω-6 mà là cơ chất cho sự tổng hợp prostaglandins và alpha-linolenic acid, tiền thân của các acid béo omega-3 mà quan trọng đối với sự tăng trưởng và phát triển, là các acid béo thiết yếu trong chế độ ăn ở người bởi vì chúng ta thiếu đi các enzymes mà có thể hình thành nên các liên kết đôi carbon-carbon sau carbon thứ 9 tính từ đầu methyl (ω) của một acid béo. Các thực phẩm thực vật cung cấp cho chúng ta các loại acids béo thiết yếu này. (Chú ý: Arachidonic acid trở nên thiết yếu nếu như linoleic acid bị thiếu trong chế độ ăn. Xem các bài viết tiếp theo trong sự bàn luận về tầm quan trọng của các acids béo ω-3 và ω-6).
Sự thiếu hụt acid béo thiết yếu (hiếm) có thể gây ra viêm da khô và bong vảy do sự mất khả năng trong việc tổng hợp các phân tử mà hình thành hàng rào nước (water barrier) trong da.
III. Sự tổng hợp mới acid béo
Các carbohydrates và proteins thu được từ chế độ ăn mà vượt quá các nhu cầu của cơ thể đối với các chất dinh dưỡng này thì có thể được chuyển thành các acids béo. Ở người trưởng thành, sự tổng hợp acid béo mới xảy ra chủ yếu trong gan và các tuyến vú đang tạo sữa và, với một mức độ ít hơn, là trong mô mỡ. Quá trình bào tương này là nội sinh và khử. Nó tích hợp các carbons từ acetyl coenzyme A (CoA) vào trong chuỗi acid béo đang phát triển, sử dụng ATP và nicotinamide adenine dinucleotide phosphate khử (NADPH). (Chú ý: TAG trong chế độ ăn cũng cung cấp các acids béo. Xem các bài viết tiếp theo cho việc bàn luận về sự chuyển hóa các chất dinh dưỡng trong chế độ ăn ở trạng thái no).
A. Sự sản xuất acetyl CoA của bào tương
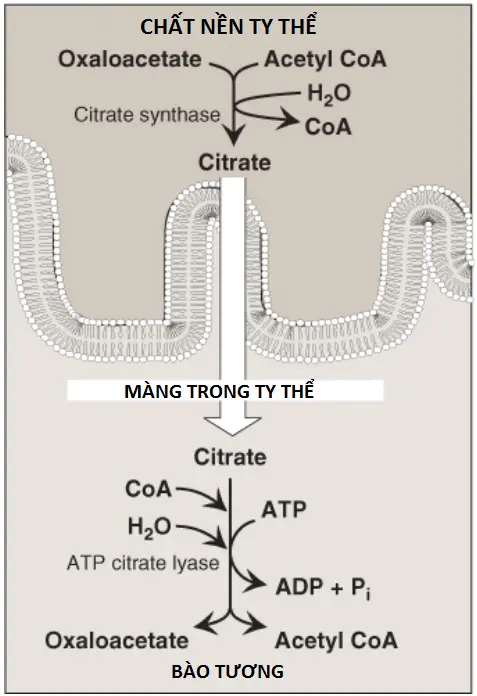
Bước đầu tiên trong sự tổng hợp acid béo là sự chuyển các đơn vị acetate từ acetyl CoA của ty thể đến bào tương. Acetyl CoA của ty thể được sản xuất bởi sự oxy hóa của pyruvate (xem các bài viết trước) và bởi sự dị hóa của các amino acids nhất định (xem các bài viết sau). Tuy nhiên, phần CoA của acetyl CoA không thể đi qua màng trong ty thể, và chỉ phần acetyl đi vào được trong bào tương. Do đó, nó chuyển acetyl CoA vào trong bào tương như là một phần của citrate được sản xuất bởi sự ngưng tụ acetyl CoA với oxaloacetate (OAA) bởi citrate synthase (Hình 6). (Chú ý: Sự vận chuyển citrate đến bào tương xảy ra khi nồng độ citrate ty thể cao. Điều này được quan sát thấy khi isocitrate dehydrogenase của chu trình tricarboxylic acid [chu trình TCA] bị ức chế bởi sự có mặt của các lượng lớn ATP, làm cho citrate và isocitrate tích tụ lại. Vì thế, citrate bào tương có thể được xem như là một tín hiệu cao năng lượng. Bởi vì một lượng lớn ATP thì cần cho sự tổng hợp của acid béo nên sự tăng lên trong cả ATP và citrate sẽ làm tăng cường con đường này). Trong bào tương, citrate bị phân tách thành OAA và acetyl CoA bởi ATP citrate lyase.
B. Sự carboxyl hóa acetyl CoA thành malonyl CoA
Năng lượng cho các sự ngưng tụ carbon-đến-carbon (carbon-to-carbon) trong quá trình tổng hợp acid béo được cung cấp bởi sự carboxyl hóa và sau đó decarboxyl hóa của các nhóm acyl trong bào tương. Sự carboxyl hóa của acetyl CoA thành maloyl CoA được xúc tác bởi acetyl CoA carboxylase (ACC) (Hình 7). ACC chuyển carbon dioxide (CO2) từ bicarbonate (HCO3–) trong một phản ứng cần ATP. Coenzyme là biotin (vitamin B7), là thành phần liên kết cộng hóa trị với một gốc lysyl của carboxylase. ACC carboxyl hóa biotin liên kết, thành phần giúp chuyển nhóm carboxyl hoạt hóa đến acetyl CoA.
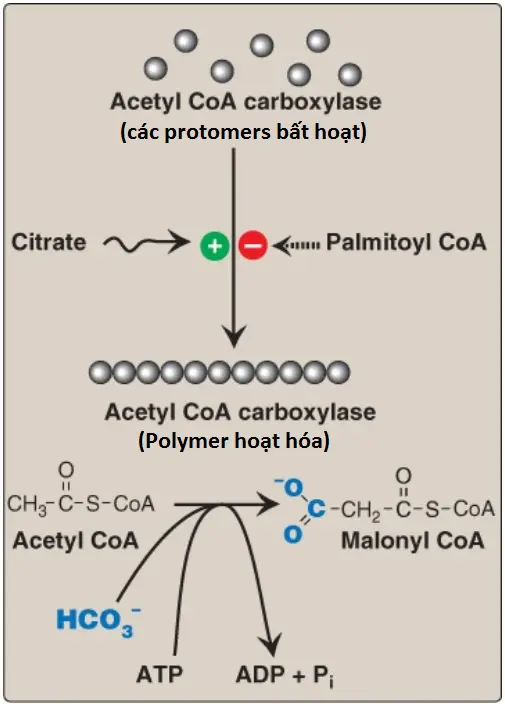
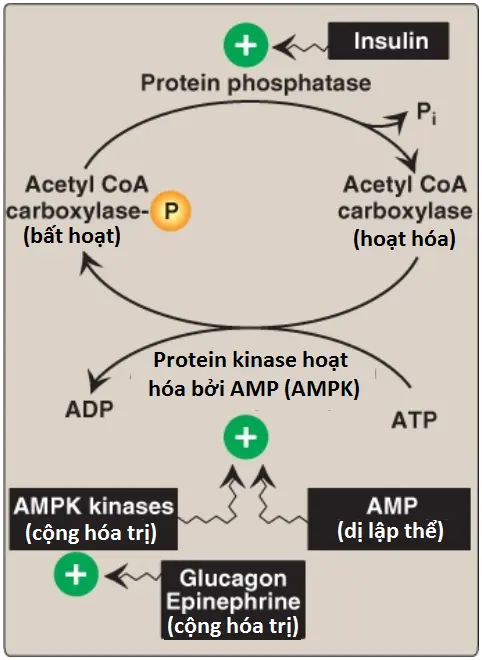
1. Sự điều hòa ngắn hạn của acetyl CoA carboxylase: Sự carboxyl hóa này vừa là bước giới hạn tốc độ vừa là bước điều hòa trong sự tổng hợp acid béo (xem Hình 7). Dạng bất hoạt của ACC là một protomer (phức hợp của 2 polypeptides hoặc nhiều hơn). Enzyme được hoạt hóa về mặt dị lập thể bởi citrate, chất mà làm cho các protomers polymer hóa và được bất hoạt dị lập thể bởi palmitoyl CoA (sản phẩm cuối cùng của con đường), chất mà gây ra sự depolymer hóa. Một cơ chế thứ hai của sự điều hòa ngắn hạn là bởi sự phosphoryl hóa có thể đảo ngược. Protein kinase hoạt hóa bởi adenosine monophosphate (adenosine monophosphate–activated protein kinase – AMPK) phosphoryl hóa và bất hoạt ACC. Chính AMPK được hoạt hóa dị lập thể bởi AMP và cộng hóa trị bởi sự phosphoryl hóa thông qua một số kinases. Ít nhất một trong số các AMPK kinase này được hoạt hóa bởi protein kinase A (PKA) phụ thuộc AMP vòng (cyclic AMP – cAMP). Vì thế, trong sự có mặt của các hormone điều hòa ngược (counterregulatory hormones), như epinephrine và glucagon, ACC bị phosphoryl hóa và bất hoạt (Hình 8). Trong sự có mặt của insulin, ACC bị dephosphoryl hóa và hoạt hóa. (Chú ý: Điều này tương tự với sự điều hòa của glycogen synthase [xem các bài viết trước]).
2. Sự điều hòa dài hạn của acetyl CoA carboxylase: Sự tiêu thụ một chế độ ăn thừa calories kéo dài (đặc biệt là các chế độ ăn nhiều carbohydrate, ít chất béo) gây ra một sư tăng lên trong sự tổng hợp ACC, bằng cách đó, làm tăng sự tổng hợp acid béo. Một chế độ ăn thấp calories hoặc một chế độ ăn nhiều chất béo, ít carbohydrate có tác động trái ngược. (Chú ý: Sự tổng hợp ACC thì được tăng điều hòa (upregulate) bởi carbohydrate [đặc biệt là glucose] thông qua yếu tố phiên mã protein liên kết thành phần đáp ứng carbohydrate [carbohydrate response element–binding protein – ChREBP] và bởi insulin thông qua yếu tố dịch mã protein-1c liên kết thành phần điều hòa sterol [sterol regulatory element–binding protein-1c – SREBP-1c]. Acid béo synthase (fatty acid synthase – FAS) [xem phần C bên dưới] thì được điều hòa một cách tương tự. Chức năng và sự điều hòa của SREBP sẽ được mô tả trong các bài viết tiếp theo nhé). Metformin, được sử dụng trong điều trị đái tháo đường type 2, giúp làm giảm TAG huyết tương thông qua sự hoạt hóa của AMPK, gây ra sự ức chế hoạt động của ACC (bằng sự phosphoryl hóa) và sự ức chế biểu hiện của ACC và FAS (bằng việc làm giảm SREBP-1c). Metformin làm giảm glucose máu bằng cách làm tăng sự hấp thu glucose qua trung gian AMPK bởi cơ.
C. Sự tổng hợp acid béo ở sinh vật nhân thực
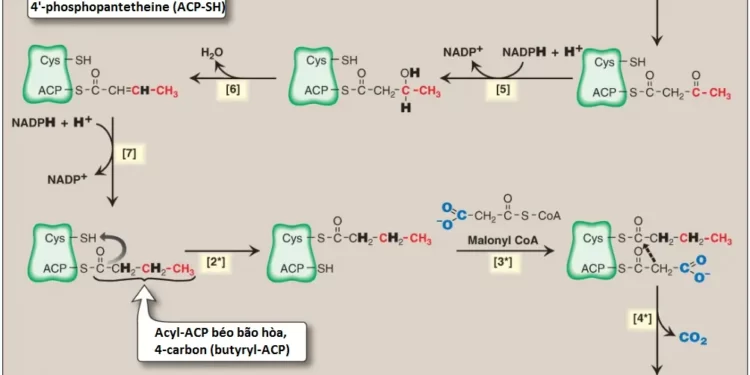
Các chuỗi phản ứng còn lại của sự tổng hợp acid béo ở các sinh vật nhân thực được xúc tác bởi enzyme dimer đồng nhất (homodimeric) đa chức năng FAS. Quá trình liên quan với sự bổ sung của hai carbons từ malonyl CoA đến đầu carboxyl của một chuỗi các chất nhận acyl. Mỗi monomer FAS là một polypeptide đa xúc tác với 6 miền enzyme khác nhau cùng với một miền protein mang acyl (acyl carrier protein – ACP) chứa 4’-phosphopantetheine. 4’-phosphopantetheine, một dẫn xuất của pantothenic acid (vitamin B5, xem các bài viết tiếp theo), mang các đơn vị acyl trên nhóm thiol (-SH) tận cùng của nó và trình diện chúng đến các miền xúc tác của FAS trong suốt quá trình tổng hợp acid béo. Nó cũng là một thành phần của CoA. Phản ứng đánh số trong dấu ngoặc tròn bên dưới đề cập đến Hình 9.
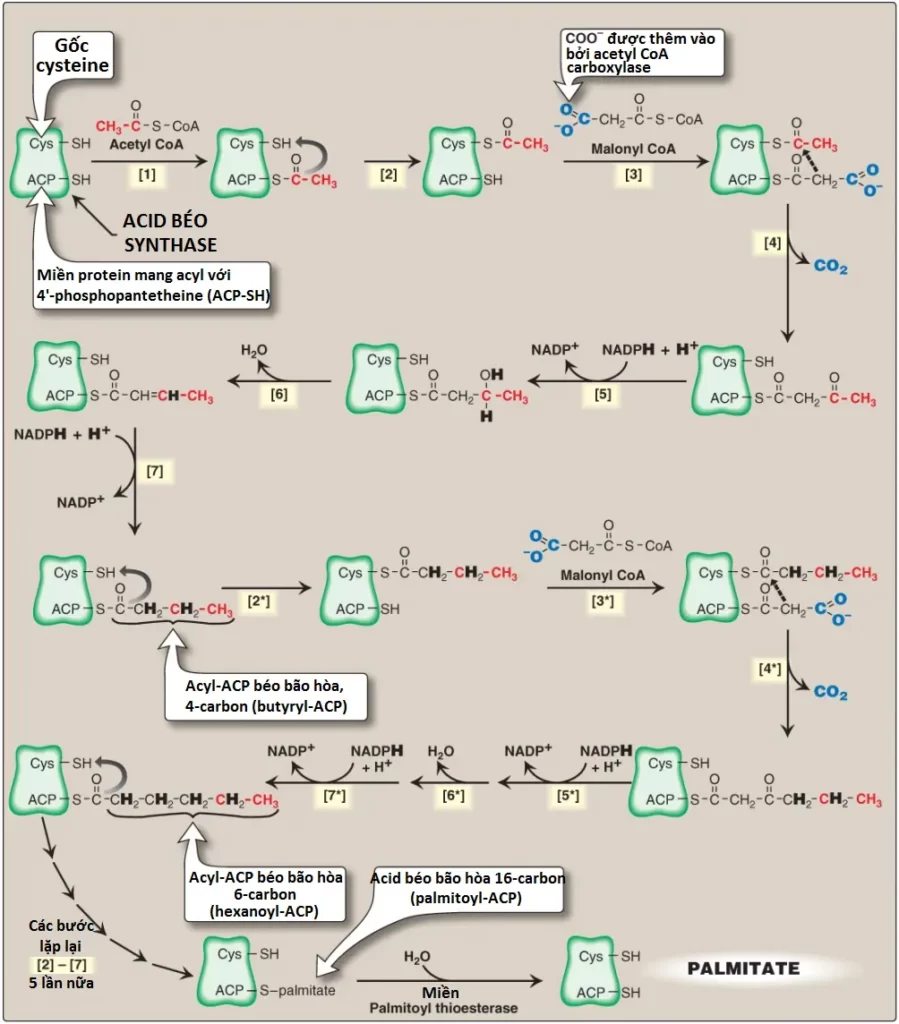
(1) Một nhóm acetyl được chuyển từ acetyl CoA đến nhóm -SH của ACP.
(2) Tiếp theo, mảnh hai carbons này được chuyển đến một vị trí giữ tạm thời.
(3) ACP trống bây giờ nhận một nhóm malonyl 3 carbons từ malonyl CoA.
(4) Nhóm acetyl trên gốc cysteine ngưng tụ với nhóm malonyl trên ACP cùng với sự giải phóng của CO2, là thành phần ban đầu thêm bởi ACC. Kết quả là một đơn vị 4 carbons nối với miền ACP.
Ba phản ứng tiếp theo sẽ chuyển nhóm 3-ketoacyl thành nhóm acyl bão hòa tương ứng bởi một cặp quá trình khử cần NADPH và một bước dehydrat hóa.
(5) Nhóm keto bị khử thành một rượu.
(6) Một phân tử nước bị loại bỏ, tạo ra một liên kết đôi trans giữa hai carbons 2 và 3 (α-carbon và β-carbon).
(7) Liên kết đôi bị khử.
Trình tự các bước này tạo ra một nhóm 4 carbons (butyryl) mà 3 carbons tận cùng của nó thì bão hoàn hoàn toàn và carbon còn lại gắn với miền ACP. Các bước được lặp lại (biểu thị bởi dấu sao), bắt đầu với việc chuyển đơn vị butyryl từ ACP đến gốc cysteine [2*], sự nối của một nhóm malonyl vào ACP [3*] và sự ngưng tụ của hai nhóm giải phóng ra CO2 [4*]. Nhóm carbonyl ở β-carbon (carbon 3, carbon thứ 3 tính từ lưu huỳnh) sau đó được khử [5*], dehydrate hóa [6*] và khử [7*], tạo thành hexanoyl-ACP. Chu trình các phản ứng này được lặp lại cho đến khi acid béo đạt đến một độ dài là 16 carbons. Hoạt động xúc tác cuối cùng của FAS, phân tách liên kết thioester, giải phóng phân tử palmitate bão hòa hoàn toàn (16:0). (Chú ý: Tất cả carbons trong palmitic acid đều đi qua malonyl CoA trừ hai carbons được cho bởi acetyl CoA ban đầu [chất nhận acyl đầu tiên], mà được tìm thấy ở đầu methyl [ω] của acid béo. Điều này nhấn mạnh bản chất giới hạn tốc độ của phản ứng ACC). Các acid béo chuỗi ngắn hơn chỉ được sản xuất trong tuyến vú đang tạo sữa.
D. Các nguồn chất khử
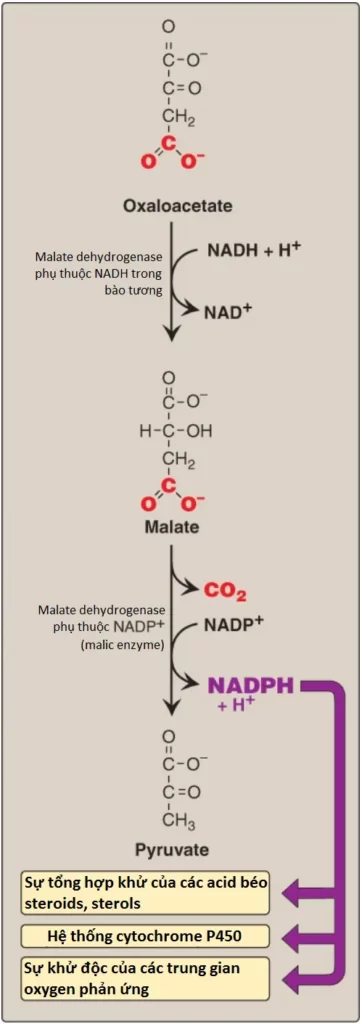
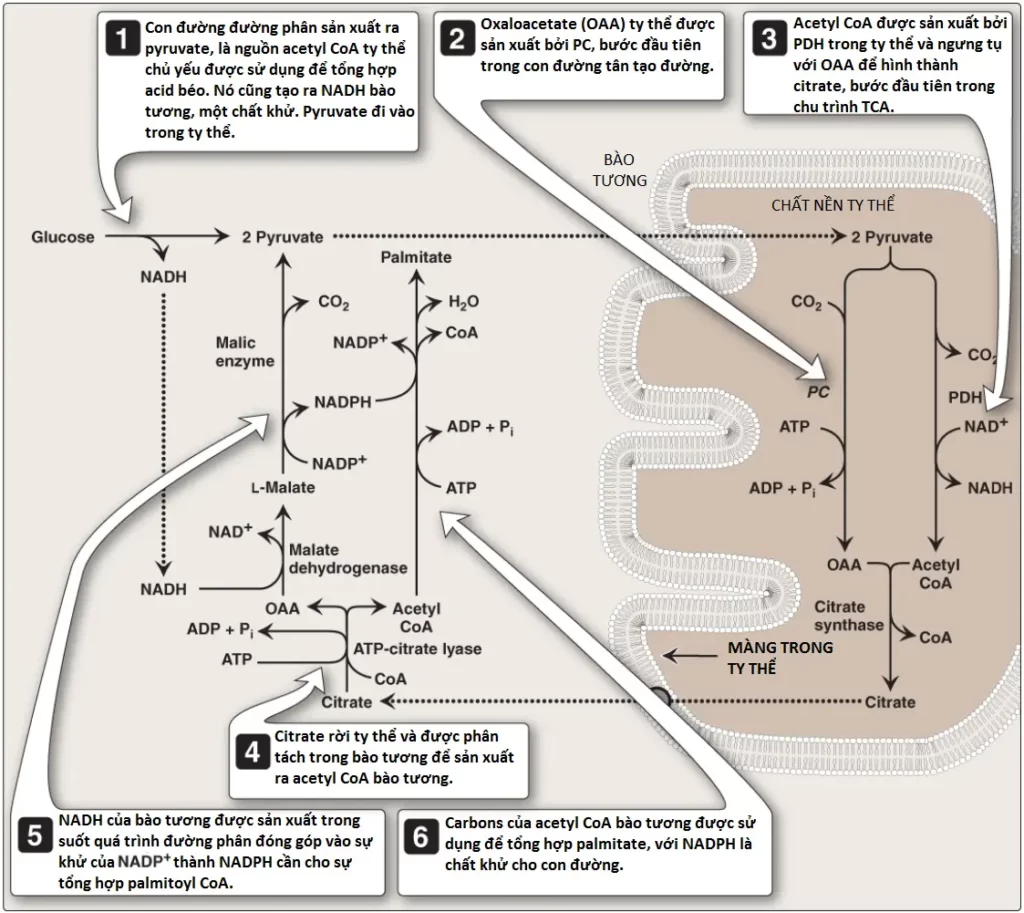
Sự tổng hợp của một palmitate cần 14 NADPH, một chất khử (reductant – reducing agent). Con đường pentose phosphate (xem các bài viết trước) là một nguồn cung cấp NADPH chính. Hai NADPH được tạo ra cho mỗi phân tử glucose 6-phosphate mà đi vào trong con đường này. Sự chuyển đổi malate thành pyruvate trong bào tương mà trong đó malate bị oxy hóa và decarboxyl hóa bởi malic enzyme bào tương (malate dehydrogenase phụ thuộc NADP+), tạo ra NADPH bào tương (và CO2), như được thể hiện trong Hình 10. (Chú ý: Malate có thể có nguồn gốc từ sự khử của OAA bởi malate dehydrogenase phụ thuộc NADH bào tương [xem Hình 10]. Một nguồn NADH bào tương cần cho phản ứng này là quá trình đường phân. Cuối cùng, OAA có thể có nguồn gốc từ sự phân tách citrate bởi ATP citrate lyase). Một sự tóm tắt của mối liên hệ giữa chuyển hóa glucose và tổng hợp palmitate được thể hiện trong Hình 11.
E. Sự kéo dài nhiều hơn nữa
Mặc dù palmitate, một LCFA dài 16 carbons, bão hòa hoàn toàn (16:0), là sản phẩm cuối cùng chính của hoạt động FAS nhưng nó có thể được kéo dài nhiều hơn nữa bởi sự bổ sung các đơn vị 2 carbons vào đầu carboxylate chủ yếu trong lưới nội chất trơn (smooth endoplasmic reticulum – SER). Sự kéo dài cần một hệ thống các enzymes riêng lẻ chứ không phải là một enzyme đa chức năng. Malonyl CoA là chất cho 2 carbons và NADPH cung cấp các electron. Não có các khả năng kéo dài chuỗi acid béo thêm, cho phép nó sản xuất ra các acid béo chuỗi rất dài ([VLCFA] dài hơn 22 carbons) mà cần cho sự tổng hợp của các lipids não.
F. Sự giảm bão hòa chuỗi
Các enzymes (acyl CoA béo desaturases [fatty acyl CoA desaturases]) cũng xuất hiện trong SER mà chịu trách nhiệm cho sự giảm bão hòa LCFA (nghĩa là thêm các liên kết đôi cis). Các phản ứng giảm bão hòa cần oxygen (O2), NADH, cytochrome b5 và reductase liên kết flavin adenine dinucleotide (FAD) (flavin adenine dinucleotide [FAD]-linked reductase) của nó. Acid béo và NADH bị oxy hóa khi O2 bị khử thành H2O. Liên kết đôi đầu tiên thường chèn giữa carbon 9 và carbon 10, tạo ra chủ yếu oleic acid, 18:1(9) và các lượng nhỏ của palmitoleic acid, 16:1(9). Nhiều loại acids béo không bão hòa đa có thể được tạo thành thông qua sự giảm bão hòa kết hợp với sự kéo dài chuỗi.
Con người có các desaturases của carbon thứ 9, 6, 5 và 4 nhưng thiếu khả năng tạo các liên kết đôi từ carbon thứ 10 tính từ đầu ω của chuỗi. Điều này tạo ra tính thiết yếu về mặt dinh dưỡng của acid linoleic ω-6 không bão hòa đa và acid linolenic ω-3 không bão hòa đa.
G. Tích trữ dưới dạng các thành phần TAG
Mono-, di- và triacylglycerol bao gồm một, hai hoặc ba phân tử acid béo được ester hóa với một phân tử glycerol. Các acid béo được ester hóa thông qua các nhóm carboxyl của chúng, tạo ra một sự mất tích điện âm và hình thành nên chất béo trung tính. (Chú ý: Một acylglycerol mà ở thể rắn ở nhiệt độ phòng thì được gọi là mỡ. Nếu ở dạng lỏng thì được gọi là dầu.)
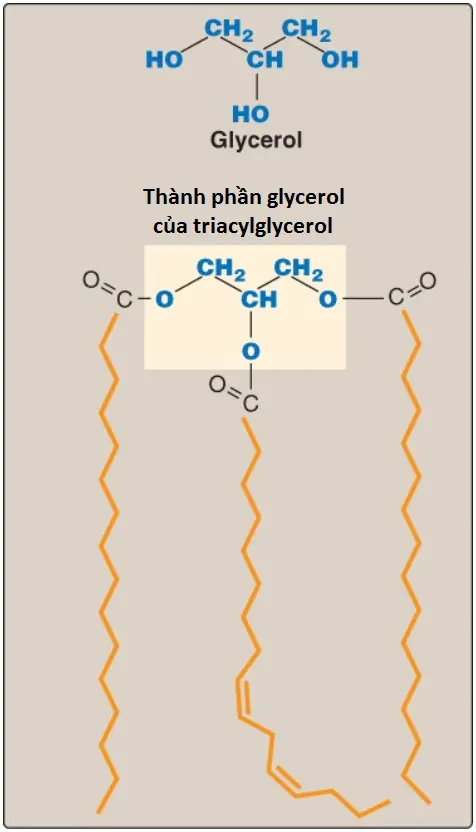
1. Sự sắp xếp: 3 acid béo được ester hóa với một phân tử glycerol để hình thành nên một TAG thường không không cùng loại. Acid béo trên carbon 1 thường bão hòa, trên carbon 2 thường không bão hòa và trên carbon 3 có thể là một trong hai. Nhớ lại rằng là sự có mặt của các acid béo không bão hòa sẽ làm giảm nhiệt độ chảy của lipid. Một ví dụ về một phân tử TAG được thể hiện trong Hình 12.
2. Sự tích trữ và chức năng triacylglycerol: Bởi vì TAG chỉ hơi tan trong nước và không thể hình thành nên các micelles ổn định bởi chính nó nên chúng sẽ kết tụ bên trong các tế bào mỡ trắng để hình thành nên các giọt dầu lớn mà gần như khan (không chứa nước). Các giọt lipid bào tương này là sự tích trữ năng lượng chính của cơ thể. (Chú ý: TAG tích trữ trong các tế bào mỡ nâu đóng vai trò như là một nguồn nhiệt thông qua sự tạo nhiệt không do run [nonshivering thermogenesis] [xem các bài viết trước]).
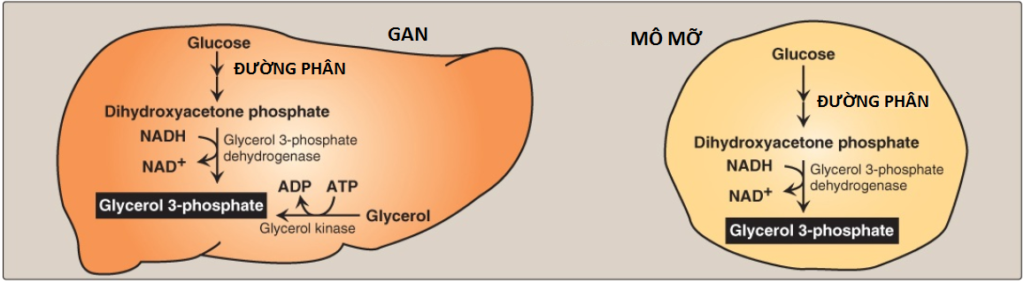
3. Sự tổng hợp glycerol 3-phosphate: Glycerol 3-phosphate là chất nhận acid béo ban đầu trong suốt quá trình tổng hợp TAG. Có hai con đường chính cho sự tổng hợp của nó (Hình 13). (Chú ý: Một quá trình thứ 3 [quá trình tân tạo glycerol – glyceroneogenesis] sẽ được mô tả trong các bài viết tiếp theo). Trong cả gan (vị trí tổng hợp TAG chủ yếu) và mô mỡ, glycerol 3-phosphate có thể được sản xuất từ glucose, đầu tiên sử dụng các phản ứng của con đường đường phân để sản xuất dihydroacetone phosphate [DHAP]. DHAP bị khử bởi glycerol 3-phosphate dehydrogenase thành glycerol 3-phosphate. Một con đường thứ hai được tìm thấy trong gan nhưng không có trong mô mỡ, sử dụng glycerol kinase để chuyển glycerol tự do thành glycerol 3-phosphate (xem Hình 13). (Chú ý: Chất vận chuyển glucose trong các tế bào mỡ [GLUT-4] thì phụ thuộc insulin [xem các bài viết tiếp theo]. Vì thế, khi các mức glucose huyết tương thấp, các tế bào mỡ chỉ có một khả năng giới hạn để tổng hợp glycerol phosphate và không thể tạo ra TAG mới).
4. Sự hoạt hóa acid béo: Một FFA phải được chuyển thành dạng hoạt hóa của nó (liên kết với CoA thông qua một liên kết thioester) trước khi nó có thể tham gia vào các quá trình chuyển hóa như sự tổng hợp TAG. Phản ứng này, được minh họa trong Hình 6 của bài viết trước, được xúc tác bởi một họ các acyl CoA béo synthetases (thiokinases) (fatty acyl CoA synthetases [thiokinases]).
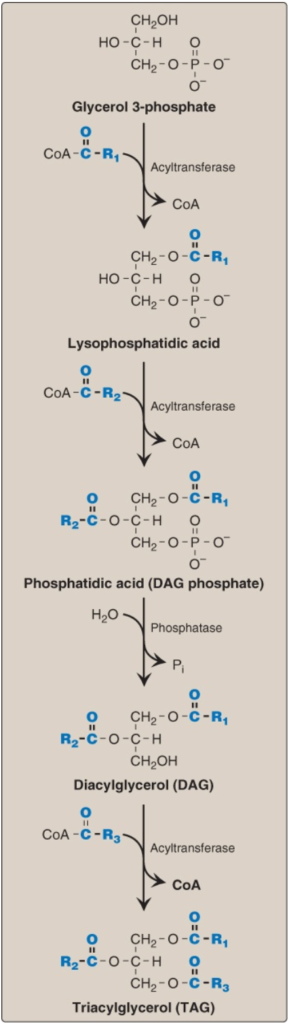
5. Sự tổng hợp triacylglycerol: Con đường này từ glycerol 3-phosphate liên quan với 4 phản ứng, được thể hiện trong Hình 14. Các phản ứng này bao gồm sự bổ sung tuần tự của 2 acids béo từ acyl CoA béo (fatty acyl CoA), sự loại bỏ phosphate và sự bổ sung của acid béo thứ ba.
H. Số phận triacylglycerol trong gan và trong mô mỡ
Trong mô mỡ trắng, TAG được tích trữ ở dạng gần như khan dưới dạng các giọt chất béo trong bào tương của các tế bào. Các giọt chất béo được phủ bởi một họ các protein được gọi là perilipins mà giúp cô lập và bảo vệ TAG khỏi sự phân giải lipid cho đến khi cơ thể cần các acids béo để sinh năng lượng. (Perilipins có thể đóng vai trò trong các tình trạng bệnh lý như đái tháo đường type 2, xơ vữa động mạch và bệnh tim mạch). Ít TAG được tích trữ trong gan khỏe mạnh. Thay vào đó, hầu hết được xuất ra ngoài, đóng gói cùng với các lipids khác và apolipoprotein để hình thành nên các phần tử lipoprotein được gọi là các lipoproteins mật độ rất thấp (very–low-density lipoproteins – VLDL). VLDL mới tạo ra được tiết một cách trực tiếp vào trong máu nơi mà chúng sẽ trưởng thành và thực hiện chức năng vận chuyển các lipids có nguồn gốc nội sinh đến các mô ngoại vi. (Chú ý: Nhớ lại các bài viết trước, khi mà chylomicrons vận chuyển các lipids trong chế độ ăn [các lipids có nguồn gốc ngoại sinh]. Các lipoproteins trong huyết tương sẽ được bàn đến trong các bài viết tiếp theo).
Các bạn có thể xem bài viết mới trên Facebook tại đây: https://www.facebook.com/profile.php?id=61550892771585
Các bạn có thể xem bài viết trước tại đây: https://docsachxyz.com/su-chuyen-hoa-lipid-chat-beo-trong-che-do-an/
Cảm ơn các bạn đã theo dõi bài viết. Hẹn gặp lại các bạn trong các bài viết tiếp theo nhé !!!