I. Tổng quan về trạng thái hấp thu (absorptive state)
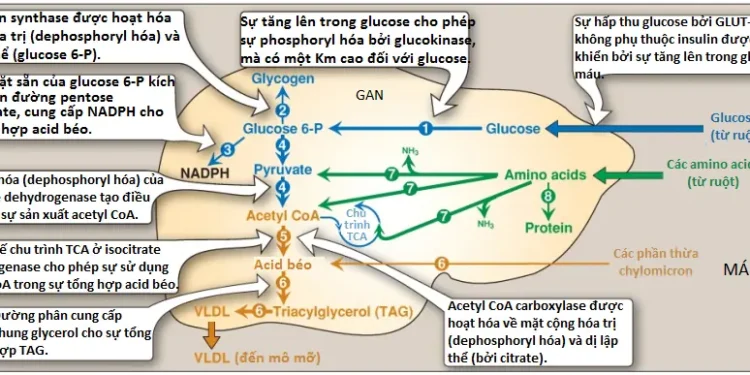
Trạng thái hấp thu (absorptive state) (trạng thái ăn no [well-fed state]) là khoảng thời gian 2 đến 4 giờ sau khi ăn một bữa ăn bình thường. Trong suốt khoảng thời gian này, các sự tăng lên tạm thời trong mức glucose, amino acids và triacylglycerols (TAG) huyết tương xuất hiện, TAG chủ yếu là thành phần của chylomicrons được tổng hợp và được bài tiết bởi các tế bào niêm mạc ruột. Mô tiểu đảo của tuyến tụy đáp ứng với sự bài tiết incretin của đường tiêu hóa và mức glucose tăng lên với sự tăng bài tiết insulin và giảm bài tiết glucagon. Tỷ số insulin/glucagon tăng lên và sự có mặt sẵn của các cơ chất tuần hoàn khiến trạng thái hấp thu trở thành một giai đoạn đồng hóa được đặc trưng bởi sự tăng tổng hợp và tích trữ TAG và glycogen để làm đầy lại các sự tích trữ nguyên liệu cũng như là tăng tổng hợp protein. Trong suốt giai đoạn hấp thu này, hầu như tất cả các mô sử dụng glucose như là một nguyên liệu và đáp ứng chuyển hóa của cơ thể được chi phối bởi các sự thay đổi trong chuyển hóa của gan, mô mỡ, cơ xương và não. Trong loạt bài viết này, một “sơ đồ cơ quan” (organ map) được giới thiệu để hiểu được sự di chuyển của các chất chuyển hóa giữa các mô. Mục tiêu là tạo ra một cái nhìn bao quát và hữu ích về mặt lâm sàng của quá trình chuyển hóa trên toàn bộ cơ thể.
II. Các cơ chế điều hòa
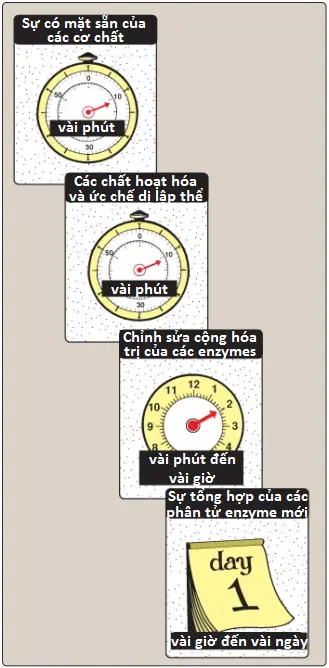
Dòng các chất trung gian qua các con đường chuyển hóa được kiểm soát bởi bốn cơ chế: (1) sự có mặt sẵn của các cơ chất, (2) sự điều hòa dị lập thể của các enzymes, (3) sự chỉnh sửa cộng hóa trị của các enzymes, và (4) sự cảm ứng-sự ức chế của sự tổng hợp enzyme, chủ yếu thông qua sự điều hòa phiên mã. Mặc dù các cơ chế này lúc đầu nhìn vào là thừa thải nhưng mỗi cơ chế sẽ vận hành trên một giai đoạn khác nhau (Hình 1) và cho phép cơ thể thích nghi với nhiều tình huống sinh lý thay đổi mạnh. Trong trạng thái hấp thu, các cơ chế điều hòa này đảm bảo rằng các chất dinh dưỡng được giữ dưới dạng glycogen, TAG và protein.
A. Sự có mặt sẵn của các cơ chất
Trong giai đoạn hấp thu, glucose là cơ chất năng lượng chính đối với hầu hết tất cả các loại tế bào. Các chất vận chuyển GLUT (GLUT transporter) tạo điều kiện cho sự hấp thu glucose và các hexokinases giữ glucose trong tế bào bởi sự phosphoryl hóa, theo động lực học tương ứng (Km [hằng số Michaelis]) của mỗi enzyme. Với các mức glucose máu cao của trạng thái hấp thu, nồng độ cơ chất tăng lên đảm bảo rằng thậm chí có một lượng glucose đủ cho các isoforms của gan, là GLUT-2 và glucokinase (hexokinase IV), mà sở hữu các giá trị Km cao hơn (ái tính thấp hơn) lần lượt so với các isoforms của cơ xương, là GLUT-4 và hexokinase I.
B. Các chất tác động dị lập thể
Các sự thay đổi dị lập thể thường liên quan đến các phản ứng xác định tốc độ (rate-determining reactions). Ví dụ, quá trình đường phân trong gan được kích thích sau một bữa ăn bởi một sự tăng lên trong fructose 2,6-bisphosphate, một chất hoạt hóa dị lập thể của phosphofructokinase-1 ([PKF-1]). Ngược lại, quá trình tân tạo đường bị giảm bởi fructose 2,6-bisphosphate, một chất ức chế dị lập thể của fructose 1,6-bisphosphatase.
C. Sự chỉnh sửa cộng hóa trị
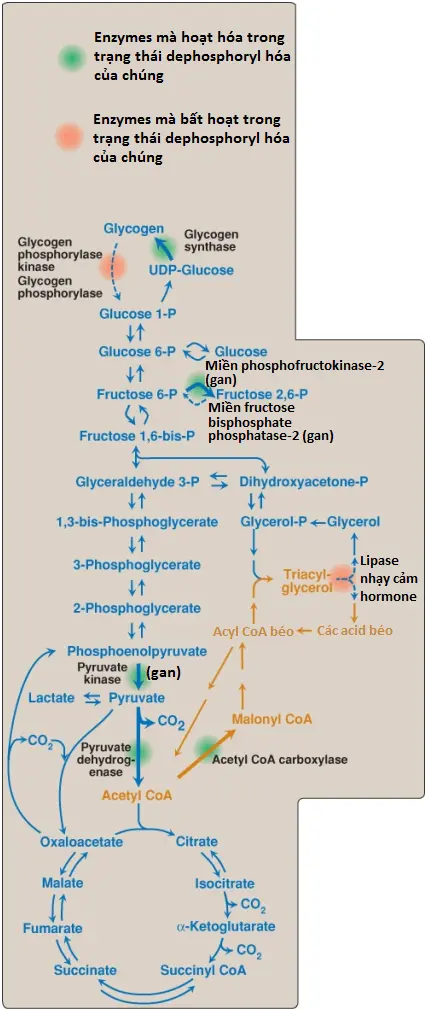
Hoạt động của nhiều enzyme được điều hòa bởi sự bổ sung (thông qua các kinases, như protein kinase A [PKA] phụ thuộc adenosine monophosphate vòng [cAMP] và protein kinase được hóa hóa bởi adenosine monophosphate [AMPK]) hay sự loại bỏ các nhóm phosphate (thông qua các phosphatase) khỏi các gốc serine, threonine hay tyrosine của protein. Trong trạng thái hấp thu, hầu hết các enzymes được điều hòa về mặt cộng hóa trị thì ở dạng dephosphoryl hóa và hoạt hóa (Hình 2). Ba ngoại lệ là glycogen phosphorylase kinase, glycogen phosphorylase và lipase nhạy cảm hormone (hormone-sensitive lipase – HSL), mà bất hoạt ở dạng dephosphoryl hóa của chúng. (Chú ý: Trong gan, dạng dephosphoryl hóa của miền phosphofructokinase-2 [PFK-2] hai chức năng là hoạt động, làm tăng sự sản xuất chất hoạt hóa dị lập thể fructose 2,6-bisphosphate. Miền còn lại, là fructose 2,6-bisphosphatase, cũng bất hoạt trong dạng dephosphoryl hóa).
D. Sự cảm ứng và sự ức chế tổng hợp enzyme
Tăng (sự cảm ứng) hay giảm (sự ức chế) tổng hợp enzyme dẫn đến các sự thay đổi trong số lượng các phân tử enzyme, chứ không phải thay đổi hoạt động của các phân tử enzyme đang tồn tại. Enzymes mà là đối tượng của sự điều hòa tổng hợp thường là các enzymes mà được cần đến dưới các tình trạng sinh lý nhất định. Ví dụ, trong trạng thái ăn no, các mức insulin tăng lên gây ra sự tăng lên trong tổng hợp các enzymes quan trọng, như acetyl coenzyme A (CoA) carboxylase (ACC) và synthase acid béo (FA), liên quan đến sự chuyển hóa đồng hóa. Trong trạng thái đói, glucagon cảm ứng sự biểu hiện của phosphoenolpyruvate carboxykinase (PEPCK) của quá trình tân tạo đường. (Chú ý: Cả hai hormone đều ảnh hưởng đến sự phiên mã của gene).
III. Gan: Trung tâm phân bố chất dinh dưỡng
Gan có vị trí đặc biệt trong việc xử lý và phân bố các chất dinh dưỡng trong chế độ ăn bởi vì sự thoát máu tĩnh mạch của ruột và tụy thì đi qua tĩnh mạch cửa của gan trước khi đi vào trong hệ thống tuần hoàn chung. Vì thế, sau một bữa ăn, gan được “tưới máu” chứa các chất dinh dưỡng được hấp thu và các mức insulin tăng lên được bài tiết bởi tụy. Trong suốt giai đoạn hấp thu, gan thu nhận carbohydrates, lipids và hầu hết các amino acids. Các chất dinh dưỡng này sau đó được chuyển hóa, tích trữ hoặc đưa đến các mô khác. Theo cách này, gan làm “dịu đi” các sự biến động lớn trong việc cung cấp các chất dinh dưỡng cho các mô ngoại vi.
A. Sự chuyển hóa carbohydrate
Gan bình thường là một cơ quan sản xuất glucose chứ không phải là một cơ quan sử dụng glucose. Tuy nhiên, sau một bữa ăn chứa carbohydrate, gan trở thành một cơ quan tiêu thụ toàn phần, giữ lại gần 60 grams trong mỗi 100 grams glucose xuất hiện trong tuần hoàn cửa. Sự tăng sử dụng này phản ánh sự tăng hấp thu glucose bởi các tế bào gan. Chất vận chuyển glucose không phụ thuộc insulin (GLUT-2) có một Km cao đối với glucose và vì thế, chỉ nhận glucose khi glucose máu cao. Các quá trình mà được điều hòa tăng (upregulated) khi glucose gan được tăng lên là như sau:
1. Sự phosphoryl hóa glucose tăng lên: Các mức glucose tăng lên bên trong tế bào gan (do các mức ngoại bào tăng lên) cho phép glucokinase phosphoryl hóa glucose thành glucose 6-phosphate (Hình 3). (Chú ý: Glucokinase có một Km cao đối với glucose, không phải là đối tượng của sự ức chế sản phẩm (product inhibition) trực tiếp, và có một đường cong phản ứng dạng sigmoid).
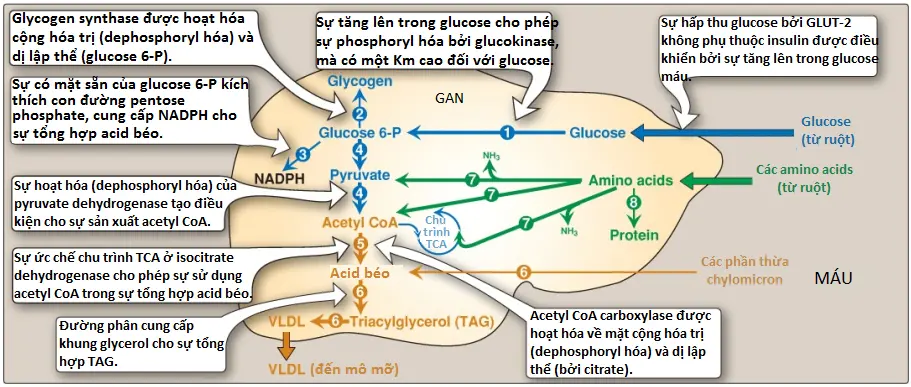
2. Tăng tổng hợp glycogen: Sự chuyển đổi của glucose 6-phosphate thành glycogen được tạo điều kiện bởi sự hoạt hóa của glycogen synthase, cả bởi sự dephosphoryl hóa và bởi sự tăng cung cấp glucose 6-phosphate, chất tác động dị lập thể dương của nó (Hình 3).
3. Tăng hoạt động của con đường pentose phosphate: Sự có mặt sẵn tăng lên của glucose 6-phosphate, kết hợp với sự sử dụng chủ động nicotinamide adenine dinucleotide phosphate (NADPH) trong quá trình tạo lipid của gan, kích thích con đường pentose phosphate. Con đường này thường chiếm khoảng 5% đến 10% glucose được chuyển hóa bởi gan (Hình 3).
4. Tăng quá trình đường phân: Trong gan, quá trình đường phân chỉ đáng kể trong suốt giai đoạn hấp thu sau một bữa ăn giàu carbohydrate. Sự chuyển đổi glucose thành pyruvate được kích thích bởi sự tăng lên của tỷ số insulin/glucagon mà tạo ra các lượng enzymes điều hòa tăng lên của quá trình đường phân: glucokinase, PFK-1, và pyruvate kinase (PK). Ngoài ra, PFK-1 được hoạt hóa dị lập thể bởi fructose 2,6-bisphosphate được tạo ra bởi miền kinase hoạt hóa (dephosphoryl hóa) của PFK-2 hai chức năng. PK được dephosphoryl hóa và hoạt hóa. Pyruvate dehydrogenase (PDH), mà chuyển pyruvate thành acetyl CoA, được hoạt hóa (dephosphoryl hóa) bởi vì pyruvate ức chế PDH kinase (Hình 3). Acetyl CoA hoặc được sử dụng như là một cơ chất cho sự tổng hợp FA hoặc bị oxy hóa để sinh năng lượng trong chu trình tricarboxylic acid (TCA) (Hình 4 cho vai trò trung tâm của glucose 6-phosphate).
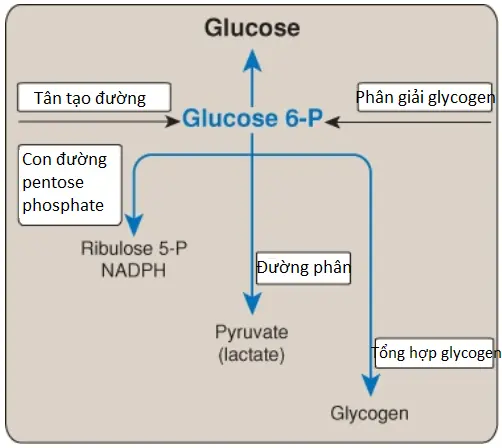
5. Giảm sự sản xuất glucose: Mặc dù quá trình đường phân (glycolysis) và tổng hợp glycogen (glycogenesis) (các con đường mà làm tăng cường sự tích trữ glucose) được kích thích trong gan trong trạng thái hấp thu nhưng quá trình tân tạo đường (gluconeogenesis) và quá trình phân giải glycogen (glycogenolysis) (các con đường mà tạo glucose) bị ức chế. Pyruvate carboxylase (PC), mà xúc tác bước đầu tiên trong con đường tân tạo đường, thì bất hoạt mạnh do các mức acetyl CoA thấp, chất hoạt hóa dị lập thể của nó. (Chú ý: Acetyl CoA được sử dụng cho sự tổng hợp FA). Tỷ số insulin/glucagon cao cũng tạo điều kiện cho sự bất hoạt của các enzymes tân tạo đường khác như fructose 1,6-bisphosphatase bởi chất ức chế dị lập thể fructose 2,6-bisphosphate (xem loạt bài viết trước). Quá trình phân giải glycogen bị ức chế bởi sự dephosphoryl hóa của glycogen phosphorylase và phosphorylase kinase. (Chú ý: Sự hấp thu tăng lên và sự sản xuất của gan giảm xuống đối với glucose máu trong giai đoạn hấp thu ngăn cản tăng đường huyết).
B. Chuyển hóa chất béo
1. Sự tổng hợp FA tăng lên: Gan là vị trí chủ yếu của sự tổng hợp mới FA (fatty acids – các acids béo) (Hình 3). Sự tổng hợp FA, một quá trình trong bào tương, được tạo điều kiện thuận lợi trong giai đoạn hấp thu bởi sự có mặt sẵn của các cơ chất acetyl CoA (từ sự chuyển hóa glucose và amino acid) và NADPH (từ sự chuyển hóa glucose trong con đường pentose phosphate) và bởi sự hoạt hóa của ACC, cả bởi sự dephosphoryl hóa và bởi sự có mặt của chất hoạt hóa dị lập thể của nó, là citrate. (Chú ý: Sự bất hoạt của AMPK tạo điều kiện thuận lợi cho sự dephosphoryl hóa). ACC xúc tác cho sự hình thành của malonyl CoA từ acetyl CoA, phản ứng giới hạn tốc độ đối với sự tổng hợp FA. (Chú ý: Malonyl CoA cũng ức chế carnitine palmitoyltransferase-I [CPT-I] của sự oxy hóa FA. Vì thế, citrate hoạt hóa sự tổng hợp FA một cách trực tiếp và ức chế sự thoái hóa FA một cách gián tiếp).
a. Nguồn acetyl CoA trong bào tương: Pyruvate từ quá trình đường phân hiếu khí (aerobic glycolysis) đi vào trong ty thể và được decarboxyl hóa bởi PDH. Sản phẩm acetyl CoA được kết hợp với oxaloacetate (OAA) để hình thành nên citrate thông qua citrate synthase của chu trình TCA. Khi chu trình TCA rất hoạt động, các mức ATP tăng lên. ATP ức chế isocitrate dehydrogenase, dẫn đến sự tích tụ của citrate. Citrate rời ty thể và đi vào trong bào tương. Citrate được phân tách bởi ATP citrate lyase (cảm ứng bởi insulin), tạo thành cơ chất acetyl CoA của ACC cùng với OAA.
b. Nguồn NADPH bổ sung: OAA được khử thành malate, mà bị decarboxyl hóa oxy hóa thành pyruvate bởi malic enzyme khi NADPH được hình thành (xem loạt bài viết trước).
2. Tăng sự tổng hợp triacylglycerol: Sự tổng hợp TAG được tạo điều kiện bởi vì các acyl CoA béo (fatty acyl CoAs) có sẵn cả từ sự tổng hợp mới và từ sự thủy phân của thành phần TAG của phần thừa chylomicron (chylomicron remnants) được loại bỏ khỏi máu bởi các tế bào gan. Glycerol 3-phosphate, khung cho sự tổng hợp TAG, được cung cấp bởi quá trình đường phân. Gan đóng gói các TAG nội sinh này vào trong các phần tử lipoprotein mật độ rất thấp (very–low-density lipoprotein – VLDL) mà được bài tiết vào trong máu để sử dụng bởi các mô ngoài gan, đặc biệt là các mô mỡ và cơ (Hình 3).
C. Sự chuyển hóa amino acid
1. Sự thoái hóa amino acid tăng lên: Trong giai đoạn hấp thu, nhiều amino acids hơn xuất hiện hơn so với việc gan có thể sử dụng trong sự tổng hợp protein và các hợp chất chứa nitrogen khác. Số amino acids dư không được tích trữ mà được giải phóng vào trong máu cho các mô khác sử dụng trong sự tổng hợp protein hoặc deamine hóa, với các khung carbon tạo thành được thoái hóa bởi gan thành pyruvate, acetyl CoA hoặc các trung gian của chu trình TCA. Các chất chuyển hóa này có thể được oxy hóa để sinh năng lượng hoặc được sử dụng trong sự tổng hợp FA (Hình 3). Gan có khả năng giới hạn trong việc khởi động sự thoái hóa các amino acids phân nhánh (branched-chain amino acids – BCAAs) – leucine, isoleucine và valine. Chúng đi qua gan hầu như không thay đổi và được chuyển hóa trong cơ.
2. Tăng tổng hợp protein: Cơ thể không tích trữ protein để sinh năng lượng giống như việc nó duy trì các sự dự trữ glycogen hay TAG. Tuy nhiên, một sự tăng lên tạm thời trong sự tổng hợp proteins của gan xảy ra trong trạng thái hấp thu, tạo ra sự thay thế của bất cứ proteins nào mà bị thoái hóa trong suốt quá trình ăn trước đó (Hình 3).
IV. Mô mỡ: kho tích trữ năng lượng
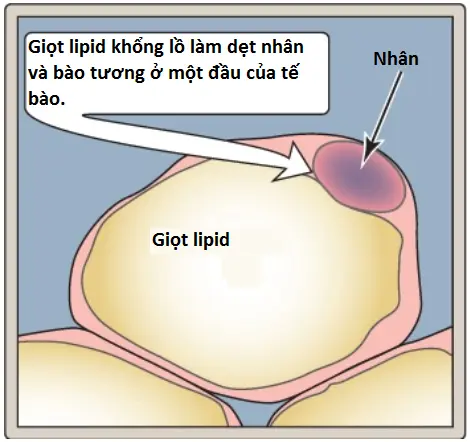
Mô mỡ chỉ đứng thứ hai sau gan về khả năng trong việc phân bố các phân tử nguyên liệu. Ở một người nam giới nặng 70 kg, mô mỡ trắng (white adipose tissue – WAT) nặng khoảng 14 kg hay khoảng một nửa so với tổng khối lượng cơ. Gần như toàn bộ thể tích của mỗi tế bào mỡ trong WAT có thể được chiếm bởi một giọt TAG khan giàu năng lượng (Hình 5).
A. Chuyển hóa carbohydrate
1. Sự vận chuyển glucose tăng lên: Các mức insulin tuần hoàn được tăng lên trong trạng thái hấp thu, tạo ra một dòng glucose đi vào trong các tế bào mỡ thông qua GLUT-4 nhạy cảm insulin (insulin-sensitive GLUT-4) được huy động đến bề mặt tế bào từ các túi nội bào (Hình 6). Glucose được phosphoryl hóa bởi hexokinase.
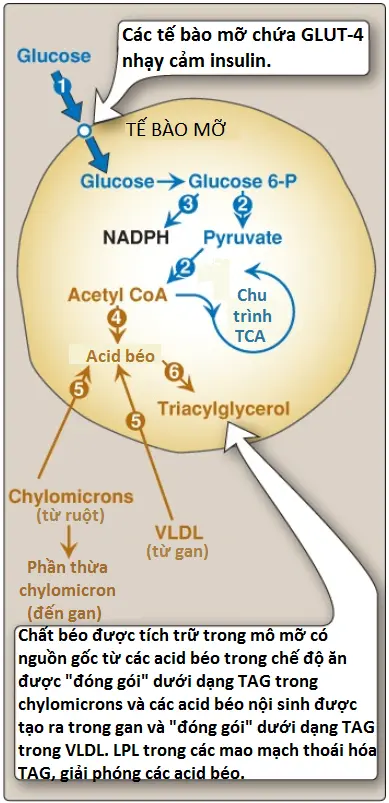
2. Tăng quá trình đường phân: Sự có mặt sẵn của glucose nội bào tăng lên gây ra một mức độ đường phân tăng lên (Hình 6). Trong mô mỡ, quá trình đường phân đóng vai trò như là một chức năng tổng hợp bằng cách cung cấp glycerol 3-phosphate cho sự tổng hợp TAG. (Chú ý: Mô mỡ thiếu glycerol kinase).
3. Tăng hoạt động của con đường pentose phosphate: Mô mỡ có thể chuyển hóa glucose bởi con đường pentose phosphate, bằng cách đó tạo ra NADPH mà cần thiết cho sự tổng hợp FA (Hình 6). Tuy nhiên, ở người, sự tổng hợp mới không phải là một nguồn FA chính trong mô mỡ, ngoại trừ khi cho một người đã nhịn đói trước đó ăn lại (Hình 6).
B. Sự chuyển hóa chất béo
Hầu hết FA được thêm vào các tích trữ TAG của các tế bào mỡ sau khi tiêu thụ một bữa ăn chứa lipid thì được cung cấp bởi sự thoái hóa của TAG ngoại sinh (trong chế độ ăn) trong các chylomicrons được đưa tới bởi ruột và TAG nội sinh trong VLDL được gửi đến bởi gan (Hình 6). FA được giải phóng từ lipoproteins bởi lipoprotein lipase (LPL), một enzyme ngoại bào được bám vào các tế bào nội mô của các thành mao mạch trong nhiều mô, đặc biệt là mô mỡ và mô cơ. Trong mô mỡ, LPL được điều hòa tăng bởi insulin. Vì thế, trong trạng thái đói, các mức glucose và insulin tăng lên tạo điều kiện cho sự tích trữ của TAG (Hình 6), tất cả carbons đều được cung cấp bởi glucose. (Chú ý: Insulin tăng lên tạo điều kiện cho dạng dephosphoryl hóa [bất hoạt] của HSL, bằng cách đó, ức chế sự phân giải lipid của TAG tích trữ trong trạng thái ăn no).
V. Cơ xương nghỉ ngơi
Cơ xương chiếm khoảng 40% khối lượng cơ thể ở những người có cân nặng khỏe mạnh và nó có thể sử dụng glucose, amino acids, FA và các thể ketone như là nguồn nguyên liệu. Trong trạng thái ăn no, cơ nhận glucose thông qua GLUT-4 (để sinh năng lượng và tổng hợp glycogen) và các amino acids (để sinh năng lượng và tổng hợp protein). Ngược lại với gan, không có sự điều hòa cộng hóa trị của PFK-2 trong cơ xương. Tuy nhiên, trong các isozyme tim, miền kinase được hoạt hóa bởi sự phosphoryl hóa qua trung gian epinephrine.
Cơ xương có khả năng đặc biệt trong việc đáp ứng với các sự thay đổi lớn trong nhu cầu đối với ATP mà kèm theo sự co cơ. Lúc nghỉ, cơ chiếm khoảng 25% sự tiêu thụ oxygen (O2) của cơ thể, ngược lại, trong suốt quá trình gắng sức mạnh, nó chiếm đến 90%. Việc này nhấn mạnh một điều là cơ xương, mặc cho khả năng của nó trong các giai đoạn đường phân yếm khí tạm thời, là một mô oxy hóa.
A. Chuyển hóa carbohydrate
1. Tăng sự vận chuyển glucose: Sự tăng lên tạm thời trong glucose và insulin huyết tương sau một bữa ăn giàu carbohydrate dẫn đến một sự tăng lên trong sự vận chuyển glucose vào trong các tế bào cơ (myocytes) bởi GLUT-4 (Hình 7), bằng cách đó, làm giảm glucose máu. Glucose được phosphoryl hóa thành glucose 6-phosphate bởi hexokinase và được chuyển hóa để đáp ứng các nhu cầu năng lượng của các tế bào cơ.
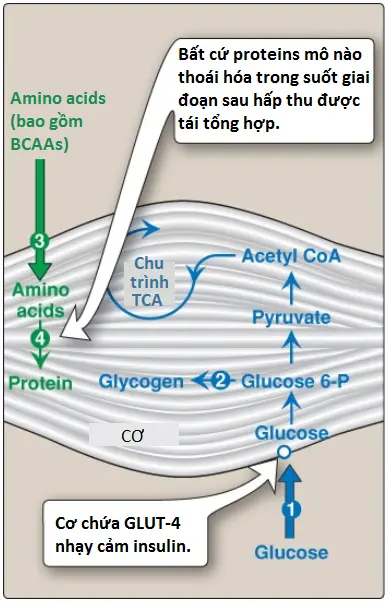
2. Tăng quá trình tổng hợp glycogen: Tăng tỷ số insulin/glucagon và sự có mặt sẵn của glucose 6-phosphate tạo điều kiện cho sự tổng hợp glycogen, đặc biệt là nếu như các sự tích trữ glycogen bị cạn kiệt do gắng sức (Hình 7).
B. Chuyển hóa chất béo
FA được giải phóng từ chylomicrons và VLDL bởi hoạt động của LPL. Tuy nhiên, FA có tầm quan trọng thứ cấp như là nguyên liệu cho cơ đang nghỉ trong suốt trạng thái ăn no, trong đó glucose là nguồn năng lượng chủ yếu. Kết quả, cơ xương bài tiết một mức LPL nền trong trạng thái hấp thu. (Chú ý: Cơ tim sẽ luôn luôn bài tiết LPL ở một mức nền cao hơn so với cơ xương. Cơ tim có thể thu được 50% đến 60% năng lượng của nó từ FA trong giai đoạn hấp thu. Trong trạng thái đói, mức này có thể tăng đến 90%).
C. Sự chuyển hóa các amino acid
1. Tăng sự tổng hợp protein: Một sự tăng lên trong sự hấp thu amino acid và sự tổng hợp protein xảy ra trong giai đoạn hấp thu sau khi tiêu hóa một bữa ăn chứa protein (Hình 7). Sự tổng hợp này thay thế protein thoái hóa từ bữa ăn trước đó.
2. Tăng sự hấp thu amino acid phân nhánh: Cơ là vị trí chủ yếu cho sự thoái hóa của BCAA bởi vì nó chứa transaminase cần thiết. BCAAs trong chế độ ăn thoát khỏi sự chuyển hóa bởi gan và được hấp thu bởi cơ, nơi mà chúng được sử dụng để tổng hợp protein (Hình 7) và như là các nguồn năng lượng.
Cảm ơn các bạn đã theo dõi bài viết. Hẹn gặp lại các bạn trong các bài viết tiếp theo nhé !!!