Cơ chế của quá trình đông máu
Phản hồi dương của sự hình thành cục máu đông
Một khi một cục máu đông bắt đầu phát triển, nó bình thường mở rộng trong vòng nhiều phút vào trong máu xung quanh – nghĩa là, cục máu đông khởi động một phản hồi dương để tăng cường quá trình đông máu. Một trong số các nguyên nhân quan trọng nhất của sự tăng cường đông máu này chính là hoạt động phân giải protein của thrombin cho phép nó tác động lên nhiều trong số các yếu tố của quá trình đông máu khác ngoài fibrinogen. Ví dụ, thrombin có một tác động phân giải protein trực tiếp lên prothrombin, có khuynh hướng chuyển nó thành nhiều thrombin hơn nữa và nó đóng vai trò lên một số trong số các yếu tố đông máu chịu trách nhiệm cho sự hình thành của yếu tố hoạt hóa prothrombin. (Các tác động này, được nói đến trong phần tiếp theo, bao gồm sự tăng cường các hoạt động của các yếu tố VIII, IX, X, XI và XII và sự kết tập tiểu cầu). Một khi lượng tới ngưỡng của thrombin được hình thành, một phản hồi dương phát triển mà gây ra nhiều quá trình đông máu hơn nữa và ngày càng nhiều thrombin được hình thành; vì thế, cục máu đông tiếp tục được phát triển cho đến khi sự mất máu ngừng lại.
Sự khởi động của quá trình đông máu: Sự hình thành của yếu tố hoạt hóa prothrombin
Bây giờ chúng ta sẽ bàn luận đến quá trình đông máu, các cơ chế phức tạp hơn mà khởi động quá trình đông máu ban đầu sẽ được mô tả. Các cơ chế này được thiết lập bởi các yếu tố sau đây: (1) chấn thương đối với thành mạch máu và các mô lân cận; (2) chấn thương đối với máu; hay (3) sự tiếp xúc của máu với các tế bào biểu mô bị tổn thương hoặc với collagen và các thành phần mô khác bên ngoài của mạch máu. Trong mỗi trường hợp, điều này dẫn đến sự hình thành của yếu tố hoạt hóa prothrombin (prothrombin activator), mà sau đó gây ra sự chuyển đổi thành thrombin và tất cả các bước bước của quá trình đông máu tiếp theo.
Yếu tố hoạt hóa prothrombin nhìn chung được xem là được hình thành theo hai cách, mặc dù, trong thực tế, hai cách tương tác hằng định với nhau: (1) bằng con đường ngoại sinh (extrinsic pathway) mà bắt đầu với chấn thương đối với thành mạch và các mô xung quanh; và (2) bằng con đường nội sinh (intrinsic pathway) mà bắt đầu trong máu.
Trong cả con đường ngoại sinh và nội sinh, một chuỗi các proteins huyết tương khác nhau được gọi là các yếu tố đông máu (blood-clotting factors) đóng một vai trò chính. Hầu hết các proteins này là các dạng bất hoạt của các enzymes phân giải protein. Khi được chuyển thành các dạng hoạt hóa, các hoạt động enzyme của chúng gây ra các phản ứng dây chuyền kế tiếp của quá trình đông máu.
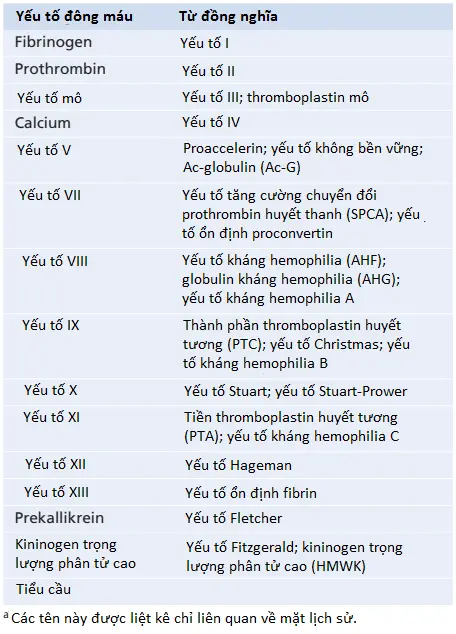
Hầu hết các yếu tố đông máu được liệt kê trong Bảng 1 được ký hiệu bởi các số La Mã. Để chỉ dạng hoạt hóa của các yếu tố, một chữ cái “a” nhỏ được thêm vào sau chữ số La Mã, như yếu tố VIIIa để chỉ trạng thái hoạt hóa của yếu tố VIII.
Con đường ngoại sinh trong khởi động quá trình đông máu
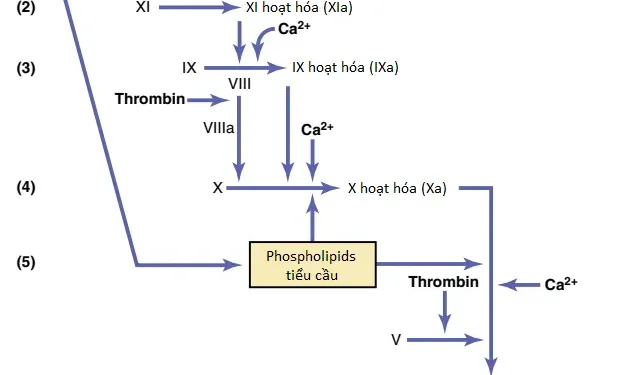
Con đường ngoại sinh trong khởi động sự hình thành của yếu tố hoạt hóa prothrombin bắt đầu với một thành mạch máu bị chấn thương hoặc các mô ngoại mạch chấn thương mà tiếp xúc với máu. Tình trạng này dẫn đến các bước tiếp theo, như được thể hiện trong Hình 1 và Hình 2.
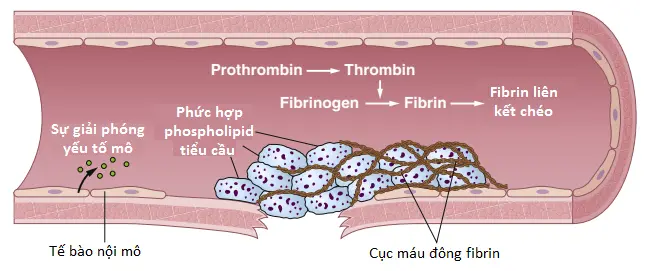
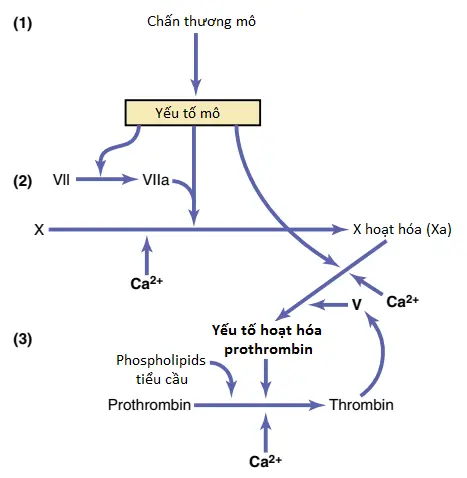
1. Sự giải phóng của yếu tố mô (tissue factor). Mô chấn thương giải phóng một phức hợp của một số yếu tố được gọi là yếu tố mô (tissue factor) hay thromboplastin mô (tissue thromboplastin). Yếu tố này bao gồm đặc biệt là phospholipids từ các màng của mô cùng với một phức hợp lipoprotein (lipoprotein complex) mà thực hiện chức năng chủ yếu như là một enzyme phân giải protein (proteolytic enzyme).
2. Sự hoạt hóa của yếu tố X – vai trò của yếu tố VII và yếu tố mô. Phức hợp lipoprotein của yếu tố mô tạo phức nhiều hơn với yếu tố đông máu VII và trong sự có mặt của ion canxi, đóng vai trò về mặt enzymes lên yếu tố X để hình thành nên yếu tố X hoạt hóa (Xa).
3.Tác động của Xa trong sự hình thành yếu tố hoạt hóa prothrombin – vai trò của yếu tố V. Yếu tố X hoạt hóa kết hợp ngay lập tức với phospholipids mô mà là một phần của các yếu tố mô hoặc với phospholipids thêm được giải phóng từ các tiểu cầu, cũng như với yếu tố V, để hình thành nên phức hợp được gọi là yếu tố hoạt hóa prothrombin (prothrombin activator). Trong vòng một vài giây, trong sự có mặt của Ca2+, prothrombin được phân tách để hình thành nên thrombin, và quá trình đông máu tiếp diễn như đã được giải thích. Đầu tiên, yếu tố V trong phức hợp yếu tố hoạt hóa prothrombin thì bất hoạt nhưng một khi quá trình đông máu bắt đầu và thrombin bắt đầu hình thành, hoạt động phân giải protein của thrombin hoạt hóa yếu tố V. Sự hoạt hóa này sau đó trở thành yếu tố tăng cường mạnh của sự hoạt hóa prothrombin. Vì thế, trong phức hợp yếu tố hoạt hóa prothrombin cuối cùng, yếu tố V hoạt hóa thực sự là protease mà gây ra sự phân tách của prothrombin để hình thành nên thrombin. Yếu tố V hoạt hóa làm tăng cường đáng kể hoạt động protease này và phospholipids tiểu cầu đóng vai trò như là một phương tiện mà tăng cường nhiều hơn quá trình. Đặc biệt chú ý tác động phản hồi dương của thrombin, tác động thông qua yếu tố V, để tăng cường toàn bộ quá trình một khi nó bắt đầu.
Con đường nội sinh trong khởi động quá trình đông máu
Cơ chế thứ hai để khởi động sự hình thành của yếu tố hoạt hóa prothrombin và vì thế để khởi động quá trình đông máu, bắt đầu với tổn thương đối với máu hoặc sự tiếp xúc của máu với collagen từ một thành mạch máu tổn thương. Sau đó, quá trình tiếp tục qua một chuỗi các phản ứng dây chuyền được thể hiện trong Hình 3.
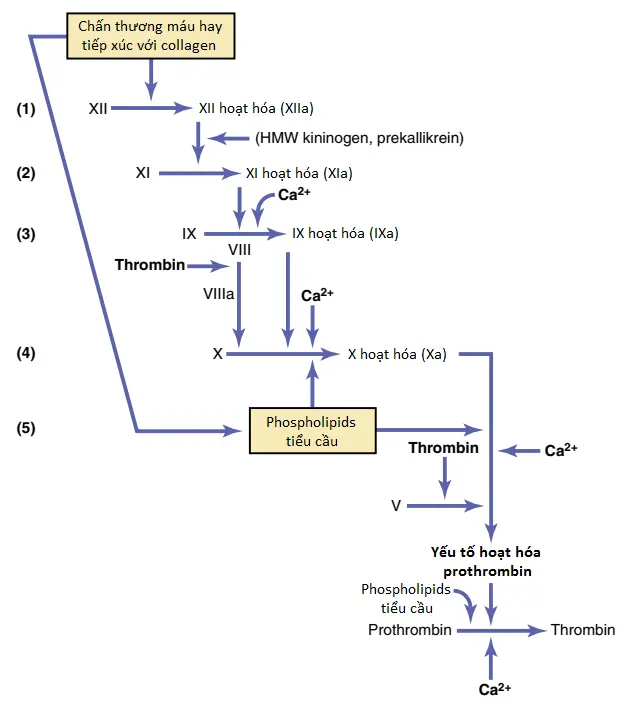
1. Các nguyên nhân của tổn thương máu (1) sự hoạt hóa của yếu tố XII và (2) sự giải phóng của phospholipids tiểu cầu. Tổn thương đối với máu hoặc sự tiếp xúc của máu với collagen của thành mạch máu làm thay đổi hai yếu tố đông máu quan trọng trong máu: yếu tố XII và các tiểu cầu. Khi yếu tố XII bị nhiễu động, như bằng cách tiếp xúc với collagen hay với một bề mặt có khả năng thấm ướt như thủy tinh, nó nhận một cấu hình phân tử mới mà chuyển nó thành một enzyme phân giải protein được gọi là yếu tố XII hoạt hóa. Đồng thời, tổn thương máu cũng làm tổn thương tiểu cầu do sự dính với collagen hoặc với bề mặt có khả năng thấm ướt (hoặc bởi tổn thương theo các cách khác); điều này làm giải phóng phospholipids tiểu cầu mà chứa lipoprotein được gọi là yếu tố tiểu cầu 3 (platelet factor 3), mà cũng đóng một vai trò trong các phản ứng đông máu kế tiếp.
2. Sự hoạt hóa của yếu tố XI. Yếu tố XII hoạt hóa cũng đóng vai trò về mặt enzyme lên yếu tố XI để hoạt hóa yếu tố này, đây là bước thứ hai trong con đường nội sinh. Phản ứng này cũng cần kininogen trọng lượng phân tử cao (high-molecular weight kininogen) và được tăng cường bởi prekallikrein.
3. Sự hoạt hóa của yếu tố IX bởi yếu tố XI hoạt hóa. Yếu tố XI hoạt hóa sau đó đóng vai trò về mặt enzyme lên yếu tố IX để hoạt hóa yếu tố này.
4. Sự hoạt hóa của yếu tố X – vai trò của yếu tố VIII. Yếu tố IX hoạt hóa, tác động trong sự phối hợp yếu tố VIII hoạt hóa, các phospholipids tiểu cầu và yếu tố III từ các tiểu cầu tổn thương, hoạt hóa yếu tố X. Rõ ràng rằng là khi yếu tố VIII hoặc tiểu cầu không được cung cấp đầy đủ, bước này sẽ bị suy giảm. Yếu tố VIII là yếu tố mà thiếu ở một người mà mắc hemophilia cổ điển, vì thế, được gọi là yếu tố kháng hemophilia (antihemophilic factor). Các tiểu cầu là yếu tố đông máu mà thiếu trong bệnh chảy máu được gọi là tình trạng suy giảm tiểu cầu (thrombocytopenia).
5. Hoạt động của yếu tố X hoạt hóa trong sự hình thành yếu tố hoạt hóa prothrombin – vai trò của yếu tố V. Bước này trong con đường nội sinh thì giống với bước cuối cùng trong con đường ngoại sinh. Nghĩa là, yếu tố X hoạt hóa kết hợp với yếu tố V và phospholipids tiểu cầu hay mô để hình thành nên phức hợp được gọi là yếu tố hoạt hóa prothrombin (prothrombin activator). Yếu tố hoạt hóa prothrombin, cuối cùng, khởi động sự phân tách của prothrombin để hình thành nên thrombin trong vòng nhiều giây, bằng cách đó, thiết lập quá trình đông máu cuối cùng, như được mô tả trước đây.
Vai trò của ion canxi trong các con đường nội sinh và ngoại sinh
Ngoại trừ hai bước đầu tiên trong con đường nội sinh, ion canxi thì cần cho sự thúc đẩy hay tăng cường của tất cả các phản ứng đông máu. Vì thế, trong sự vắng mặt của ion canxi, quá trình đông máu bởi cả hai con đường thì sẽ không xảy ra.
Trong cơ thể sống, nồng độ ion canxi hiếm khi giảm đủ thấp để ảnh hưởng đến động lực học của quá trình đông máu một cách đáng kể. Tuy nhiên, khi máu được lấy khỏi một người nào đó, nó có thể bị ngăn cản đông bằng cách làm giảm nồng độ ion canxi bên dưới ngưỡng cho sự đông máu bằng cách làm deion hóa canxi bằng cách làm cho nó phản ứng với các chất như ion citrate hoặc bằng cách lắng đọng canxi với các chất như ion oxalate.
Sự tương tác giữa các con đường ngoại sinh và nội sinh – Tóm tắt sự khởi đầu quá trình đông máu
Rõ ràng là từ các sơ đồ của các hệ thống nội sinh và ngoại sinh mà sau khi sự vỡ các mạch máu, quá trình đông máu xảy ra bởi cả hai con đường một cách đồng thời. Yếu tố mô khởi động con đường ngoại sinh, ngược lại, sự tiếp xúc của yếu tố XII và các tiểu cầu với collagen trong thành mạch máu khởi động con đường nội sinh.
Một sự khác biệt đặc biệt quan trọng giữa các con đường ngoại sinh và nội sinh chính là con đường ngoại sinh có thể “dữ dội”, một khi bắt đầu, tốc độ hoàn thành của nó thành cục máu đông cuối cùng thì chỉ được giới hạn bởi lượng yếu tố mô được giải phóng từ các mô tổn thương và bởi các lượng của các yếu tố X, VII và V trong máu. Với tổn thương mô nghiêm trọng, quá trình đông máu có thể xảy ra trong ít đến 15 giây. Con đường nội sinh thì tiếp diễn chậm hơn nhiều, thường cần 1 đến 6 phút để gây ra quá trình đông máu.
Các chất chống đông nội mạch ngăn cản quá trình đông máu trong hệ thống mạch máu bình thường
Các yếu tố bề mặt nội mô. Có lẽ các yếu tố quan trọng nhất trong ngăn cản quá trình đông máu trong hệ thống mạch máu bình thường là các yếu tố sau đây: (1) tính trơn láng của bề mặt tế bào nội mô, mà ngăn cản sự hoạt hóa tiếp xúc của hệ thống đông máu nội sinh; (2) một lớp glycocalyx trên lớp nội mô (glycocalyx là một mucopolysaccharide được hấp phụ vào các bề mặt của các tế bào nội mô), mà đẩy lui các yếu tố đông máu và các tiểu cầu, bằng cách đó, ngăn cản sự hoạt hóa quá trình đông máu; và (3) một protein liên kết với màng nội mô, thrombomodulin, mà liên kết thrombin. Không chỉ sự liên kết thrombin với thrombomodulin làm chậm quá trình đông máu bằng cách loại bỏ thrombin, mà phức hợp thrombomodulin-thrombin cũng hoạt hóa một protein huyết tương, là protein C, mà đóng vai trò như là một chất chống đông bằng cách bất hoạt các yếu tố V và VIII hoạt hóa.
Khi thành nội mô bị tổn thương, tính trơn láng và lớp glycocalyx-thrombomodulin bị mất, điều mà hoạt hóa cả yếu tố XII và các tiểu cầu, vì thế, làm thiết lập con đường nội sinh của quá trình đông máu. Nếu như yếu tố XII và các tiểu cầu tiếp xúc với collagen dưới nội mô thì sự hoạt hóa thậm chí còn mạnh mẽ hơn.
Các tế bào biểu mô nguyên vẹn cũng sản xuất các chất khác như prostacyclin và nitric oxide (NO) mà ức chế sự kết tập tiểu cầu và sự khởi động của quá trình đông máu. Prostacyclin, còn được gọi là prostaglandin I2 (PGI2), là một thành viên của họ lipid eicosanoid và là một yếu tố giãn mạch, cũng như là một chất ức chế sự kết tập tiểu cầu. Như được nói đến trong các bài viết trước, NO là một chất giãn mạch mạnh được giải phóng từ các tế bào nội mô mạch máu khỏe mạnh trên khắp cơ thể, và nó là một chất ức chế quan trọng của sự kết tập tiểu cầu. Khi các tế bào nội mô bị tổn thương, sự sản xuất prostacyclin và NO của chúng bị giảm đáng kể.
Hoạt động kháng thrombin của fibrin và antithrombin III. Trong số các chất kháng đông (anticoagulants) quan trọng nhất trong máu là các chất mà loại bỏ thrombin khỏi máu. Mạnh mẽ nhất trong số này là các chất sau: (1) các sợi fibrin mà được hình thành trong suốt quá trình đông máu; và (2) một α globulin được gọi là antithrombin III hay đồng yếu tố antithrombin-heparin.
Trong khi một cục máu đông đang hình thành, khoảng 85% đến 90% thrombin được hình thành từ prothrombin được hấp phụ vào các sợi fibrin khi chúng phát triển. Sự hấp phụ này giúp ngăn cản sự lan rộng của thrombin vào trong máu còn lại và vì thế, ngăn cản sự lan rộng quá mức của quá trình đông máu.
Thrombin mà không hấp phụ vào các sợi fibrin sẽ sớm kết hợp với antithrombin III. Điều này làm ngăn chặn thêm tác động của thrombin lên fibrinogen và sau đó cũng bất hoạt chính thrombin trong suốt 12 đến 20 phút tiếp theo.
Heparin. Heparin là một chất chống đông mạnh nhưng bởi vì nồng độ của nó trong máu bình thường thấp, nên nó có các tác động kháng đông đáng kể chỉ dưới các tình trạng sinh lý cụ thể. Tuy nhiên, heparin được sử dụng một cách rộng rãi như là một chất dược học trong thực hành y khoa ở các nồng động cao hơn nhiều để ngăn cản quá trình đông máu nội mạch.
Phân tử heparin là một polysaccharide liên hợp tích điện âm mạnh. Chính nó có ít hoặc không có thuộc tính kháng đông nhưng khi nó kết hợp với antithrombin III, tính hiệu quả của antithrombin III trong việc loại bỏ thrombin tăng lên một trăm lần đến một nghìn lần và vì thế, đóng vai trò như là một chất kháng đông. Vì thế, trong sự có mặt quá mức heparin, sự loại bỏ thrombin tự do khỏi máu tuần hoàn bởi antithrombin III thì gần như là tức thời.
Phức hợp của heparin và antithrombin III loại bỏ một số yếu tố đông máu hoạt hóa khác ngoài thrombin, tăng cường nhiều hơn nữa tính hiệu quả của sự kháng đông. Các yếu tố khác bao gồm cả các yếu tố IX đến XII hoạt hóa.
Heparin được sản xuất bởi nhiều tế bào khác nhau của cơ thể nhưng các lượng lớn nhất được hình thành bởi các dưỡng bào (mast cells) ái kiềm nằm trong mô liên kết quanh mao mạch trên khắp cơ thể. Các tế bào này liên tục bài tiết các lượng heparin nhỏ mà khuếch tán vào trong hệ thống tuần hoàn. Các tế bào bạch cầu ái kiềm (basophil cells) của máu, mà hầu như tương tự về mặt chức năng với các dưỡng bào, giải phóng các lượng heparin nhỏ vào trong huyết tương.
Các dưỡng bào thì dồi dào trong mô quanh các mao mạch của các phổi và với một mức độ nhỏ hơn, là các mao mạch của gan. Dễ dàng hiểu được tại sao các lượng lớn heparin phải được cần đến trong các khu vực này bởi vì các mao mạch của các phổi và gan nhận nhiều cục máu đông mà được hình thành trong máu tĩnh mạch chảy chậm; sự sản xuất heparin đầy đủ ngăn cản sự tăng trưởng nhiều hơn của các cục máu đông.
Plasmin gây ra sự phân giải của các cục máu đông
Các proteins huyết tương chứa một euglobulin được gọi là plasminogen (profibrinolysin) mà khi được hoạt hóa, trở thành một chất mà được gọi là plasmin (fibrinolysin). Plasmin là một enzyme phân giải protein mà tương tự trypsin, enzyme tiêu hóa phân giải protein quan trọng nhất của dịch tiết tuyến tụy. Plasmin tiêu hóa các sợi fibrin và một số protein đông máu khác, như fibrinogen, yếu tố V, yếu tố VIII, prothrombin và yếu tố XII. Vì thế, bất cứ khi nào plasmin được hình thành, nó có thể gây ra sự phân giải của một cục máu đông bằng cách phá hủy nhiều yếu tố đông máu, bằng cách đó, đôi khi thậm chí gây ra sự giảm khả năng đông của máu.
Sự hoạt hóa của plasminogen để hình thành plasmin, sau đó là sự phân giải cục máu đông. Khi một cục máu đông được hình thành, một lượng lớn plasminogen bị giữ trong cục máu đông, cùng với các proteins huyết tương khác. Chất này sẽ không trở thành plasmin hoặc gây ra sự phân giải của cục máu đông cho đến khi nó được hoạt hóa. Các mô và nội mô mạch máu tổn thương giải phóng rất chậm một yếu tố hoạt hóa mạnh được gọi là yếu tố hoạt hóa plasminogen mô (t-PA – tissue plasminogen activator); một vài ngày sau, sau khi cục máu đông làm ngừng chảy máu, t-PA cuối cùng chuyển plasminogen thành plasmin, chất mà cuối cùng loại bỏ cục máu đông không cần thiết còn lại. Trong thực tế, nhiều mạch máu nhỏ mà trong đó dòng máu bị chặn bởi các cục máu đông được mở trở lại bởi cơ chế này. Vì thế, một chức năng đặc biệt quan trọng của hệ thống plasmin là loại bỏ các cục máu đông nhỏ khỏi hàng triệu các mạch máu ngoại vi nhỏ mà cuối cùng sẽ bị tắc nếu như không có cách nào để loại bỏ chúng.
Các tình trạng mà gây ra sự chảy máu quá mức ở người
Chảy máu quá mức có thể do một sự suy giảm của bất cứ yếu tố nào trong số các yếu tố đông máu. Ba loại khuynh hướng chảy máu cụ thể được nghiên cứu nhiều nhất mà được bàn đến ở đây – chảy máu được gây ra bởi (1) sự thiếu hụt vitamin K, (2) hemophilia và (3) bệnh giảm tiểu cầu (thrombocytopenia) (sự thiếu hụt tiểu cầu).
Giảm prothrombin, yếu tố VII, yếu tố IX và yếu tố X được gây ra bởi sự thiếu hụt vitamin K
Với một số ít ngoại trừ, hầu như tất cả các yếu tố đông máu đều được hình thành bởi gan. Vì thế, các bệnh của gan như viêm gan, xơ gan và teo vàng cấp tính (acute yellow atrophy) (sự thoái hóa gan được gây ra bởi các chất độc, các nhiễm trùng hay các chất khác) đôi khi có thể làm suy yếu hệ thống đông máu nhiều đến nỗi bệnh nhân phát triển một khuynh hướng chảy máu nghiêm trọng.
Một nguyên nhân khác của giảm sự hình thành các yếu tố đông máu bởi gan là sự thiếu hụt vitamin K. Vitamin K là một yếu tố thiết yếu đối với một carboxylase của gan mà thêm nhóm carboxyl vào các gốc glutamic acid trên năm trong số các yếu tố đông máu quan trọng – prothrombin, yếu tố VII, yếu tố IX, yếu tố X và protein C. Khi thêm nhóm carboxyl vào các gốc glutamic acid trên các yếu tố đông máu chưa trưởng thành thì vitamin K bị oxy hóa và trở nên bất hoạt. Một enzyme khác, là vitamin K epoxide reductase complex 1 (VKORC1), làm giảm lượng vitamin K quay trở lại dạng hoạt hóa của nó. Trong sự vắng mặt của vitamin K hoạt hóa, sự suy yếu kế tiếp của các yếu tố đông máu này trong máu có thể dẫn đến các khuynh hướng chảy máu nghiêm trọng.
Vitamin K thì liên tục được tổng hợp trong đường tiêu hóa bởi các vi khuẩn, vì thế, sự thiếu hụt vitamin K hiếm khi xảy ra ở những người khỏe mạnh như là kết quả của sự vắng mặt vitamin K từ chế độ ăn (ngoại trừ ở các trẻ sơ sinh, trước khi chúng thiết lập hệ vi khuẩn đường ruột). Tuy nhiên, ở những người mắc các bệnh về đường tiêu hóa, sự thiếu hụt vitamin K thường xảy ra do sự hấp thu kém các chất béo từ đường tiêu hóa bởi vì vitamin K tan trong chất béo và thường được hấp thu vào trong máu cùng với các chất béo.
Một trong số các nguyên nhân phổ biến nhất của sự thiếu hụt vitamin K là suy yếu gan trong việc bài tiết mật vào trong đường tiêu hóa, điều mà xảy ra do sự tắc các ống mật hoặc bệnh gan. Thiếu mật sẽ ngăn cản sự tiêu hóa và hấp thu chất béo một cách đầy đủ và vì thế, cũng làm giảm sự hấp thu vitamin K nữa. Vì thế, bệnh gan thường gây ra sự suy giảm sản xuất prothrombin và một số các yếu tố đông máu khác do sự hấp thu vitamin K kém và do các tế bào gan mắc bệnh. Kết quả, vitamin K được tiêm vào trong các bệnh nhân phẫu thuật mắc bệnh gan hoặc có tắc nghẽn ống mật trước khi thực hiện phẫu thuật. Thông thường, nếu như vitamin K được sử dụng cho một bệnh nhân 4 đến 8 giờ trước khi phẫu thuật và các tế bào nhu mô gan thì ít nhất có chức năng một nửa so với bình thường, thì các yếu tố đông máu đầy đủ sẽ được sản xuất để ngăn cản sự chảy máu quá mức trong suốt quá trình phẫu thuật.
Cảm ơn các bạn đã theo dõi bài viết. Hẹn gặp lại các bạn trong các bài viết tiếp theo nhé !!!