Tăng huyết áp và bệnh thận
Các tổn thương thận mà làm giảm khả năng các thận trong việc bài tiết natri và nước làm tăng cường tăng huyết áp. Các tổn thương thận mà làm giảm khả năng của các thận trong việc bài tiết natri và nước hầu như là gây ra tăng huyết áp không thể thay đổi. Vì thế, các tổn thương mà làm giảm GFR hay tăng sự tái hấp thu ống thận thường dẫn đến tăng huyết áp với các mức độ khác nhau. Một số loại đặc hiệu của các bất thường thận mà có thể gây ra tăng huyết áp là như sau:
1. Tăng sức cản mạch máu thận, mà làm giảm lưu lượng máu thận và GFR. Một ví dụ là tăng huyết áp được gây ra bởi hẹp động mạch thận.
2. Giảm hệ số lọc mao mạch cầu thận, mà làm giảm GFR. Một ví dụ là viêm cầu thận mạn tính, mà gây ra viêm và dày các màng mao mạch cầu thận, bằng cách đó, làm giảm hệ số lọc mao mạch cầu thận.
3. Sự tái hấp thu natri ống thận quá mức. Một ví dụ là tăng huyết áp được gây ra bởi sự bài tiết aldosterone quá mức, mà làm tăng sự tái hấp thu natri chủ yếu trong các vi ống thu thập vỏ.
Một khi tăng huyết áp phát triển, sự bài tiết natri và nước của thận trở về bình thường bởi vì áp suất động mạch cao gây ra lợi niệu natri áp suất và lợi niệu áp suất, vì thế, lượng nước và natri ăn vào và thải ra được cân bằng lại một lần nữa. Thậm chí khi có các sự tăng lên nhiều trong sức cản mạch máu thận hay các sự giảm trong hệ số lọc mao mạch cầu thận, GFR có thể vẫn trở về các mức gần như bình thường sau khi áp suất động mạch tăng lên. Tương tự, khi sự tái hấp thu của ống thận tăng lên, như xảy ra với sự bài tiết aldosterone quá mức, thì mức bài tiết nước tiểu bị giảm ban đầu nhưng sau đó trở về bình thường khi áp suất động mạch tăng lên. Vì thế, sau khi tăng huyết áp phát triển, có thể không có dấu hiệu rõ ràng của suy giảm sự bài tiết natri và nước ngoài tăng huyết áp. Như được giải thích trong loạt bài viết trước, sự bài tiết bình thường của natri và nước ở một áp suất động mạch tăng lên có nghĩa là lợi niệu natri áp suất và lợi niệu áp suất đã được “đặt lại” (reset) đến một áp suất động mạch cao hơn.
Tăng huyết áp được gây ra bởi tổn thương thận mảng và tăng sự bài tiết renin của thận. Nếu như một phần của thận bị thiếu máu và phần còn lại không bị thiếu máu, như khi một động mạch thận bị co nghiêm trọng, mô thận thiếu máu bài tiết các lượng lớn renin. Sự bài tiết này dẫn đến tăng hình thành Ang II, mà có thể gây ra tăng huyết áp, như được nói đến trong loạt bài viết trước, là như sau: (1) mô thận thiếu máu bài tiết ít hơn các lượng nước và muối bình thường; (2) renin được bài tiết bởi thận thiếu máu, cũng như là sự hình thành Ang II tăng lên tiếp theo, ảnh hưởng đến mô thận không thiếu máu, làm cho nó cũng giữ lại muối và nước; và (3) lượng muối và nước dư thừa gây ra tăng huyết áp theo cách thông thường.
Một loại tăng huyết áp tương tự có thể xảy ra khi các vùng của một hoặc cả hai thận trở nên thiếu máu do xơ vữa động mạch hoặc tổn thương mạch máu trong các vùng đặc hiệu của các thận. Khi điều này xảy ra, các nephrons thiếu máu bài tiết ít muối và nước hơn nhưng bài tiết các lượng renin lớn hơn, mà gây ra tăng sự hình thành Ang II. Các mức cao của Ang II sau đó làm suy giảm khả năng của các nephrons bình thường xung quanh trong việc bài tiết natri và nước. Kết quả, tăng huyết áp phát triển, điều mà hồi phục sự bài tiết bình thường của natri và nước bởi thận, vì thế, thăng bằng giữa lượng muối và nước ăn vào và thải ra được duy trì, nhưng có tăng huyết áp.
Các bệnh thận mà gây ra sự mất khối nephrons dẫn đến bệnh thận mạn tính nhưng có thể không gây ra tăng huyết áp
Sự mất các lượng lớn của khối nephrons, như xảy ra trong sự mất của một thận và một phần của thận còn lại, gần như luôn luôn dẫn đến CKD nếu như sự mất mô thận là đủ lớn. Nếu như các nephrons còn lại bình thường và muối ăn vào không quá mức thì tình trạng này có thể không gây ra tăng huyết áp đáng kể trên lâm sàng. Điều này là bởi vì ngay cả một sự tăng lên nhỏ trong huyết áp cũng sẽ làm tăng GFR và làm giảm sự tái hấp thu natri của ống thận ở các nephrons đang còn sống đủ để thúc đẩy đủ sự bài tiết muối và nước trong nước tiểu, ngay cả với một ít nephrons còn nguyên vẹn. Tuy nhiên, một bệnh nhân mắc loại bất thường này có thể trở nên tăng huyết áp nghiêm trọng nếu như thêm các stress được bổ sung, như ăn một lượng lớn muối. Trong trường hợp này, các thận đơn giản là không thể loại bỏ đủ các lượng muối ở một huyết áp bình thường với một số lượng nhỏ nephrons thực hiện chức năng còn lại. Tăng huyết áp hồi phục sự bài tiết muối và nước để phù hợp với lượng muối và nước ăn vào dưới các tình trạng ổn định.
Điều trị tăng huyết áp hiệu quả cần tăng cường khả năng của thận trong việc bài tiết muối và nước bằng cách tăng GFR hay bằng cách giảm sự tái hấp thu của ống thận, sao cho cân bằng giữa lượng ăn vào và bài tiết của thận đối với muối và nước có thể được duy trì ở một huyết áp thấp. Tác động này có thể đạt được bởi các thuốc mà chặn các tác động của các tín hiệu thần kinh và hormone mà làm cho các thận giữa lại muối và nước (như với các thuốc chặn β-adrenergic, các thuốc đối kháng thụ cảm thể Ang II hay các thuốc ức chế ACE), cùng với các thuốc mà làm giãn mạch các thận và làm tăng GFR (như các thuốc chặn kênh canxi) hoặc cùng với các thuốc lợi niệu mà ức chế trực tiếp sự tái hấp thu của ống thận đối với muối và nước.
Các rối loạn ống thận đặc hiệu
Trong loạt bài viết trước, chúng ta đã nói đến một số cơ chế chịu trách nhiệm cho việc vận chuyển các chất khác nhau qua các màng biểu mô ống thận. Trong một loạt bài viết khác, chúng ta cũng chỉ ra rằng mỗi enzyme của tế bào và mỗi protein mang được hình thành trong đáp ứng với một gene tương ứng trong nhân. Nếu như bất cứ gene được cần đến nào bị vắng mặt hay bất thường thì các ống thận có thể bị suy giảm một trong số các proteins mang thích hợp hoặc một trong số các enzymes cần cho sự vận chuyển chất tan bởi các tế bào biểu mô ống thận. Trong các trường hợp khác, quá nhiều enzyme hoặc chất mang protein được sản xuất. Vì thế, nhiều rối loạn ống thận di truyền xảy ra do sự vận chuyển bất thường các chất riêng biệt hoặc các nhóm chất qua màng ống thận. Ngoài ra, tổn thương đối với màng ống thận bởi các chất độc hay thiếu máu có thể gây ra các rối loạn ống thận quan trọng.
Glucose niệu (glycosuria) do thận – Suy yếu khả năng thận trong việc tái hấp thu glucose. Trong glucose niệu, nồng độ glucose máu có thể bình thường nhưng cơ chế vận chuyển đối với sự tái hấp thu glucose của ống thận thì giới hạn đáng kể hay vắng mặt. Kết quả, mặc dù một mức glucose máu bình thường nhưng các lượng lớn glucose đi vào trong nước tiểu mỗi ngày. Bởi vì tiểu đường cũng liên quan với sự có mặt của glucose trong nước tiểu nên glucose niệu, là một tình trạng tương đối nhẹ, phải được loại trừ trước khi đưa ra chẩn đoán đái tháo đường.
Amino acid niệu (aminoaciduria) – Suy yếu khả năng của các thận trong việc tái hấp thu các amino acids. Một số amino acids có chung các hệ thống vận chuyển, ngược lại, các amino acids khác có các hệ thống riêng biệt của chúng. Hiếm khi, một tình trạng được gọi là amino acid niệu toàn thể (generalized aminoaciduria) do sự thiếu hụt tái hấp thu của tất cả các amino acids. Thường gặp hơn, các sự thiếu hụt của các hệ thống chất mang chuyên biệt có thể gây ra các tình trạng sau đây: (1) cystine niệu vô căn (essential cystinuria), trong đó các lượng lớn cystine không được tái hấp thu và thường kết tinh trong nước tiểu để hình thành nên các sỏi thận; (2) glycine niệu đơn giản (simple glycinuria), trong đó glycine không được tái hấp thu; hay (3) beta-aminoisobutyric acid niệu (beta-aminoisobutyricaciduria), mà xảy ra ở khoảng 5% dân số nhưng dường như không có tầm quan trọng lâm sàng đáng kể.
Hạ phosphate máu (hypophosphatemia) do thận – suy giảm khả năng của các thận trong việc tái hấp thu phosphate. Trong hạ phosphate máu do thận, các ống thận không tái hấp thu đủ nhiều ions phosphate khi nồng độ phosphate của các dịch cơ thể giảm xuống rất thấp. Tình trạng này thường không gây ra các bất thường ngay lập tức bởi vì nồng độ phosphate của dịch ngoại bào có thể thay đổi rộng mà không gây ra rối loạn chức năng tế bào lớn. Tuy nhiên, qua một khoảng thời gian dài, một mức phosphate thấp gây ra sự vôi hóa giảm của các xương, gây ra sự phát triển của còi xương (rickets). Loại còi xương này thì kháng với liệu pháp vitamin D, ngược lại với đáp ứng nhanh của loại còi xương thông thường, như được nói đến trong một loạt bài viết sau.
Nhiễm toan ống thận (renal tubular acidosis) – Giảm sự bài tiết ion hydrogen của ống thận. Trong nhiễm toan ống thận, các ống thận không thể bài tiết các lượng đủ ions hydrogen. Kết quả, các lượng lớn natri bicarbonate bị mất một cách liên tục trong nước tiểu. Sự mất này gây ra một tình trạng nhiễm toan chuyển hóa liên tục, như được nói đến trong loạt bài viết trước. Loại bất thường thận này có thể được gây ra bởi các rối loạn hoặc có thể xảy ra như là kết quả của tổn thương lan rộng đối với các ống thận.
Đái tháo nhạt do thận (nephrogenic diabetes insipidus) – Suy giảm khả năng của các thận trong đáp ứng với hormone chống bài niệu. Đôi khi, các ống thận không đáp ứng với hormone chống bài niệu, làm cho các lượng lớn nước tiểu loãng được bài tiết. Miễn là người đó được cung cấp nhiều nước, tình trạng này hiếm khi gây ra khó khăn nghiêm trọng. Tuy nhiên, khi các lượng nước đủ không có sẵn thì người đó nhanh chóng bị mất nước.
Hội chứng Fanconi (Fanconi syndrome) – Suy giảm tái hấp thu toàn thể của các ống thận. Hội chứng Fanconi thường liên quan với sự tăng bài tiết trong nước tiểu của hầu hết tất cả các amino acids, glucose và phosphate. Trong các trường hợp nghiêm trọng, các biểu hiện khác cũng được quan sát thấy, như (1) suy yếu khả năng tái hấp thu natri bicarbonate, mà gây ra nhiễm toan chuyển hóa; (2) tăng sự bài tiết kali và đôi khi là canxi và (3) đái tháo nhạt do thận.
Có nhiều nguyên nhân của hội chứng Fanconi, mà do một sự mất khả năng toàn thể của các tế bào ống thận trong việc vận chuyển các chất khác nhau. Một số trong số này bao gồm các nguyên nhân sau: (1) các khiếm khuyết di truyền trong các cơ chế vận chuyển tế bào; (2) các chất độc hoặc các thuốc mà làm tổn thương các tế bào biểu mô ống thận; và (3) tổn thương đối với các tế bào ống thận là kết quả của thiếu máu. Các tế bào ống lượn gần thì đặc biệt bị ảnh hưởng trong hội chứng Fanconi mà được gây ra bởi tổn thương ống thận bởi vì các tế bào này tái hấp thu và bài tiết nhiều trong số các thuốc và các chất độc mà gây ra tổn thương.
Hội chứng Bartter (Bartter syndrome) – Giảm sự tái hấp thu natri, chloride và kali trong quai Henle. Hội chứng Bartter (Bartter syndrome) là một nhóm các rối loạn thận hiếm gặp được gây ra bởi các đột biến là làm giảm chức năng của chất đồng vận chuyển 1-natri, 2-chloride, 1-kali hoặc bởi các khiếm khuyết trong các kênh kali trong màng lòng hoặc các kênh chloride trong màng đáy-bên của nhánh lên dày của quai Henle. Ít nhất năm đột biến, thường được di truyền theo kiểu lặn trên nhiễm sắc thể thường, được phát hiện là gây ra hội chứng Bartter. Các rối loạn này gây ra sự bài tiết tăng lên của nước, natri, chloride, kali và canxi bởi các thận. Sự mất muối và nước dẫn đến sự suy giảm thể tích nhẹ, gây ra sự hoạt hóa của hệ thống renin-angiotensin-aldosterone (renin-angiotensin-aldosterone system – RAAS). Aldosterone tăng và lưu lượng ống lượn xa cao, do giảm sự tái hấp thu của quai Henle kích thích sự bài tiết kali và hydrogen trong các vi ống thu thập, dẫn đến hạ kali máu và nhiễm kiềm chuyển hóa.
Hội chứng Gitelman (Gitelman syndrome) – Giảm sự tái hấp thu natri chloride trong các ống lượn xa. Hội chứng Gitelman (Gitelman syndrome) là một rối loạn lặn trên nhiễm sắc thể thường của chất đồng vận chuyển natri-chloride nhạy cảm thiazide trong các ống lượn xa. Những bệnh nhân mắc hội chứng Gitelman có một số đặc điểm giống với các bệnh nhân mắc hội chứng Bartter – mất muối và nước, giảm thể tích nước nhẹ và sự hoạt hóa của hệ thống renin-angiotensin-aldosterone – mặc dù các bất thường này thường ít nghiêm trọng hơn ở những người mắc hội chứng Gitelman.
Bởi vì các khiếm khuyết ống thận trong hội chứng Bartter hay Gitelman không thể được điều chỉnh hiện tại nên điều trị thường tập trung vào việc thay thế các sự mất natri chloride và kali. Một số nghiên cứu cho thấy rằng sự chặn tổng hợp prostaglandin bằng các thuốc kháng viêm không steroid (nonsteroidal antiinflammatory drugs – NSAIDs) và sử dụng các thuốc đối kháng aldosterone, như spironolactone, có thể hữu ích trong việc điều trị hạ kali máu.
Hội chứng Liddle (Liddle syndrome) – Sự tái hấp thu natri tăng lên. Hội chứng Liddle (Liddle syndrome) là một rối loạn trội trên nhiễm sắc thể thường hiếm gặp mà do nhiều đột biến khác nhau trong kênh natri biểu mô (epithelial sodium channel – ENaC) nhạy cảm với amiloride trong các ống lượn xa và vi ống thu thập. Các đột biến này gây ra hoạt động quá mức của ENaC, gây ra sự tái hấp thu tăng lên của natri và nước, tăng huyết áp và nhiễm kiềm chuyển hóa tương tự với các thay đổi mà xảy ra với sự quá bài tiết của aldosterone (cường aldosterone nguyên phát [primary aldosteronism]).
Tuy nhiên, những bệnh nhân mắc hội chứng Liddle, có sự giữ lại natri và giảm sự bài tiết renin và các mức Ang II, điều mà cuối cùng làm giảm sự bài tiết aldosterone của tuyến thượng thận. May mắn thay, hội chứng Liddle có thể được điều trị với thuốc lợi niệu amiloride, thuốc mà chặn hoạt động của ENaC quá mức.
Điều trị suy thận bằng cấy ghép hay thẩm phân máu (lọc máu) với một thận nhân tạo
Mất chức năng thận nghiêm trọng, một cách cấp tính hoặc mạn tính, thì đe dọa mạng sống và cần loại bỏ các sản phẩm thải độc hại và hồi phục thể tích và thành phần dịch cơ thể về mức bình thường. Điều này có thể được thận hiện bởi cấy ghép thận hoặc bởi thẩm phân máu bằng một thận nhân tạo. Hơn 700,000 bệnh nhân ở Hoa Kỳ hiện nay đang nhận một số dạng của phương pháp điều trị ESRD.
Sự cấy ghép thành công của một thận hiến đơn vào một bệnh nhân mắc ESRD có thể phục hồi chức năng thận đến một mức đủ để duy trì cân bằng nội môi về bản chất là bình thường của các dịch cơ thể và các chất điện giải. Gần 19,000 ca cấy ghép thận được thực hiện mỗi năm ở Hoa Kỳ nhưng hơn 100,000 bệnh nhân vẫn đang đợi cấy ghép thận. Những bệnh nhân mà nhận được thận cấy ghép thường sống lâu hơn và có ít vấn đề về sức khỏe hơn so với những người mà duy trì sự sống bằng thẩm phân máu. Sự duy trì điều trị thuốc ức chế miễn dịch là cần thiết đối với hầu hết tất cả các bệnh nhân để giúp ngăn cản sự thải ghép cấp tính và sự mất thận được cấy ghép. Các tác dụng phụ của các thuốc mà ức chế miễn dịch bao gồm tăng nguy cơ nhiễm trùng và một số ung thư, mặc dù mức điều trị ức chế miễn dịch thường có thể giảm theo thời gian để làm giảm các nguy cơ này một cách đáng kể.
Hơn 475,000 người ở Hoa Kỳ mà có suy thận không thể đảo ngược hay loại bỏ thận hoàn toàn đang được duy trì sự sống lâu dài bởi thẩm phân máu (lọc máu) bởi các thận nhân tạo. Thẩm phân máu cũng được sử dụng trong một số loại AKI để khắc phục cho bệnh nhân cho đến khi các thận phục hồi chức năng của chúng. Nếu như sự mất chức năng thận không thể đảo ngược thì cần thực hiện thẩm phân lâu dài để duy trì sự sống. Bởi vì thẩm phân không thể duy trì thành phần dịch cơ thể bình thường một cách hoàn toàn và không thể thay thế tất cả các chức năng được thực hiện bởi các thận nên sức khỏe của các bệnh nhân được duy trì bằng việc sử dụng các thận nhân tạo thường vẫn bị suy giảm đáng kể.
Các nguyên lý cơ bản của thẩm phân máu
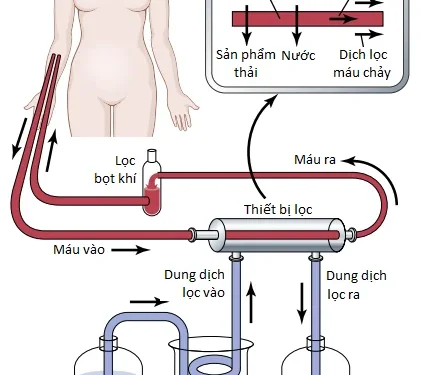
Nguyên lý cơ bản của thận nhân tạo là đưa máu qua các kênh máu nhỏ được liên kết bởi một màng mỏng. Ở phía bên kia của màng là một dịch thẩm phân (dialyzing fluid) mà các chất không mong muốn trong máu sẽ đi vào đó bởi sự khuếch tán.
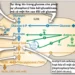
Hình 1 cho thấy các thành phần của một loại thận nhân tạo mà trong đó máu chảy một cách liên tục giữa hai màng mỏng cellophane, ở bên ngoài màng là một dịch thẩm phân. Giấy bóng kính thì có lỗ đủ để cho phép các thành phần của huyết tương, ngoại trừ các proteins huyết tương, khuếch tán theo cả hai hướng – từ huyết tương vào trong dịch thẩm phân hay từ dịch thẩm phân quay ngược vào trong huyết tương. Nếu như nồng độ của một chất cao hơn trong huyết tương so với trong dịch thẩm phân thì sẽ có một sự vận chuyển toàn phần của chất từ huyết tương vào trong dịch thẩm phân.
Mức di chuyển của chất tan qua màng thẩm phân phụ thuộc vào các yếu tố sau đây: (1) gradient nồng độ của chất tan giữa hai dung dịch; (2) tính thấm của màng đối với chất tan; (3) diện tích bề mặt của màng; và (4) khoảng thời gian mà máu và dịch tiếp xúc với màng.
Vì thế, mức tối đa của sự vận chuyển chất tan xảy ra ban đầu khi gradient nồng độ là lớn nhất (khi thẩm phân bắt đầu) và chậm lại khi gradient nồng độ giảm bớt. Trong một hệ thống đang chảy, như trong trường hợp thẩm phân máu mà trong đó máu và dịch thẩm phân chảy qua thận nhân tạo, sự giảm bớt của gradient nồng độ có thể được giảm đi và sự khuếch tán của chất tan qua màng có thể được tối ưu, bằng cách làm tăng mức lưu lượng máu, dịch thẩm phân hoặc cả hai.
Trong sự vận hành bình thường của thận nhân tạo, máu chảy một cách liên tục hoặc gián đoạn trở lại vào trong tĩnh mạch. Tổng lượng máu trong thận nhân tạo ở bất cứ một thời điểm nào thường dưới 500 milliliters, mức lưu lượng có thể là vài trăm milliliters mỗi phút và tổng diện tích bề mặt khuếch tán là giữa 0.6 và 2.5 m2. Để ngăn cản sự đông lại của máu trong thận nhân tạo, một lượng nhỏ heparin được truyền vào trong máu khi nó đi vào trong thận nhân tạo. Ngoài sự khuếch tán của các chất tan, sự vận chuyển khối (mass transfer) của các chất tan và nước có thể được tạo ra bằng cách tạo ra một áp suất thủy tĩnh để đẩy dịch và các chất tan qua các màng của bộ phận thẩm phân (bộ phân lọc) (dialyzer); loại lọc này được gọi là “bulk flow” (tạm dịch là “dòng chảy khối”) hay “hemofiltration” (tạm dịch là “siêu lọc máu”).
Dịch thẩm phân (dịch lọc máu)
Bảng 1 so sánh các thành phần trong một dịch thẩm phân thông thường với các thành phần trong huyết tương thông thường và huyết tương nhiễm urea huyết. Chú ý rằng nồng độ của các ions và các chất khác trong dịch thẩm phân thì không giống như các nồng độ trong huyết tương bình thường hay trong huyết tương nhiễm urea. Thay vào đó, chúng được điều chỉnh đến các mức cần để gây ra sự di chuyển thích hợp của nước và các chất tan qua màng trong suốt quá trình thẩm phân.
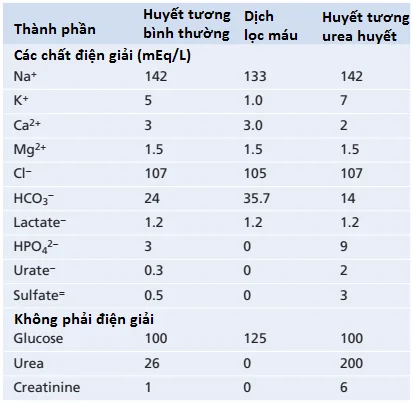
Chú ý rằng không có phosphate, urea, sulfate hay creatinine trong dịch thẩm phân; tuy nhiên, các chất này xuất hiện ở các nồng độ cao trong máu nhiễm urea. Vì thế, khi một bệnh nhân nhiễm urea huyết trải qua thẩm phân, các chất này bị mất với các lượng lớn vào trong dịch thẩm phân.
Tính hiệu quả của thận nhân tạo có thể được biểu hiện ở lượng huyết tương mà có thể được làm sạch các chất khác nhau mỗi phút, mà, như được nói đến trong loạt bài viết trước, là phương tiện chủ yếu để biểu thị hiệu quả về mặt chức năng của chính các thận trong việc loại bỏ khỏi cơ thể các chất không mong muốn. Hầu hết các thận nhân tạo có thể loại bỏ urea khỏi huyết tương ở một mức là 100 đến 225 ml/phút, điều mà cho thấy ít nhất đối với sự bài tiết urea, thận nhân tạo có thể thực hiện chức năng nhanh khoảng 2 lần so với hai thận bình thường cùng nhau thực hiện chức năng, khi mà độ thanh thải urea chỉ khoảng 70 ml/phút. Tuy nhiên, thận nhân tạo được sử dụng chỉ 4 đến 6 giờ/ngày, ba lần mỗi tuần. Vì thế, độ thanh thải huyết tương tổng quan thì vẫn bị giới hạn một cách đáng kể khi thận nhân tạo thay thế các thận bình thường. Ngoài ra, cũng quan trọng trong việc nhớ là thận nhân tạo không thể thay thế một số chức năng khác của các thận, như bài tiết erythropoietin, mà cần cho sự sản xuất hồng cầu.
Cảm ơn các bạn đã theo dõi bài viết. Hẹn gặp lại các bạn trong các bài viết tiếp theo nhé !!!