Bệnh thận mạn tính thường liên quan với sự mất nephron chức năng không thể đảo ngược
Tổn thương đối với khoảng kẽ thận là một nguyên nhân của bệnh thận mạn tính – viêm thận kẽ
Bệnh nguyên phát hay thứ phát của khoảng kẽ thận được gọi là viêm thận kẽ (interstitial nephritis). Nhìn chung, tình trạng này có thể là do tổn thương của mạch máu, cầu thận hay ống thận mà phá hủy các nephrons riêng rẽ hoặc nó có thể liên quan với các tổn thương nguyên phát đối với khoảng kẽ thận bởi các chất độc, các thuốc và các nhiễm trùng.
Tổn thương thận kẽ được gây ra bởi nhiễm khuẩn được gọi là viêm thận-bể thận (pyelonephritis). Nhiễm trùng này có thể do các loại vi khuẩn khác nhau nhưng đặc điệt là do Escherichia coli, mà có nghiêm gốc từ sự phơi nhiễm phân của đường tiết niệu. Các vi khuẩn này đến các thận bởi đường máu hoặc thường gặp hơn là bởi sự đi lên từ đường tiết niệu dưới thông qua các niệu quản đến các thận.
Mặc dù bàng quang bình thường có khả năng loại bỏ vi khuẩn một cách dễ dàng nhưng có hai tình trạng lâm sàng mà có thể ảnh hưởng đến sự loại bỏ bình thường vi khuẩn khỏi bàng quang: (1) sự mất khả năng làm rỗng bàng quang một cách hoàn toàn, để lại nước tiểu dư trong bàng quang; (2) sự tắc đường ra của nước tiểu. Với sự suy giảm khả năng đẩy vi khuẩn khỏi bàng quang, vi khuẩn sẽ nhân lên và bàng quang trở nên bị viêm, một tình trạng được gọi là viêm bàng quang (cystitis). Một khi viêm bàng quang xảy ra, nó sẽ vẫn cục bộ tại chỗ mà không đi lên các thận hoặc ở một số người, vi khuẩn có thể đến bể thận (chậu thận) do tình trạng bệnh lý mà trong đó nước tiểu được đẩy lên trên một hoặc cả hai niệu quản trong suốt quá trình đi tiểu. Tình trạng này được gọi là trào ngược bàng quang-niệu quản (vesicoureteral reflux) và là do sự suy yếu của thành bàng quang trong việc đóng niệu quản trong suốt quá trình đi tiểu; kết quả, một ít nước tiểu được đẩy lên trên về phía thận, mang theo nó vi khuẩn mà có thể đến bể thận và tủy thận, nơi mà chúng có thể khởi động nhiễm trùng và viêm liên quan với viêm thận-bể thận.
Viêm thận-bể thận bắt đầu trong tủy thận và vì thế thường ảnh hưởng đến chức năng của tủy thận nhiều hơn việc nó ảnh hưởng đến vỏ thận, ít nhất là trong các giai đoạn ban đầu. Bởi vì một trong số các chức năng chủ yếu của tủy thận là cung cấp cơ chế ngược dòng cho sự cô đặc nước tiểu nên các bệnh nhân mắc viêm thận-bể thận thường có sự suy giảm khả năng cô đặc nước tiểu đáng kể.
Với viêm thận-bể thận kéo dài, sự xâm nhập các thận bởi vi khuẩn không chỉ gây ra tổn thương đối với khoảng kẽ tủy thận mà còn gây ra tổn thương tiến triển của các ống thận, các mao mạch cầu thận và các cấu trúc khác trên khắp thận. Cuối cùng, các phần lớn mô thận chức năng bị mất và CKD có thể phát triển.
Hội chứng thận hư – sự bài tiết protein trong nước tiểu
Hội chứng thận hư (nephrotic syndrome), được đặc trưng bởi sự mất các lượng lớn proteins vào trong nước tiểu, phát triển ở nhiều bệnh nhân mắc bệnh thận. Trong một số trường hợp, hội chứng này xảy ra mà không có bằng chứng của các bất thường đáng kể khác của chức năng thận, nhưng thường liên quan với một ít mức độ của CKD.
Nguyên nhân của sự mất protein trong nước tiểu thường là tăng tính thấm của màng cầu thận. Vì thế, bất cứ bệnh lý nào mà làm tăng tính thấm của màng có thể gây ra hội chứng thận hư. Những bệnh như thế bao gồm: (1) viêm cầu thận mạn tính (chronic glomerulonephritis), mà ảnh hưởng chủ yếu đến các mao mạch cầu thận và thường gây ra sự tăng tính thấm đáng kể của màng cầu thận; (2) amyloidosis, mà do sự lắng đọng của chất proteinoid bất thường trong các thành của các mạch máu và làm tổn thương nghiêm trọng màng đáy của các mao mạch cầu thận; và (3) hội chứng thận hư thay đổi tối thiểu (minimal-change nephrotic syndrome) mà không liên quan với các bất thường lớn trong màng mao mạch cầu thận mà có thể được phát hiện với kính hiển vi quang học. Như được nói đến trong loạt bài viết trước, bệnh thận thay đổi tối thiểu liên quan với một đáp ứng miễn dịch bất thường và tăng sự bài tiết các cytokines của tế bào T mà làm tổn thương tế bào có chân và tăng tính thấm với các protein trọng lượng phân tử thấp, như albumin.
Bệnh thận tổn thương tối thiểu có thể xảy ra ở người trưởng thành, nhưng nó thường xảy ra hơn ở trẻ em giữa 2 và 6 tuổi. Tăng tính thấm của màng mao mạch cầu thận đôi khi cho phép đến 40 grams protein huyết tương mất vào trong nước tiểu mỗi ngày, đó là lượng cực kỳ lớn đối với một trẻ nhỏ. Vì thế, nồng độ protein huyết tương của trẻ em thường giảm xuống dưới 2 g/dl và áp suất thẩm thấu keo giảm từ một giá trị bình thường là 28 mm Hg xuống thấp hơn 10 mm Hg. Kết quả của nồng độ thẩm thấu keo thấp này trong huyết tương là các lượng lớn dịch thoát từ các mao mạch trên khắp cơ thể vào trong hầu hết các mô, gây ra phù nghiêm trọng, như được nói đến trong loạt bài viết trước.
Chức năng nephron trong bệnh thận mạn
Sự mất các nephrons chức năng cần các nephrons sống sót bài tiết nhiều nước và chất tan hơn. Sẽ hợp lý khi nghi ngờ rằng giảm số lượng nephrons chức năng, mà làm giảm GFR, cũng sẽ gây ra các sự giảm nhiều trong sự bài tiết nước và các chất tan của thận. Tuy nhiên, các bệnh nhân mà mất đến 75% đến 80% nephrons của họ có thể bài tiết các lượng nước và các chất điện giải bình thường mà không có sự tích tụ dịch hay hầu hết các chất điện giải nghiêm trọng trong các dịch cơ thể. Tuy nhiên, sự giảm nhiều hơn trong số lượng các nephrons dẫn đến sự giữ lại chất điện giải và dịch và tử vong thường xảy ra khi số lượng các nephrons giảm xuống bên dưới 5% đến 10% so với bình thường.
Ngược lại với các chất điện giải, nhiều sản phẩm thải của chuyển hóa, như urea và creatinine, tích tụ gần như tỷ lệ với số lượng các nephrons bị phá hủy. Nguyên nhân cho điều này chính là các chất như creatinine và urea phụ thuộc nhiều vào sự lọc cầu thận cho sự bài tiết của chúng và chúng không được tái hấp thu một cách mạnh mẽ như các chất điện giải. Creatinine, chẳng hạn, không được tái hấp thu và mức bài tiết thì gần bằng với mức mà nó được lọc (bỏ qua lượng nhỏ được bài tiết):
Mức lọc creatinine = GFR x Nồng độ creatinine huyết tương = Mức bài tiết creatinine
Vì thế, nếu như GFR giảm, mức bài tiết creatinine cũng giảm tạm thời, gây ra sự tích tích của creatinine trong các dịch cơ thể và làm tăng nồng độ trong huyết tương cho đến khi mức bài tiết của creatinine trở về bình thường – cùng mức mà ở đó creatinine được sản xuất trong cơ thể (Hình 1). Vì thế, dưới các tình trạng ổn định, mức bài tiết creatinine bằng với mức sản xuất creatinine, mặc cho các sự giảm trong GFR; tuy nhiên, mức bài tiết creatinine bình thường này xảy ra nhờ nồng độ creatinine huyết tương tăng lên, như được thể hiện trong đường cong A của Hình 2.

Một số chất tan, như phosphate, urate và ion hydrogen, thường được duy trì gần khoảng giá trị bình thường cho đến khi GFR giảm xuống dưới 20% đến 30% bình thường. Sau đó, các nồng độ huyết tương của các chất này tăng lên, nhưng không tỷ lệ với sự giảm trong GFR, như được thể hiện trong đường cong B của Hình 2. Sự duy trì của các nồng độ huyết tương tương đối hằng định của các chất này khi GFR giảm được thực hiện bằng cách bài tiết các phần lớn dần của các lượng các chất tan này mà được lọc ở các mao mạch cầu thận; điều này diễn ra bằng cách làm giảm mức tái hấp thu hoặc trong một số trường hợp, bằng cách làm tăng các mức bài tiết của ống thận.
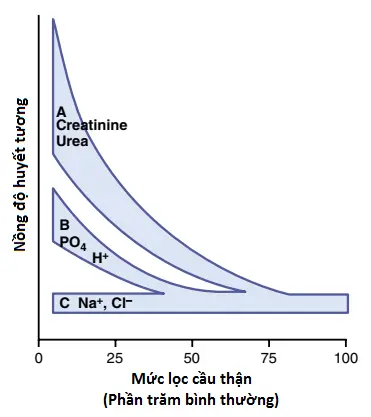
Trong trường hợp của ion natri và chloride, các nồng độ trong huyết tương của chúng được duy trì gần như hằng định, thậm chí với các sự giảm mạnh trong GFR (xem đường cong C của Hình 2). Sự duy trì này được thực hiện bởi sự giảm mạnh tái hấp thu của ống thận đối với các chất điện giải này.
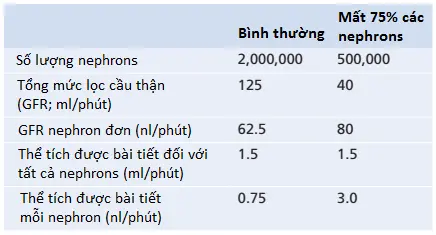
Ví dụ, với một sự mất 75% số nephrons chức năng, mỗi nephron sống sót phải bài tiết nhiều gấp 4 lần lượng natri và 4 lần thể tích như dưới các điều kiện bình thường (Bảng 1). Một phần của sự thích nghi này xảy ra nhờ tăng lưu lượng máu và tăng GFR trong mỗi nephrons sống sót do sự phì đại của các mạch máu và các mao mạch cầu thận, cũng như là các sự thay đổi chức năng mà làm cho các mạch máu giãn. Ngay cả với các sự giảm nhiều trong tổng mức GFR, các mức bình thường của sự bài tiết thận vẫn có thể được duy trì bằng cách làm giảm mức mà ở đó các ống thận tái hấp thu nước và các chất tan.
Đẳng tỷ trọng niệu – sự mất khả năng của thận trong khả năng cô đặc hay pha loãng nước tiểu. Một tác động quan trọng của mức dòng chảy ống thận nhanh mà xảy ra trong các nephrons còn lại của các thận mắc bệnh là các ống thận mất khả năng cô đặc hay pha loãng nước tiểu của chúng một cách hoàn toàn. Khả năng cô đặc của thận bị suy giảm chủ yếu là do nguyên nhân sau: (1) dòng chảy nhanh của dịch ống thận qua các ống thu thập ngăn cản sự tái hấp thu nước một cách đầy đủ và (2) dòng chảy nhanh qua cả quai Henle và các ống thu thập ngăn cản cơ chế ngược dòng không được vận hành một cách hiệu quả để cô đặc các chất tan trong dịch kẽ tủy thận. Vì thế, khi ngày càng nhiều nephrons bị phá hủy, khả năng cô đặc tối đa của thận giảm xuống và nồng độ thẩm thấu và trọng lượng riêng nước tiểu tiệm cận đến nồng độ thẩm thấu và trọng lượng riêng của dịch lọc cầu thận, như được thể hiện trong Hình 3.
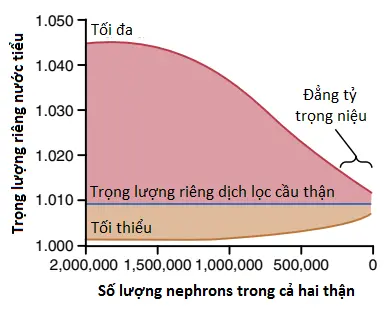
Cơ chế pha loãng trong thận cũng bị suy giảm khi số lượng nephrons giảm xuống một cách đáng kể bởi vì sự đẩy nhanh của dịch qua các quai Henle và các tải chất tan cao như urea gây ra một nồng độ chất tan tương đối cao trong dịch ống thận của phần nephron này. Kết quả, khả năng pha loãng của thận giảm và nồng độ thẩm thấu nước tiểu và trọng lượng riêng tối thiểu tiệm cận đến giá trị của dịch lọc cầu thận. Bởi vì cơ chế cô đặc trở nên suy giảm đến một mức độ lớn hơn cơ chế pha loãng trong CKD nên một xét nghiệm lâm sàng quan trọng của chức năng thận để xác định xem các thận có thể cô đặc nước tiểu tốt đến mức nào khi lượng nước uống vào của một người bị hạn chế trong 12 giờ hoặc hơn.
Các tác động của suy thận lên các dịch cơ thể – urea huyết
Tác động của CKD lên các dịch cơ thể phụ thuộc vào các yếu tố sau: (1) nước và thức ăn ăn vào; và (2) mức độ giảm suy giảm chức năng thận. Giả sử rằng một người mắc suy thận hoàn toàn liên tục tiêu hóa cùng các lượng nước và thức ăn thì các nồng độ của các chất khác nhau trong dịch ngoại bào sẽ thay đổi, như được thể hiện trong Hình 4. Các tác động quan trọng bao gồm: (1) phù toàn thân (generalized edema) do sự giữ lại muối và nước; (2) nhiễm toan (acidosis) do suy các thận trong việc loại bỏ khỏi cơ thể các sản phẩm có tính acid bình thường; (3) nồng độ cao của các nitrogens không phải protein (nonprotein nitrogens) – đặc biệt là urea, creatinine và uric acid – do sự suy yếu của cơ thể trong việc bài tiết các sản phẩm cuối cùng của chuyển hóa các proteins; và (4) các nồng độ cao của các chất khác mà được bài tiết bởi thận, bao gồm phenols, sulfates, phosphates, kali và bases guanidine. Toàn bộ tình trạng này được gọi là urea huyết (uremia) do nồng độ cao của urea trong các dịch cơ thể.

Sự giữ lại nước và sự phát triển của phù trong bệnh thận mạn tính. Nếu như nước hấp thu bị hạn chế ngay lập tức sau khi tổn thương thận cấp bắt đầu, toàn bộ thành phần dịch cơ thể có thể chỉ trở nên hơi tăng. Nếu như lượng dịch hấp thu không được giới hạn và bệnh nhân uống trong đáp ứng với các cơ chế khát bình thường thì các dịch cơ thể sẽ bắt đầu tăng nhanh chóng.
Miễn là muối và dịch hấp thu không dư thừa thì sự tích tụ dịch trong CKD có thể không nghiêm trọng cho đến khi chức năng thận giảm xuống 25% so với bình thường hoặc thấp hơn. Nguyên nhân cho việc này, như được nói đến trước đây, là do các nephrons còn sống bài tiết các lượng muối và nước lớn hơn. Ngay cả sự giữ lại dịch nhỏ xảy ra, cùng với tăng sự bài tiết renin và sự hình thành Ang II mà thường xảy ra trong bệnh thận thiếu máu, thường gây ra tăng huyết áp nghiêm trọng. Khi chức năng thận giảm đến nỗi mà lọc máu (dialysis) được cần đến để bảo toàn sự sống thì tăng huyết áp gần như phát triển không thể khác được. Ở nhiều bệnh nhân trong số này, sự giảm mạnh lượng muối ăn vào hay sự loại bỏ nhiều dịch ngoại bào bởi sự lọc máu có thể kiểm soát tăng huyết áp. Một số bệnh nhân tiếp tục có tăng huyết áp, thậm chí sau khi lượng natri quá mức được loại bỏ bởi lọc máu. Trong nhóm bệnh nhân này, sự loại bỏ các thận thiếu máu thường sẽ điều chỉnh được tăng huyết áp (miễn là sự giữ lại dịch bị ngăn cản bởi lọc máu) bởi vì nó loại bỏ nguồn bài tiết renin quá mức và sự tăng hình thành Ang II kế tiếp.
Sự tăng trong urea và các nitrogens không phải protein khác (azot huyết [azotemia]). Các nitrogen không phải protein bao gồm urea, uric acid, creatinine và một số hợp chất ít quan trọng hơn. Các nitrogens không phải protein này, nhìn chung, là các sản phẩm cuối cùng của chuyển hóa protein và phải được loại bỏ khỏi cơ thể để đảm bảo sự chuyển hóa protein bình thường liên tục trong các tế bào. Các nồng độ của các nitrogen không phải protein này, đặc biệt là của urea, có thể tăng lên cao đến 10 lần so với bình thường trong suốt 1 đến 2 tuần của suy thận hoàn toàn. Với CKD, các nồng độ tăng gần như tỉ lệ với mức độ giảm của GFR. Vì lý do này, đo các nồng độ của các chất này, đặc biệt là urea và creatinine, cung cấp một phương tiện quan trọng trong đánh giá mức độ nghiêm trọng của CKD.
Nhiễm toan trong CKD. Mỗi ngày, cơ thể bình thường sản xuất khoảng 50 đến 80 millimoles nhiều acid chuyển hóa hơn so với kiềm chuyển hóa. Vì thế, khi các thận suy giảm chức năng, acid tích tụ trong các dịch cơ thể. Các hệ đệm của các dịch cơ thể bình thường có thể đệm 500 đến 1000 millimoles acid mà không làm tăng đến các mức gây tử vong trong nồng độ H+ dịch ngoại bào và các hợp chất phosphate trong các xương có thể đệm thêm vài nghìn millimoles H+. Tuy nhiên, khi khả năng đệm này cạn kiệt, pH máu giảm đáng kể và bệnh nhân sẽ hôn mê và tử vong nếu như pH giảm xuống dưới khoảng 6.8.
Thiếu máu trong bệnh thận mạn tính được gây ra bởi giảm sự bài tiết erythropoietin. Thiếu máu hầu như luôn luôn phát triển ở những bệnh nhân mắc CKD nghiêm trọng. Nguyên nhân quan trọng nhất của thiếu máu là giảm sự bài tiết erythropoietin của thận, là chất mà kích thích tủy xương sản xuất các tế bào hồng cầu. Nếu như các thận bị tổn thương nghiêm trọng, chúng không thể hình thành đủ các lượng erythropoietin, điều mà dẫn đến suy giảm sản xuất tế bào hồng cầu và thiếu máu xảy ra tiếp theo.
Tuy nhiên, sự có sẵn từ năm 1989 của erythropoietin tái tổ hợp (recombinant erythropoietin) đã cung cấp một phương tiện trong điều trị thiếu máu ở những bệnh nhân mắc suy thận mạn tính.
Nhuyễn xương (osteomalacia) trong bệnh thận mạn tính được gây ra bởi giảm sản xuất vitamin D hoạt hóa bởi sự giữ lại phosphate bởi các thận. CKD kéo dài cũng gây ra nhuyễn xương (osteomalacia), một tình trạng mà trong đó các xương một phần bị hấp thụ và vì thế, trở nên suy yếu nghiêm trọng. Một nguyên nhân quan trọng của nhuyễn xương là vitamin D phải được chuyển bởi một quá trình hai giai đoạn, đầu tiên trong gan và sau đó trong thận, thành 1,25-dihydroxycholecalciferol trước khi nó có khả năng thúc đẩy sự hấp thụ canxi từ ruột. Vì thế, tổn thương nghiêm trọng đối với thận làm giảm đáng kể nồng độ vitamin D hoạt động trong máu, điều mà cuối cùng làm giảm sự hấp thu canxi ở ruột và sự có mặt sẵn của canxi cho các xương.
Một nguyên nhân quan trọng khác của sự mất khoáng của xương trong CKD là sự tăng lên trong nồng độ phosphate huyết thanh mà xảy ra do giảm GFR. Sự tăng lên trong mức phosphate huyết thanh này làm tăng sự liên kết của phosphate với canxi trong huyết thanh, vì thế, làm giảm nồng độ canxi ion hóa huyết thanh của huyết tương, điều mà, cuối cùng, kích thích sự bài tiết hormone cận giáp (parathyroid hormone). Tình trạng cường cận giáp thứ phát (secondary hyperparathyroidism) này sau đó kích thích sự giải phóng của canxi từ các xương, gây ra sự mất khoáng nhiều hơn của xương.
Tăng huyết áp và bệnh thận
Như được nói đến trước trong loạt bài viết này, tăng huyết áp có thể làm tăng cường tổn thương đối với các mao mạch cầu thận và các mạch máu của các thận và là một nguyên nhân chính của ESRD. Các bất thường của chức năng thận cũng có thể gây ra tăng huyết áp, như được nói đến trong loạt bài viết trước. Vì thế, mối liên hệ giữa tăng huyết áp và bệnh thận có thể, trong một số trường hợp, dẫn đến một vòng “luẩn quẩn” – tổn thương thận nguyên phát dẫn đến tăng huyết áp, tình trạng mà gây ra tổn thương đối với các thận nhiều hơn và làm tăng huyết áp nhiều hơn nữa, cho đến khi ESRD phát triển.
Không phải tất cả các loại bệnh thận đều gây ra tăng huyết áp bởi vì tổn thương đối với các phần nhất định của thận gây ra urea huyết (uremia) mà không gây ra tăng huyết áp. Bất kể là vậy, một số loại tổn thương thận thì đặc biệt dễ gây ra tăng huyết áp. Một sự phân loại bệnh thận tương ứng với các tác động làm tăng huyết áp hoặc không làm tăng huyết áp được cung cấp trong các phần tiếp theo nhé.
Cảm ơn các bạn đã theo dõi bài viết. Hẹn gặp lại các bạn trong các bài viết tiếp theo nhé !!!