Viêm: Vai trò của các bạch cầu trung tính và đại thực bào
Các đáp ứng của đại thực bào và bạch cầu trung tính trong suốt quá trình viêm
Sự xâm nhập của đại thực bào lần thứ hai vào trong mô viêm là một “lớp phòng ngự” thứ ba. Cùng với sự xâm nhập của các bạch cầu trung tính, bạch cầu đơn nhân từ máu đi vào trong mô viêm và phình to để trở thành các đại thực bào. Tuy nhiên, số lượng bạch cầu đơn nhân trong máu tuần hoàn thì thấp. Ngoài ra, “hồ tích trữ” của các bạch cầu đơn nhân trong tủy xương thì thấp hơn nhiều so với bạch cầu trung tính. Vì thế, sự tích tụ của các đại thực bào trong vùng mô viêm thì chậm hơn nhiều so với của các bạch cầu trung tính, mà cần một vài ngày để trở nên hiệu quả. Hơn thế nữa, thậm chí sau khi xâm nhập mô viêm, các bạch cầu đơn nhân vẫn chưa trưởng thành, cần 8 giờ hoặc lâu hơn để phình to đến các kích thước lớn hơn và phát triển các lượng lysosomes khổng lồ. Chỉ sau đó chúng mới đạt đến khả năng đầy đủ của các đại thực bào mô (tissue macrophages) cho quá trình thực bào. Sau một vài ngày đến một vài tuần, các đại thực bào cuối cùng chiếm ưu thế trong số các tế bào thực bào của vùng viêm do sự tăng sản xuất đáng kể của tủy xương đối với các bạch cầu đơn nhân mới, như được giải thích sau.
Như đã lưu ý, các đại thực bào có thể thực bào nhiều vi khuẩn hơn nhiều (nhiều khoảng gấp năm lần) và các phần tử lớn hơn nhiều, bao gồm thậm chí cả các bạch cầu trung tính và các lượng lớn mô hoại tử, so với bạch cầu trung tính. Ngoài ra, các đại thực bào đóng một vai trò quan trọng trong việc khởi động sự phát triển của các kháng thể, như được nói đến trong loạt bài viết tiếp theo.
Sự tăng sản xuất bạch cầu hạt và bạch cầu đơn nhân bởi tủy xương là “lớp phòng ngự” thứ tư. Lớp phòng ngự thứ tư là sự tăng sản xuất đáng kể của các bạch cầu hạt và bạch cầu đơn nhân bởi tủy xương. Hoạt động này do sự kích thích các tế bào tiền thân của bạch cầu hạt và bạch cầu đơn nhân của tủy xương. Tuy nhiên, mất 3 đến 4 ngày trước khi các bạch cầu hạt và bạch cầu đơn nhân được hình hành mới đạt đến giai đoạn rời khỏi tủy xương. Nếu như sự kích thích từ mô viêm tiếp tục, tủy xương có thể tiếp tục sản xuất các tế bào này với các lượng lớn trong nhiều tháng và thậm chí nhiều năm, đôi khi ở một mức 20 đến 50 lần so với bình thường.
Sự kiểm soát phản hồi của các đáp ứng đại thực bào và bạch cầu trung tính
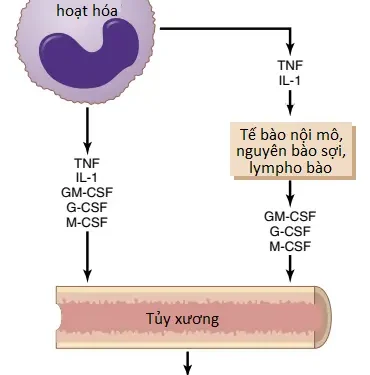
Mặc dù nhiều hơn hai tá (two dozen) yếu tố mà tác động đến sự kiểm soát đáp ứng đại thực bào đối với quá trình viêm nhưng năm trong số này được cho là đóng các vai trò chủ yếu. Chúng được thể hiện trong Hình 1 và bao gồm các yếu tố sau đây: (1) yếu tố hoại tử u (tumor necrosis factor – TNF); (2) interleukin-1 (IL-1), (3) yếu tố kích thích cụm bạch cầu hạt-bạch cầu đơn nhân (granulocyte-monocyte colony-stimulating factor – GM-CSF); (4) yếu tố kích thích cụm bạch cầu hạt (granulocyte colony-stimulating factor – G-CSF); và (5) yếu tố kích thích cụm bạch cầu đơn nhân (monocyte colony-stimulating factor – M-CSF). Các yếu tố này được hình thành bởi các tế bào đại thực bào hoạt hóa trong các mô viêm và với các lượng nhỏ hơn bởi các tế bào mô viêm khác.
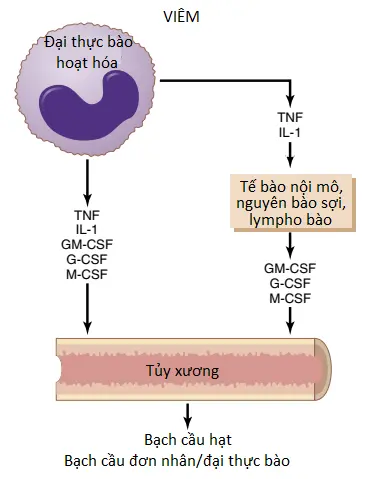
Nguyên nhân của tăng sản xuất bạch cầu hạt và bạch cầu đơn nhân bởi tủy xương chủ yếu là ba yếu tố kích thích cụm; một trong số này, GM-CSF, kích thích cả sự sản xuất bạch cầu hạt và bạch cầu đơn nhân; hai yếu tố khác, là G-CSF và M-CSF, lần lượt kích thích sự sản xuất của bạch cầu hạt và bạch cầu đơn nhân. Sự kết hợp này của TNF, IL-1 và các yếu tố kích thích cụm cung cấp một cơ chế phản hồi mạnh mẽ mà bắt đầu với sự viêm của mô và tiếp diễn thành sự hình thành của các số lượng lớn WBCs đề kháng mà giúp loại bỏ nguyên nhân viêm.
Sự hình thành của mủ (pus)
Khi các bạch cầu trung tính và đại thực bào nuốt các số lượng lớn các vi khuẩn và mô hoại tử, về bản chất tất cả các bạch cầu trung tính và nhiều, nếu không muốn nói hầu hết, các đại thực bào cuối cùng sẽ chết. Sau một vài ngày, một khoang thường được tạo ra trong các mô viêm. Khoang này chứa các phần khác nhau của mô hoại tử, các bạch cầu trung tính chết, các đại thực bào chết và dịch mô. Hỗn hợp này thường được gọi là mủ (pus). Sau khi sự nhiễm trùng đã ngừng, các tế bào chết và mô hoại tử trong mủ dần dần tự phân giải trong khoảng thời gian nhiều ngày và các sản phẩm cuối cùng được hấp thu vào trong các mô xung quanh và dịch bạch huyết cho đến khi hầu hết các dấu hiệu của tổn thương mô biến mất.
Bạch cầu ái toan (ưa acid) (eosinophils)
Bạch cầu ái toan bình thường chiếm khoảng 2% trong số tất cả các tế bào bạch cầu của máu. Bạch cầu ái toan là các tế bào thực bào yếu và chúng thực thi hóa hướng động, nhưng so với các bạch cầu trung tính thì không rõ là các bạch cầu ái toan có vai trò đáng kể trong việc bảo vệ chống lại các loại nhiễm trùng thông thường hay không.
Tuy nhiên, các bạch cầu ái toan thường được sản xuất với các số lượng lớn ở những người mà bị nhiễm ký sinh trùng và chúng di cư vào trong các mô bị mắc bệnh bởi ký sinh trùng. Mặc dù hầu hết ký sinh trùng là quá lớn để được thực bào bởi các bạch cầu ái toan hay bất cứ các tế bào thực bào nào khác nhưng các bạch cầu ái toan sẽ bám vào trong các ký sinh trùng bởi các phân tử bề mặt đặc hiệu và giải phóng các chất mà giết chết nhiều ký sinh trùng. Ví dụ, một trong số các nhiễm trùng phổ biến nhất là nhiễm sán máng (schistosomiasis), một nhiễm ký sinh trùng được phát hiện thấy ở nhiều đến một phần ba dân số của một số quốc gia đang phát triển ở châu Phi, châu Á và Nam Mỹ. Một ước tính 85% đến 90% các trường hợp trên thế giới nhiễm sán máng là ở châu Phi.
Sán máng ký sinh có thể xâm nhập bất cứ phần nào của cơ thể. Bạch cầu ái toan gắn vào các dạng non của ký sinh trùng và tiêu diệt nhiều trong số đó. Chúng làm được điều này theo một số cách: (1) bằng cách giải phóng các enzyme thủy phân từ các hạt của chúng, mà là các lysosomes đã sửa đổi; (2) cũng có thể bằng cách giải phóng các dạng oxygen phản ứng mạnh mà đặc biệt gây chết đối với ký sinh trùng; và (3) bằng cách giải phóng từ các hạt một polypeptide diệt ấu trùng mạnh được tạm gọi là “protein base chính” (major basic protein).
Trong một số khu vực của thế giới, một bệnh ký sinh trùng khác mà làm tăng bạch cầu ái toan là bệnh nhiễm giun xoắn (hay giun lợn) (trichinosis). Bệnh này là do sự xâm nhập các cơ trong cơ thể bởi ký sinh trùng Trichinella (giun lợn [pork worm]) sau khi một người ăn thịt lợn bị nhiễm giun chưa nấu chín.
Các bạch cầu ái toan có một xu hướng đặc biệt là tập hợp trong các mô mà trong đó các phản ứng dị ứng diễn ra, như trong các mô quanh phế quản của phổi ở người mắc hen và trong da sau một phản ứng da do dị ứng. Hoạt động này được gây ra ít nhất một phần bởi nhiều dưỡng bào và bạch cầu ái kiềm tham gia trong các phản ứng dị ứng, như được nói đến trong phần tiếp theo. Các dưỡng bào và các bạch cầu ái kiềm giải phóng một yếu tố hóa hướng động bạch cầu ái toan (eosinophil chemotactic factor) mà làm cho các bạch cầu ái toan di cư về phía mô dị ứng bị viêm. Các bạch cầu ái toan được cho là giải độc một số chất cảm ứng viêm được giải phóng bởi dưỡng bào và bạch cầu ái kiềm và cũng có thể thực bào và phá hủy các phức hợp dị nguyên-kháng thể (allergen-antibody complexes), vì thế, ngăn cản sự lan rộng quá mức của quá trình viêm cục bộ.
Các bạch cầu ái kiềm (ưa base) (basophils)
Các bạch cầu ái kiềm trong máu tuần hoàn thì tương tự với các dưỡng bào (mast cells) mô lớn nằm ngay bên ngoài nhiều mao mạch trong cơ thể. Cả các dưỡng bào và bạch cầu ái kiềm đều giải phóng heparin vào trong máu. Heparin là một chất mà có thể ngăn cản quá trình đông máu.
Các dưỡng bào và các bạch cầu ái kiềm cũng giải phóng histamine, cũng như là các lượng nhỏ hơn của bradykinin và serotonin. Chủ yếu là các dưỡng bào trong các mô viêm sẽ giải phóng các chất này trong suốt quá trình viêm.
Các tế bào dưỡng bào và các bạch cầu ái kiềm đóng một vai trò quan trọng trong một số loại phản ứng dị ứng bởi vì loại kháng thể mà gây ra các phản ứng dị ứng, là immunoglobulin E (IgE) (globulin miễn dịch E), có một xu hướng đặc biệt là trở nên bám vào các dưỡng bào và các bạch cầu ái kiềm. Sau đó, khi kháng nguyên đặc hiệu đối với kháng thể IgE đặc hiệu phản ứng kế tiếp với kháng thể thì sự bám cuối cùng của kháng nguyên vào kháng thể làm cho dưỡng bào hay bạch cầu ái kiềm giải phóng các lượng tăng lên của histamine, bradykinin, serotonin, heparin, chất phản vệ phản ứng chậm (slow-reacting substance of anaphylaxis) (một hỗn hợp của ba leukotrienes) và một số enzymes lysosomes. Các chất này gây ra các phản ứng mạch máu và mô cục bộ mà điều hòa nhiều, nếu không muốn nói là hầu hết, các biểu hiện của dị ứng. Các phản ứng này được nói đến chi tiết hơn trong loạt bài viết tiếp theo.
Giảm bạch cầu (leukopenia)
Một tình trạng lâm sàng được gọi là giảm bạch cầu (leukopenia), trong đó tủy xương sản xuất rất ít WBCs, đôi khi xảy ra, Tình trạng này làm cho cơ thể không được bảo vệ chống lại nhiều vi khuẩn và các tác nhân khác nhau mà có thể xâm nhập các mô.
Bình thường, cơ thể người sống cộng sinh (symbiosis) với nhiều vi khuẩn bởi vì màng niêm mạc của cơ thể thì luôn luôn tiếp xúc với các số lượng lớn của các vi khuẩn. Miệng hầu như luôn luôn chứa các xoắn khuẩn, phế cầu và liên cầu và cùng các loại vi khuẩn này cũng xuất hiện với mức độ ít hơn trong toàn bộ đường hô hấp. Phần xa đường tiêu hóa thì đặc biệt chứa nhiều các trực khuẩn đại tràng (colon bacilli). Hơn thế nữa, chúng ta có thể luôn luôn tìm thấy các vi khuẩn trên các bề mặt của các mắt, niệu đạo và âm đạo. Bất cứ sự giảm trong số lượng WBCs nào ngay lập tức sẽ cho phép sự xâm nhập của các vi khuẩn mà đã có mặt sẵn vào các mô lân cận.
Trong vòng 2 ngày sau khi tủy xương ngừng sản xuất WBCs, các vết loét có thể xuất hiện trong miệng và đại tràng hoặc một số dạng của nhiễm trùng hô hấp nghiêm trọng có thể phát triển. Các vi khuẩn từ các loét nhanh chóng xâm nhập các mô xung quanh và máu. Nếu như không điều trị, tử vong thường xảy ra trong vòng dưới 1 tuần sau khi tình trạng suy giảm bạch cầu toàn phần cấp tính bắt đầu.
Bức xạ tia X hay tia gamma đối với cơ thể hay phơi nhiễm với các thuốc và các chất hóa học mà chứa các nhân benzene hoặc anthracene, thì dường như gây ra bất sản tủy xương. Một số thuốc thông thường như chloramphenicol (một kháng sinh), thiouracil (được sử dụng để điều trị nhiễm độc tuyến giáp); và thậm chí các thuốc ngủ barbiturate khác nhau đôi khi gây ra giảm bạch cầu, vì thế, thiết lập toàn bộ trình tự nhiễm trùng của rối loạn này.
Sau tổn thương bức xạ trung bình với tủy xương, một số tế bào gốc, nguyên tủy bào và nguyên bào máu có thể vẫn không bị phá hủy trong tủy xương và có khả năng tái tạo tủy xương, miễn là có đủ thời gian. Một bệnh nhân được điều trị phù hợp với truyền máu, cùng với kháng sinh và các thuốc khác để chống lại nhiễm trùng, thường phát triển đủ tủy xương mới trong vòng một vài tuần đến một vài tháng cho các nồng độ tế bào máu trở về mức bình thường.
Bệnh leukemia (bệnh bạch cầu)
Sự sản xuất không kiểm soát của WBCs có thể được gây ra bởi đột biến dạng ung thư của một tế bào dòng lympho hoặc dòng tủy. Quá trình này gây ra bệnh bạch cầu (leukemia), mà thường được đặc trưng bởi các số lượng tăng lên đáng kể của WBCs bất thường trong máu tuần hoàn.
Có hai loại bệnh bạch cầu thông thường, là dòng lympho và dòng tủy. Bệnh bạch cầu dòng lympho (lymphocytic leukemias) được gây ra bởi sự sản xuất do ung thư của các tế bào lympho, thường bắt đầu trong một hạch lympho hoặc các mô lympho khác và lan rộng đến các khu vực khác của cơ thể. Loại thứ hai của bệnh bạch cầu là bệnh bạch cầu dòng tủy (myelogenous leukemia), bắt đầu bởi sự sản xuất do ung thư của các tế bào dòng tủy non trong tủy xương và sau đó lan rộng khắp toàn bộ cơ thể làm cho WBCs được sản xuất trong nhiều mô ngoài tủy – đặc biệt là trong các hạch lympho, lách và gan.
Trong bệnh bạch cầu dòng tủy, quá trình ung thư đôi khi sản xuất các tế bào biệt hóa một phần, gây ra các bệnh bạch cầu được gọi là bệnh bạch cầu dòng bạch cầu trung tính, bệnh bạch cầu dòng bạch cầu ái toan, bệnh bạch cầu dòng bạch cầu ái kiềm hoặc bệnh bạch cầu dòng bạch cầu đơn nhân. Tuy nhiên, thường gặp hơn là các tế bào bệnh bạch cầu dị hình và không biệt hóa và không giống bất cứ WBCs bình thường nào. Thông thường, các tế bào càng không biệt hóa, bệnh bạch cầu càng cấp tính (acute), thường dẫn đến tử vong trong vòng một vài tháng nếu không điều trị. Với một số trong số các tế bào được biệt hóa nhiều hơn, quá trình có thể là mạn tính (chronic), đôi khi phát triển chậm trong vòng 10 đến 20 năm. Các tế bào bệnh bạch cầu, đặc biệt là các tế bào rất không biệt hóa, thường không có chức năng trong việc cung cấp sự bảo vệ khỏi nhiễm trùng bình thường.
Các tác động của bệnh bạch cầu lên cơ thể
Tác động đầu tiên của bệnh bạch cầu là sự tăng trưởng di căn của các tế bào bệnh bạch cầu trong các khu vực bất thường của cơ thể. Các tế bào bệnh bạch cầu từ tủy xương có thể sản sinh nhiều đến nỗi mà chúng xâm nhập vào xương xung quanh, gây ra đau và cuối cùng, một khuynh hướng làm xương dễ gãy.
Hầu như tất cả các bệnh bạch cầu đều cuối cùng lan rộng đến lách, các hạch lympho, gan và các vùng mạch máu khác, bất kể liệu bệnh bạch cầu có nguồn gốc trong tủy xương hay các hạch bạch huyết. Các tác động thông thường trong bệnh bạch cầu là sự phát triển của nhiễm khuẩn, thiếu máu nặng và một khuynh hướng chảy máu được gây ra bởi tình trạng giảm tiểu cầu (thrombocytopenia). Các tác động này chủ yếu do sự thay thế của các tế bào lympho và tủy xương bình thường bởi các tế bào bệnh bạch cầu không thực hiện chức năng.
Cuối cùng, một tác động quan trọng của bệnh bạch cầu lên cơ thể là sự sử dụng quá mức của các chất chuyển hóa bởi các tế bào ung thư đang tăng trưởng. Các mô bệnh bạch cầu sản xuất các tế bào mới nhanh đến nỗi các nhu cầu khổng lồ được tạo ra trên các sự trữ của cơ thể đối với thức ăn, các amino acids chuyên biệt và các vitamins. Kết quả, năng lượng của bệnh nhân bị suy kiệt đáng kể và sự sử dụng quá mức các amino acids bởi các tế bào bệnh bạch cầu gây ra sự suy giảm đặc biệt nhanh chóng của các mô proteins bình thường của cơ thể. Vì thế, trong khi các mô bệnh bạch cầu tăng trưởng, các mô khác trở nên suy yếu. Sau khi tình trạng thiếu hụt chuyển hóa tiếp tục đủ lâu thì chỉ mỗi yếu tố này cũng đủ để gây ra tử vong.
Cảm ơn các bạn đã theo dõi bài viết. Hẹn gặp lại các bạn trong các bài viết tiếp theo nhé !!!