III. Đái tháo đường type 2
T2D là dạng phổ biến nhất của bệnh, ảnh hưởng đến >90% dân số Hoa Kỳ mắc đái tháo đường. Ở Hoa Kỳ, T2D là phổ biến nhất trong số những người Mỹ Hispanic (có gốc gác ở quốc gia nói tiếng Tây Ban Nha), người Mỹ bản địa và người Mỹ gốc Phi, được theo sau bởi người Mỹ gốc Á. Các dân số người Mỹ da trắng/gốc Âu non-Hispanic có tỷ lệ mắc bệnh thấp nhất đối với T2D. Thông thường, T2D phát triển dần dần mà không có các triệu chứng rõ ràng. Bệnh thường được phát hiện bởi các xét nghiệm theo dõi thường xuyên. Tuy nhiên, nhiều người mắc T2D có các triệu chứng của đa niệu và uống nhiều trong thời gian một vài tuần. Đói nhiều có thể xuất hiện nhưng ít phổ biến hơn. Những bệnh nhân mắc T2D có một sự kết hợp của kháng insulin và các tế bào beta rối loạn chức năng (Hình 1) nhưng không cần insulin để duy trì sự sống. Tuy nhiên, ở trên 90% các bệnh nhân này, insulin cuối cùng sẽ được cần để kiểm soát tăng đường huyết và giữ HbA1c <7%. Các thay đổi chuyển hóa được quan sát thấy ở T2D thì nhẹ hơn so với những gì mô tả với T1D, một phần bởi vì sự bài tiết insulin trong T2D, mặc dù không đầy đủ, nhưng chống lại việc tạo thể ketone và làm giảm đi sự phát triển của DKA. (Chú ý: Insulin ức chế sự giải phóng của glucagon). Chẩn đoán được dựa trên sự có mặt của tăng đường huyết như được mô tả ở bài viết trước. Bệnh sinh thì không liên quan với các virus hay các kháng thể tự miễn và không được hiểu hoàn toàn. (Chú ý: Một biến chứng cấp tính của T2D ở người già là một tình trạng tăng thẩm thấu do tăng đường huyết [hyperosmolar hyperglycemic state] được đặc trưng bởi tăng đường huyết nghiêm trọng, mất nước và thay đổi trạng thái tâm thần).

T2D được đặc trưng bởi tăng đường huyết, kháng insulin, suy giảm bài tiết insulin và cuối cùng là suy yếu tế bào beta. Nhu cầu cuối cùng đối với điều trị insulin đã loại bỏ sự ghi nhận đối với T2D là đái tháo đường không phụ thuộc insulin.
A. Đề kháng insulin
Đề kháng insulin (insulin resistance) là khả năng của các mô đích, như gan, mỡ trắng và cơ xương, bị suy giảm trong đáp ứng một cách thích hợp với các nồng độ insulin tuần hoàn bình thường (hoặc tăng lên). Ví dụ, đề kháng insulin được đặc trưng bởi sự sản xuất glucose của gan tăng lên, sự hấp thu glucose giảm bởi cơ và mô mỡ và sự phân giải lipid của mô mỡ tăng lên với sự sản xuất của các acid béo tự do (free fatty acids – FFA).
1. Đề kháng insulin và béo phì: Mặc dù béo phì là nguyên nhân thường gặp nhất của đề kháng insulin và làm tăng nguy cơ của T2D nhưng hầu hết người mắc béo phì và đề kháng insulin không phát triển đái tháo đường. Trong sự vắng mặt của một chức năng tế bào beta bị khiếm khuyết, những người béo phì có thể đền bù cho sự kháng insulin với các mức insulin tăng lên. Ví dụ, Hình 2A cho thấy sự bài tiết insulin thì nhiều hơn hai lần cho đến ba lần ở những bệnh nhân mắc béo phì so với những người có thể trạng gầy hơn. Nồng độ insulin cao hơn này đền bù cho tác động suy giảm của hormone (do đề kháng insulin) và tạo ra các mức glucose máu tương tự với được quan sát thấy ở những người gầy (Hình 2B).

2. Đề kháng insulin và đái tháo đường type 2: Chỉ đề kháng insulin sẽ không dẫn đến T2D. Thay vào đó, T2D phát triển ở những người kháng insulin mà cũng cho thấy suy giảm chức năng tế bào beta. Kháng insulin và nguy cơ kế tiếp đối với sự phát triển của T2D là thường được quan sát thấy ở những người bị béo phì, không hoạt động thể chất, những người già, hoặc ở 3% đến 5% phụ nữ mang thai mà phát triển đái tháo đường thai kỳ. Những bệnh nhân này không thể đền bù đủ sự đề kháng insulin bằng sự giải phóng insulin tăng lên. Hình 3 cho thấy khoảng thời gian cho sự phát triển của đề kháng insulin, tăng đường huyết và sự mất chức năng của tế bào beta. Trước tuổi mà một chẩn đoán T2D có thể được đưa ra, một người có sự đề kháng insulin thì có thể đền bù bằng cách bài tiết các mức insulin cao hơn bình thường (>100% so với bình thường). Kết quả, người đó có khả năng duy trì các mức glucose máu gần với bình thường (mặc dù họ có thể có các mức glucose trong khoảng tiền đái tháo đường). Ở một thời điểm nào đó, sự bài tiết insulin tăng lên thì không đủ để đền bù sự đề kháng insulin và có một sự tăng lên trong nồng độ glucose máu trên ngưỡng chẩn đoán (>125 mg/dl hay ≥6.5% HbA1c). Sau sự chẩn đoán ban đầu, khiếm khuyết tế bào beta có thể gây ra sự làm giảm bài tiết insulin và làm xấu đi tình trạng tăng đường huyết. Sự bài tiết insulin giảm cuối cùng có thể giảm xuống dưới 100% mức bình thường.

3. Các nguyên nhân của sự đề kháng insulin: Sự đề kháng insulin tăng lên theo sự tăng cân và giảm theo sự giảm cân. Mô mỡ quá mức (đặc biệt là ở bụng) thì quan trọng trong sự phát triển của đề kháng insulin. Mô mỡ thì không đơn giản là một mô tích trữ năng lượng, mà còn là một mô bài tiết. Với tình trạng béo phì, có các sự thay đổi trong các sự bài tiết của mô mỡ mà gây ra tình trạng đề kháng insulin (Hình 4). Các sự bài tiết này bao gồm sự bài tiết của các cytokines gây viêm như interleukin 6 và yếu tố hoại tử u alpha bởi các đại thực bào hoạt hóa (viêm thì liên quan với sự đề kháng insulin); tăng tổng hợp leptin, một protein với các tác động gây viêm; và giảm sự bài tiết của adiponectin, một protein với các tác động kháng viêm. Kết quả toàn phần là viêm mạn tính mức độ thấp. Một tác động của đề kháng insulin là tăng phân giải lipid và sự sản xuất FFA (xem Hình 4). Sự có mặt sẵn của FFA làm giảm sự sử dụng glucose, đóng góp vào tăng đường huyết, và làm tăng sự lắng đọng lạc chỗ của TAG trong gan (gan nhiễm mỡ). (Chú ý: Gan nhiễm mỡ gây ra bệnh gan nhiễm mỡ không do rượu [NASH – nonalcoholic fatty liver disease], có thể phát triển). FFA cũng có một tác động gây viêm. Trong dài hạn, FFA làm suy giảm sự truyền tín hiệu của insulin. (Chú ý: Adiponectin làm tăng sự oxy hóa beta của FA. Kết quả, một sự giảm trong protein tế bào mỡ này đóng góp vào sự có mặt sẵn của FFA).

B. Các tế bào beta rối loạn chức năng
Trong T2D, tuyến tụy ban đầu giữ lại khả năng của tế bào beta, tạo ra các mức insulin mà thay đổi từ trên mức bình thường đến dưới mức bình thường. Tuy nhiên, theo thời gian, tế bào beta trở nên ngày càng rối loạn chức năng và không thể bài tiết đủ insulin để điều chỉnh tăng đường huyết hiện hành. Ví dụ, các mức insulin thì cao ở những người mắc T2D có béo phì so với những người mà mắc béo phì tương tự nhưng không mắc T2D. Vì thế, sự tiến triển tự nhiên của bệnh gây ra một khả năng suy giảm trong kiểm soát tăng đường huyết với sự bài tiết insulin nội sinh (Hình 5). Sự suy giảm chức năng tế bào beta có thể được tăng cường bởi các tác động gây độc của tăng đường huyết kéo dài, tăng FFA và một môi trường thúc đẩy viêm.

C. Các thay đổi chuyển hóa
Các bất thường của sự chuyển hóa glucose và TAG ở T2D là kết quả của sự đề kháng insulin mà xảy ra chủ yếu trong gan, cơ xương và mô mỡ trắng (Hình 6).

1. Tăng đường huyết: Tăng đường huyết được gây ra bởi tăng sự sản xuất glucose bởi gan kết hợp với sự sử dụng glucose suy giảm bởi cơ và các mô mỡ (do sự đề kháng insulin). Nhiễm ketone máu thường ít hay không có ở những bệnh nhân T2D bởi vì sự có mặt của insulin, ngay cả trong sự có mặt của sự đề kháng insulin, ngăn cản bất cứ sự tăng lên nào trong quá trình tổng hợp thể ketone của gan.
2. Rối loạn lipid máu: Trong gan, FFA được chuyển thành TAGs, mà được đóng gói trong VLDL và được bài tiết vào trong máu. Chylomicrons giàu TAG trong chế độ ăn được tổng hợp và bài tiết bởi các tế bào niêm mạc ruột sau một bữa ăn. Bởi vì sự thoái hóa TAG của lipoprotein được xúc tác bởi lipoprotein lipase trong mô mỡ thì thấp trong bệnh tiểu đường nên mức chylomicron huyết tương và các mức VLDL được tăng lên, gây ra tăng triacylglycerol máu (Hình 5). Các mức thấp của lipoproteins mật độ cao cũng liên quan với T2D, dường như là do tăng sự thoái hóa.
D. Điều trị
Mục tiêu điều trị T2D là duy trì các nồng độ glucose máu trong các giới hạn bình thường và ngăn cản sự phát triển của các biến chứng dài hạn. Giảm cân, luyện tập thể thao và liệu pháp dinh dưỡng y khoa (các sự điều chỉnh chế độ ăn) thường có thể điều chỉnh tăng đường huyết của T2D mới được chẩn đoán. Các thuốc chống tăng đường huyết đường uống có thể được sử dụng bởi các bệnh nhân T2D để làm giảm các mức glucose máu. (Chú ý: Các thuốc chống tăng đường huyết cũng được gọi là các thuốc hạ đường huyết, bởi vì hạ đường huyết có thể được gây ra từ việc sử dụng chúng). Các thuốc chống tăng đường huyết bao gồm biguanides như metformin (làm giảm quá trình tân tạo đường của gan), sulfonylureas và meglitinides (làm tăng sự bài tiết insulin), thiazolidinediones (làm giảm các mức FFA và tăng độ nhạy cảm insulin ngoại vi), các thuốc ức chế alpha-glucosidase (làm giảm sự hấp thu carbohydrate chế độ ăn), incretins (làm giảm sự bài tiết glucagon, làm tăng sự bài tiết insulin, cảm giác no) và các thuốc ức chế SGLT (làm giảm sự tái hấp thu glucose của thận hay liệu pháp insulin cũng có thể được cần đến để đạt được các mức glucose huyết tương thích hợp. (Chú ý: Phẫu thuật giảm béo ở những người mắc béo phì bệnh lý và T2D được chứng minh là đẩy lùi bệnh trong hầu hết bệnh nhân. Sự đẩy lui bệnh có thể không phải là vĩnh viễn). Các thuốc chống tăng đường huyết và các tác động đặc hiệu mô của chúng lên chuyển hóa glucose và lipid được tóm tắt trong Hình 7.

IV. Tác động lâu dài và sự phòng ngừa
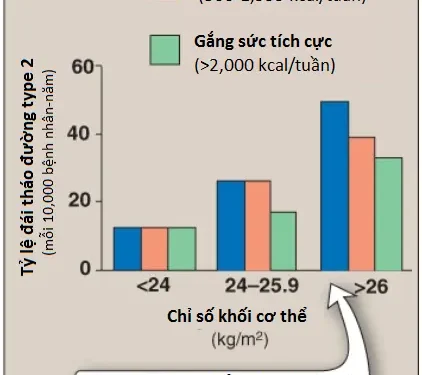
Như được lưu ý trước đây, các điều trị có sẵn điều chỉnh tăng đường huyết của bệnh đái tháo đường nhưng không hoàn toàn làm bình thường chuyển hóa. Sự tăng kéo dài của glucose máu thì liên quan với các biến chứng mạch máu mạn tính của đái tháo đường bao gồm bệnh tim mạch (CVD) và đột quỵ (các biến chứng mạch máu lớn) cũng như là bệnh lý võng mạch, bệnh lý thận và bệnh lý thần kinh (các biến chứng mạch máu nhỏ). Điều trị insulin tích cực làm trì hoãn sự khởi phát và làm chậm tiến triển của một số biến chứng dài hạn. Ví dụ, nguy cơ mắc bệnh lý võng mạch giảm khi sự kiểm soát glucose máu cải thiện và các mức HbA1c giảm (Hình 8). (Chú ý: Dữ liệu liên quan đến tác động của sự kiểm soát chặt chẽ lên CVD ở T2D thì ít rõ ràng). Các lợi ích của sự kiểm soát chặt chẽ glucose máu vượt trội hơn so với tăng nguy cơ của hạ đường huyết nặng ở hầu hết các bệnh nhân. Làm thế nào tăng đường huyết gây ra các biến chứng mạn tính của đái tháo đường thì không rõ ràng. Trong các tế bào mà trong đó sự hấp thu glucose thì không phụ thuộc vào insulin, tăng mức glucose máu dẫn đến tăng glucose nội bào và các chất chuyển hóa của nó. Ví dụ, tăng sorbitol nội bào đóng góp vào sự hình thành của đục thủy tinh thể ở bệnh đái tháo đường. Ngoài ra, tăng đường huyết làm thúc đẩy sự glucose hóa của các protein tế bào trong một phản ứng tương tự với sự hình thành của HbA1c. Các proteins glucose hóa này trải qua thêm các phản ứng và trở thành các sản phẩm cuối được glucose hóa tiến triển (advanced glycation end products – AGEs) mà điều khiển một số trong số các sự thay đổi vi mạch ban đầu của bệnh đái tháo đường và có thể làm giảm sự lành vết thương. Một số AGEs liên kết với một thụ cảm thể màng (RAGE), gây ra sự giải phóng của các phân tử thúc đẩy viêm. Hiện tại không có điều trị phòng ngừa đối với T1D. Nguy cơ T2D có thể được làm giảm đáng kể bằng một phác đồ phối hợp của liệu pháp dinh dưỡng y khoa, giảm cân, luyện tập thể thao và kiểm soát tích cực tăng huyết áp và rối loạn lipid máu. Ví dụ, Hình 9 cho thấy nguy cơ mắc bệnh ở những người bình thường và thừa cân với các mức độ luyện tập thể thao khác nhau.

V. Tóm tắt loạt bài viết

- Đái tháo đường là một nhóm các hội chứng không đồng nhất được đặc trưng bởi một sự tăng lên trong FBG (glucose huyết lúc đói) mà được gây ra bởi một sự thiếu hụt tương đối hay tuyệt đối của insulin (Hình 11).
- Đái tháo đường là nguyên nhân hàng đầu gây mù lòa và cắt cụt chi ở người trưởng thành và là một nguyên nhân chính của suy thận, tổn thương thần kinh, nhồi máu cơ tim và đột quỵ.
- Đái tháo đường có thể được phân loại thành hai nhóm, T1D và T2D.
- T1D chiếm khoảng 10% trong số >30 triệu trường hợp mắc đái tháo đường ở Hoa Kỳ. Bệnh được đặc trưng bởi một sự suy giảm tuyệt đối của insulin được gây ra bởi một bệnh tự miễn trên các tế bào beta của tuyến tụy. Sự phá hủy này cần một sự kích thích từ môi trường (như một nhiễm virus) và một yếu tố quyết định di truyền mà làm cho các tế bào beta được xác định nhầm là “không phải của cơ thể”. Các bất thường chuyển hóa của T1D bao gồm tăng đường huyết, DKA (nhiễm toan ketone do đái tháo đường) và tăng triacylglycerol máu mà gây ra do sự thiếu hụt insulin. Những người mắc T1D phải dựa vào insulin ngoại sinh được truyền dưới da để kiểm soát tăng đường huyết và nhiễm toan ketone.
- T2D có một yếu tố di truyền mạnh. Nó gây ra do một sự kết hợp của sự đề kháng insulin và các tế bào beta rối loạn chức năng. Sự đề kháng insulin là khả năng suy giảm của các mô đích, như gan, mỡ trắng và cơ xương, trong đáp ứng một cách thích hợp với các nồng độ insulin tuần hoàn bình thường (hoặc tăng lên). Béo phì là nguyên nhân thường gặp nhất của sự đề kháng insulin. Tuy nhiên, hầu hết những người mắc béo phì và đề kháng insulin thì không phát triển đái tháo đường. Trong sự vắng mặt của một chức năng tế bào beta khiếm khuyết, những người béo phì mà không mắc đái tháo đường có thể đền bù sự đề kháng insulin với các mức insulin tăng lên. Chỉ sự đề kháng insulin sẽ không dẫn đến T2D. Thay vào đó, T2D phát triển ở những người đề kháng insulin mà cũng cho thấy chức năng tế bào beta suy giảm. Các sự thay đổi chuyển hóa cấp tính quan sát thấy trong T2D thì nhẹ hơn so với những gì mô tả đối với dạng đái tháo đường type 1 phụ thuộc insulin một cách hoàn toàn, một phần bởi vì sự bài tiết insulin ở T2D, mặc dù không đầy đủ, nhưng kháng lại được quá trình tổng hợp thể ketone và làm giảm đi sự phát triển của DKA.
- Các điều trị sẵn có đối với đái tháo đường giúp điều chỉnh tình trạng tăng đường huyết mà không làm bình thường hóa chuyển hóa một cách hoàn toàn. Sự tăng lên kéo dài của glucose máu thì liên quan với các biến chứng mạn tính của đái tháo đường bao gồm CVD và đột quỵ (mạch máu lớn) cũng như là bệnh lý võng mạc, bệnh lý thận và bệnh lý thần kinh (mạch máu nhỏ).
Các bạn có thể xem bài viết mới trên Facebook tại đây: https://www.facebook.com/profile.php?id=61550892771585
Các bạn có thể xem bài viết trước tại đây: https://docsachxyz.com/dai-thao-duong-diabetes-mellitus-phan-1/
Cảm ơn các bạn đã theo dõi bài viết. Hẹn gặp lại các bạn trong các bài viết tiếp theo nhé !!!