Vai trò của hệ thống renin-angiotensin trong kiểm soát áp suất động mạch
2. Tăng huyết áp gây ra bởi khối u tiết renin hay thiếu máu thận
Đôi khi, một khối u của các tế bào JG bài tiết renin xuất hiện và bài tiết các lượng renin lớn, gây ra sự hình thành của các lượng lớn angiotensin II. Trong tất cả các bệnh nhân mà hiện tượng này xảy ra thì tăng huyết áp nặng sẽ phát triển. Ngoài ra, khi các lượng lớn angiotensin II được truyền một cách liên tục nhiều ngày hoặc nhiều tuần vào trong các động vật thì tăng huyết áp dài hạn nghiêm trọng sẽ phát triển.
Chúng ta đã lưu ý rằng angiotensin II có thể làm tăng áp suất động mạch theo 2 cách:
1. Bằng cách co các tiểu động mạch trên khắp toàn bộ cơ thể, bằng cách đó, làm tăng tổng sức cản ngoại vi và áp suất động mạch; tác động này xuất hiện trong vòng vài giây sau khi bắt đầu truyền các lượng lớn angiotensin II.
2. Bằng cách làm cho các thận giữ lại muối và nước; qua một khoảng thời gian nhiều ngày, thậm chí với các lượng angiotensin II trung bình, có thể gây ra tăng huyết áp thông qua các hoạt động trên thận của nó, nguyên nhân chủ yếu của sự tăng lên dài hạn trong áp suất động mạch.
Tăng huyết áp Goldblatt một thận. Khi một thận bị loại bỏ và một kẹp động mạch được đặt lên động mạch thận của thận còn lại, như được thể hiện trong Hình 14, tác động ngay lập tức làm áp suất bị giảm mạnh trong động mạch thận dưới mức kẹp, như được thể hiện bởi đường nét đứt trong hình. Sau đó, trong vòng vài giây hoặc vài phút, áp suất động mạch hệ thống bắt đầu tăng và tiếp tục tăng trong vòng vài ngày. Áp suất thường tăng một cách nhanh chóng trong giờ đầu hay lâu hơn và tác động này được theo sau bởi một sự tăng chậm hơn trong suốt vài ngày tiếp theo. Khi áp suất động mạch hệ thống đạt đến mức áp suất ổn định mới của nó thì áp suất động mạch thận xa vị trí kẹp (đường cong nét đứt trong hình) sẽ trở về gần như mức bình thường. Tăng huyết áp được tạo ra theo cách này được gọi là tăng huyết áp Goldblatt một thận (one-kidney Goldblatt hypertension) để vinh danh Harry Goldblatt, người đầu tiên nghiên cứu các đặc điểm định lượng quan trọng của tăng huyết áp gây ra bởi hẹp động mạch thận.
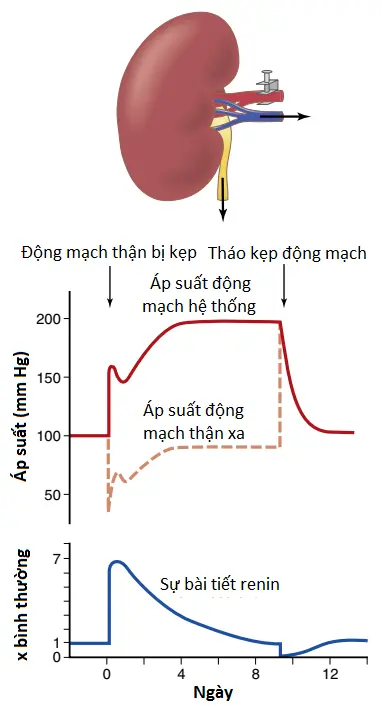
Sự tăng lên ban đầu trong áp suất động mạch trong tăng huyết áp Goldblatt được gây ra bởi cơ chế co mạch renin-angiotensin. Nghĩa là, do lưu lượng máu kém qua thận sau sự hẹp lại của động mạch thận nên các lượng lớn renin được bài tiết bởi thận, như được thể hiện bởi đường cong dưới cùng trong Hình 14 và hoạt động này làm tăng các mức angiotensin II và aldosterone trong máu. Angiotensin II cuối cùng sẽ nâng áp suất động mạch lên một cách nhanh chóng. Sự bài tiết của renin tăng lên đến đỉnh trong khoảng 1 hay 2 giờ nhưng trở về gần mức bình thường trong 5 đến 7 ngày bởi vì áp suất động mạch thận vào lúc đó cũng tăng trở lại mức bình thường, vì thế thận không còn thiếu máu nữa.
Sự tăng lên tiếp theo trong áp suất động mạch được gây ra bởi sự giữ lại muối và nước bởi thận bị kẹp động mạch, điều này cũng được kích thích bởi angiotensin II và aldosterone. Trong 5 đến 7 ngày, thể tích dịch cơ thể tăng đủ để nâng áp suất động mạch đến mức duy trì mới của nó. Giá trị định lượng của mức áp suất duy trì này được xác định bởi mức độ hẹp của động mạch thận. Nghĩa là, áp suất động mạch chủ phải tăng đủ để áp suất động mạch thận xa chỗ bị kẹp là đủ cao để tạo ra sự bài tiết nước tiểu bình thường.
Một tình huống tương tự xảy ra ở các bệnh nhân có hẹp động mạch thận của một thận đơn còn lại, như đôi khi xảy ra sau khi một người nhận một thận ghép. Ngoài ra, các sự tăng lên chức năng hay bệnh lý trong sức cản của các tiểu động mạch thận do xơ vữa động mạch hay các mức chất co mạch quá mức, có thể gây ra tăng huyết áp qua cùng các cơ chế với sự hẹp động mạch thận chính.
Tăng huyết áp Goldblatt hai thận (two-kidney Goldblatt hypertension). Tăng huyết áp cũng có thể xuất hiện khi động mạch đến chỉ một thận là bị hẹp lại trong khi động mạch đến thận còn lại là bình thường. Thận hẹp sẽ tiết renin và cũng giữ muối và nước do áp suất động mạch thận giảm trong thận này. Sau đó, thận “bình thường” bên đối diện giữ muối và nước do renin được sản xuất bởi thận thiếu máu. Renin này gây ra sự tăng hình thành của angiotensin II và aldosterone, cả hai chất này đều tuần hoàn đến thận đối diện và cũng làm cho nó giữ muối và nước. Vì thế, cả hai thận – nhưng vì các nguyên nhân khác nhau – trở thành các thành phần giữ muối và nước. Kết quả, tăng huyết áp phát triển.
Tương tự trên lâm sàng của tăng huyết áp Goldblatt hai thận xảy ra khi có một sự hẹp của một động mạch thận đơn – ví dụ, được gây ra bởi xơ vữa động mạch – ở một người mà có hai thận.
Tăng huyết áp gây ra bởi các thận mắc bệnh mà bài tiết renin dài hạn. Thông thường, các khu thay đổi màu sắc của một hoặc cả hai thận là các vùng mắc bệnh và trở nên thiếu máu bởi vì sự co mạch hay nhồi máu cục bộ, ngược lại các khu vực khác của thận là bình thường. Khi tình huống này xảy ra, hầu như các tác động tương tự sẽ xảy ra như trong tăng huyết áp Goldblatt loại hai thận. Nghĩa là, mô thận thiếu máu biến đổi màu sẽ tiết renin, điều này cuối cùng – bằng cách tác động thông qua sự hình thành của angiotensin II – làm cho khối thận còn lại cũng giữ muối và nước. Một trong các nguyên nhân thường gặp nhất của tăng huyết áp do thận, đặc biệt ở những người già, là bệnh thận thiếu máu biến đổi màu này.
Các loại tăng huyết áp khác được gây ra bởi các sự kết hợp của tải thể tích và sự co mạch:
Tăng huyết áp trong phần trên cơ thể được gây ra bởi hẹp eo động mạch chủ. Một trong mỗi vài nghìn đứa trẻ được sinh ra là mắc sự hẹp hay tắc bệnh lý của động mạch chủ ở một điểm qua các nhánh động mạch đến đầu và các tay của động mạch chủ nhưng gần hơn so với các động mạch thận, một tình trạng được gọi là hẹp eo động mạch chủ (coarctation of the aorta). Khi điều này xảy ra, lưu lượng máu đến phần dưới cơ thể được mang bởi nhiều động mạch bàng hệ nhỏ trong thành cơ thể với nhiều sức cản mạch máu giữa phần động mạch chủ bên trên và phần động mạch chủ bên dưới. Kết quả là áp suất động mạch trong phần trên của cơ thể có thể cao hơn 40% đến 50% so với trong phần dưới cơ thể.
Cơ chế của tăng huyết áp phần trên cơ thể này thì rất giống với tăng huyết áp Goldblatt một thận. Nghĩa là, khi một kẹp động mạch được đặt lên động mạch chủ phía trên các động mạch thận thì huyết áp trong cả hai thận sẽ giảm lúc đầu, renin được bài tiết, angiotensin và aldosterone được hình thành và tăng huyết áp xảy ra trong phần trên cơ thể. Áp suất động mạch trong phần dưới cơ thể ở mức các thận tăng gần đến mức bình thường, nhưng áp suất cao vẫn duy trì trong phần trên cơ thể. Các thận không còn thiếu máu nữa và vì thế sự bài tiết renin và sự hình thành của angiotensin và aldosterone trở về mức gần bình thường. Tương tự, trong hẹp eo động mạch chủ, áp suất động mạch trong phần dưới cơ thể thường gần như là bình thường, ngược lại, áp suất trong phần trên cơ thể thì cao hơn nhiều so với bình thường.
Vai trò của sự tự điều hòa trong tăng huyết áp được gây ra bởi hẹp eo động mạch chủ. Một đặc điểm đáng chú ý của tăng huyết áp gây ra bởi hẹp eo động mạch chủ đó là lưu lượng máu trong các cánh tay, nơi mà áp suất có thể cao hơn bình thường 40% đến 60%, thì gần như bằng với mức bình thường. Ngoài ra, lưu lượng máu trong các chân, nơi mà áp suất không tăng, thì cũng gần như bình thường. Làm thế nào điều này có thể xảy ra, với áp suất trong phần trên cơ thể cao hơn 40% đến 60% so với phần dưới cơ thể? Không có sự khác biệt trong các chất co mạch trong máu của phần trên và phần dưới cơ thể bởi vì cùng các dòng máu đến cả hai vùng. Tương tự, hệ thống thần kinh chi phối cả hai vùng của hệ thống tuần hoàn một cách tương tự nhau, vì thế, không có lý do gì để tin rằng có sự khác biệt trong sự kiểm soát thần kinh của các mạch máu. Nguyên nhân chính là do sự tự điều hòa (autoregulation) dài hạn phát triển gần như hoàn thiện đến nỗi các cơ chế kiểm soát lưu lượng máu cục bộ đền bù gần như 100% cho các sự khác biệt trong áp suất. Kết quả là trong cả hai vùng áp suất cao và áp suất thấp thì lưu lượng máu cục bộ được kiểm soát bởi các cơ chế tự điều hòa cục bộ gần như một cách chính xác theo các nhu cầu của mô và không theo mức áp suất.
Tăng huyết áp trong tiền sản giật (nhiễm độc huyết thai nghén). Một hội chứng được gọi là tiền sản giật (preeclampsia) (còn được gọi là nhiễm độc huyết thai nghén [toxemia of pregnancy]) phát triển ở khoảng 5% đến 10% những người phụ nữ mang thai. Một trong số các biểu hiện của tiền sản giật là tăng huyết áp mà thường mất đi sau khi sinh con. Mặc dù các nguyên nhân chính xác thì không hoàn toàn được hiểu nhưng thiếu máu nhau thai và sự giải phóng kế tiếp của các yếu tố gây độc bởi nhau thai được cho là đóng một vai trò trong việc gây ra nhiều biểu hiện của rối loạn này bao gồm tăng huyết áp ở người mẹ. Các chất được giải phóng bởi nhau thai thiếu máu cuối cùng sẽ gây rối loạn chức năng của các tế bào nội mô mạch máu trên khắp cơ thể, bao gồm cả các mạch máu của các thận. Rối loạn chức năng nội mô này làm giảm sự giải phóng nitric oxide và các chất giãn mạch khác, gây ra co mạch, giảm tốc độ lọc dịch từ cầu thận vào trong các ống thận, giảm lợi niệu natri áp suất (pressure natriuresis) của thận và phát triển tăng huyết áp.
Một bất thường bệnh lý khác mà có thể đóng góp vào tăng huyết áp trong tiền sản giật là sự dày lên của các màng cầu thận của thận (có lẽ là do quá trình tự miễn), điều này cũng làm giảm độ lọc dịch của cầu thận. Vì những lý do dễ hiểu, mức áp suất động mạch cần để tạo ra sự hình thành bình thường của nước tiểu trở nên tăng lên và mức áp suất động mạch dài hạn cũng trở nên tăng lên một cách tương ứng. Các bệnh nhân này đặc biệt dễ tăng thêm mức độ tăng huyết áp khi họ ăn vào lượng muối quá mức.
Tăng huyết áp do thần kinh (neurogenic hypertension). Tăng huyết áp do thần kinh cấp tính có thể được gây ra bởi sự kích thích hệ thống thần kinh giao cảm mạnh. Ví dụ, khi một người trở nên phấn khích vì bất kỳ lý do gì hay trong suốt các trạng thái lo âu, hệ thống giao cảm trở nên kích thích quá mức, co mạch ngoại vi xảy ra ở mọi nơi trong cơ thể và tăng huyết áp cấp tính xảy ra.
Một loại tăng huyết áp do thần kinh cấp tính khác xảy ra khi các dây thần kinh dẫn từ các baroreceptors bị cắt hoặc khi bó đơn độc (tractus solitarius) bị phá hủy ở mỗi bên của hành não. Đây là các khu vực nơi mà các dây thần kinh từ các baroreceptors của động mạch cảnh và động mạch chủ kết nối trong thân não. Sự ngừng đột ngột của các tín hiệu thần kinh bình thường từ các baroreceptors có cùng tác động lên các cơ chế kiểm soát áp suất thần kinh với một sự giảm đột ngột trong áp suất động mạch trong các động mạch cảnh và động mạch chủ. Nghĩa là, sự mất đi tác động ức chế bình thường lên trung tâm vận mạch gây ra bởi các tín hiệu thần kinh baroreceptor bình thường cho phép trung tâm vận mạch đột ngột trở nên cực kỳ hoạt hóa và áp suất động mạch trung bình tăng từ 100 mm Hg lên cao đến 160 mm Hg. Áp suất quay trở về mức gần bình thường trong vòng khoảng 2 ngày bởi vì đáp ứng của trung tâm vận mạch với tín hiệu baroreceptor vắng mặt sẽ biến mất dần, điều này được gọi là sự khôi phục trung ương của cơ chế kiểm soát áp suất áp suất baroreceptor. Vì thế, tăng huyết áp do thần kinh gây ra bởi sự cắt các dây thần kinh baroreceptor hầu như là một loại tăng huyết áp cấp tính, không phải là một loại tăng huyết áp mạn tính.
Hệ thống thần kinh giao cảm cũng đóng một vai trò quan trọng trong một số dạng tăng huyết áp mạn tính, một phần lớn là bởi sự hoạt hóa của các dây thần kinh giao cảm thận. Ví dụ, thừa cân và béo phì thường dẫn đến sự hoạt hóa của hệ thống thần kinh giao cảm mà cuối cùng sẽ kích thích các dây thần kinh giao cảm thận, làm giảm lợi niệu natri áp suất của thận và gây ra tăng huyết áp mạn tính. Các bất thường này đóng một vai trò quan trọng trong phần trăm lớn các bệnh nhân mắc tăng huyết áp nguyên phát (vô căn), sẽ được bàn luận đến trong phần sau của bài viết.
Các nguyên nhân di truyền của tăng huyết áp. Tăng huyết áp di truyền tự phát được quan sát thấy trong một vài giống động vật, bao gồm các giống chuột và thỏ khác nhau và ít nhất là một giống chó. Trong giống chuột mà được nghiên cứu rộng rãi nhất, chuột tăng huyết áp tự phát Okamoto, có bằng chứng cho thấy rằng trong sự phát triển ban đầu của tăng huyết áp, hệ thống thần kinh giao cảm thì hoạt hóa hơn đáng kể so với các con chuột bình thường. Trong các giai đoạn sau, các sự thay đổi cấu trúc được quan sát thấy trong các nephrons của thận: (1) tăng sức cản động mạch thận tiền cầu thận; và (2) giảm tính thấm của các màng cầu thận. Các sự thay đổi cấu trúc này cũng có thể đóng góp vào tính liên tục dài hạn của tăng huyết áp. Trong các giống chuột tăng huyết áp khác, suy giảm chức năng thận cũng được quan sát thấy.
Ở con người, một vài đột biến gene khác nhau đã được xác định là có thể gây ra tăng huyết áp. Các dạng tăng huyết áp này được gọi là tăng huyết áp đơn gene (monogenic hypertension) bởi vì chúng được gây ra bởi sự đột biến của một gen duy nhất. Một đặc điểm thú vị của các rối loạn di truyền này là tất cả chúng đều gây ra sự suy giảm chức năng thận, hoặc do sự tăng lên trong sức cản của các tiểu động mạch thận hoặc do sự tái hấp thu quá mức muối và nước bởi các ống thận. Trong một số trường hợp, sự tái hấp thu tăng lên là do các đột biến gene mà làm tăng một cách trực tiếp sự vận chuyển natri và chloride trong các tế bào biểu mô ống thận. Trong các trường hợp khác, các đột biến gene gây ra sự tăng tổng hợp hay tăng hoạt động của các hormones mà kích thích sự tái hấp thu muối và nước của ống thận. Vì thế, trong tất cả các rối loạn tăng huyết áp đơn gene đã được phát hiện, con đường chung cuối cùng mà dẫn đến tăng huyết áp là chức năng thận bị suy giảm. Tuy nhiên, tăng huyết áp đơn gene thì hiếm và tất cả các dạng đã biết chỉ chiếm dưới 1% các trường hợp tăng huyết áp ở người.
3. Tăng huyết áp nguyên phát (vô căn)
Khoảng 90% đến 95% tất cả những người mà có tăng huyết áp được cho là mắc tăng huyết áp nguyên phát (primary hypertension), còn được gọi là tăng huyết áp vô căn (essential hypertension) bởi nhiều bác sĩ lâm sàng. Các thuật ngữ này đơn giản có nghĩa là tăng huyết áp mà xuất phát từ nguồn gốc chưa biết, ngược lại với các dạng tăng huyết áp mà thứ phát từ các nguyên nhân đã biết, như hẹp động mạch thận hay các dạng tăng huyết áp đơn gene.
Trong hầu hết các bệnh nhân, thừa cân quá mức và một lối sống ít vận động đóng một vai trò quan trọng trong việc gây ra tăng huyết áp nguyên phát. Hầu hết các bệnh nhân mắc tăng huyết áp đều thừa cân và các nghiên cứu của các dân số khác nhau cho thấy rằng mỡ thừa có thể chiếm đến 65% đến 75% nguy cơ phát triển tăng huyết áp nguyên phát. Các nghiên cứu lâm sàng cho thấy một cách rõ ràng giá trị của giảm cân trong việc giảm huyết áp trong hầu hết các bệnh nhân mắc tăng huyết áp và các chỉ dẫn lâm sàng để điều trị tăng huyết áp khuyến cáo tăng hoạt động thể chất và giảm cân như là bước đầu tiên trong điều trị hầu hết các bệnh nhân tăng huyết áp.
Các đặc điểm sau đây của tăng huyết áp nguyên phát, trong số các đặc điểm khác, là được gây ra bởi thừa cân và béo phì:
1. Cung lượng tim được tăng lên một phần do cần thêm lưu lượng máu cho mô mỡ thừa. Tuy nhiên, lưu lượng máu trong tim, các thận, đường tiêu hóa và cơ xương cũng tăng cùng với thừa cân do sự tăng lên của tốc độ chuyển hóa và sự phát triển của các cơ quan và các mô trong đáp ứng với các nhu cầu chuyển hóa tăng lên của chúng. Khi tăng huyết áp được duy trì trong nhiều tháng và nhiều năm, tổng sức cản mạch máu ngoại vi có thể được tăng lên.
2. Hoạt động thần kinh giao cảm, đặc biệt là trong các thận, được tăng lên ở các bệnh nhân thừa cân. Các nguyên nhân tăng hoạt động giao cảm ở các cá nhân béo phì thì không hoàn toàn được hiểu nhưng các nghiên cứu đã cho thấy rằng các hormones như leptin mà được giải phóng từ các tế bào mỡ có thể kích thích một cách trực tiếp nhiều khu vực của vùng hạ đồi, điều này cuối cùng sẽ có một tác động kích thích lên các trung tâm vận mạch của hành não. Cũng có bằng chứng cho thấy giảm tính nhạy cảm của các baroreceptors động mạch trong việc đệm (buffering) cho các sự tăng lên trong áp suất động mạch, cũng như là sự hoạt hóa của các chemoreceptors (thụ cảm thể hóa học) ở những cá nhân béo phì, đặc biệt là ở những người mà cũng mắc ngưng thở khi ngủ do tắc nghẽn (obstructive sleep apnea).
3. Các mức angiotensin II và aldosterone được tăng lên trong nhiều bệnh nhân béo phì. Sự tăng này có thể được gây ra một phần bởi sự kích thích thần kinh giao cảm tăng lên, điều này làm tăng sự giải phóng renin bởi các thận và vì thế giúp cho sự hình thành của angiotensin II, điều mà cuối cùng sẽ kích thích tủy thượng thận bài tiết aldosterone.
4. Cơ chế lợi niệu natri áp suất của thận bị suy giảm và các thận sẽ không bài tiết đủ các lượng muối và nước trừ khi áp suất động mạch thì cao hay chức năng thận được cải thiện bằng một cách nào đó. Nếu như áp suất động mạch trung bình ở người tăng huyết áp vô căn là 150 mm Hg thì sự giảm nhanh của áp suất động mạch trung bình đến một giá trị bình thường là 100 mm Hg (nhưng không có sự thay đổi chức năng thận trừ việc áp suất giảm) sẽ gây ra gần như vô niệu hoàn toàn. Bệnh nhân sau đó sẽ giữ lại muối và nước cho đến khi áp suất quay trở lại mức tăng là 150 mm Hg. Tuy nhiên các sự giảm dài hạn trong áp suất động mạch bằng các liệu pháp chống tăng huyết áp hiệu quả thì thường sẽ không gây ra sự giữ lại muối và nước đáng kể bởi các thận bởi vì các liệu pháp này cũng cải thiện lợi niệu natri áp suất của thận, sẽ được bàn luận đến trong các bài viết sau này của mình nhé.
Các nghiên cứu thực nghiệm ở những động vật béo phì và những bệnh nhân béo phì cho thấy rằng suy giảm lợi niệu natri áp suất ở những người tăng huyết áp do béo phì được gây ra chủ yếu bởi sự tái hấp thu muối và nước của ống thận tăng lên do tăng hoạt động thần kinh giao cảm và tăng các mức angiotensin II và aldosterone. Tuy nhiên, nếu như tăng huyết áp không được điều trị một cách hiệu quả thì có thể cũng có tổn thương mạch máu trong các thận mà có thể làm giảm tốc độ lọc cầu thận và tăng mức độ nặng của tăng huyết áp. Cuối cùng, tăng huyết áp không kiểm soát liên quan với béo phì và các rối loạn chuyển hóa liên quan có thể dẫn đến tổn thương mạch máu nặng và mất hoàn toàn chức năng thận.
Phân tích đồ thị của sự kiểm soát áp suất động mạch trong tăng huyết áp vô căn. Hình 15 là một sự phân tích đồ thị của tăng huyết áp vô căn. Các đường cong của hình này được gọi là các đường cong chức năng thận tải natri (sodium-loading renal function curves) bởi vì áp suất động mạch trong mỗi trường hợp được tăng lên một cách rất chậm chạp, qua nhiều ngày hay nhiều tuần, bằng cách tăng dần dần mức natri ăn vào. Loại đường cong tải natri có thể được xác định bằng cách tăng mức natri ăn vào đến một mức mới mỗi vài ngày và sau đó đợi sự bài tiết natri của thận để đạt đến cân bằng với lượng natri ăn vào và cùng lúc đó, ghi lại các sự thay đổi trong áp suất động mạch.
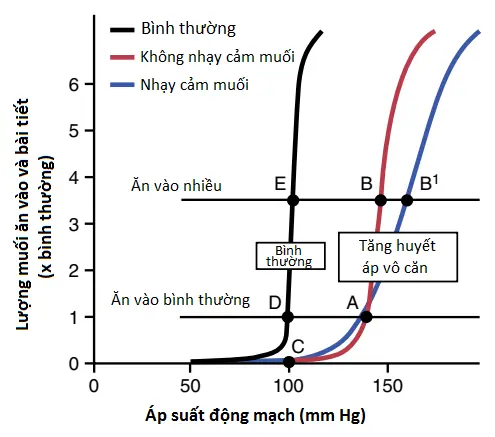
Khi quá trình này được sử dụng ở các bệnh nhân mắc tăng huyết áp vô căn thì 2 loại đường cong được thể hiện ở phía bên phải trong Hình 15 có thể được ghi lại; một đường cong được gọi là (1) tăng huyết áp không nhạy cảm với muối (salt-insensitive hypertension) và đường cong còn lại là (2) tăng huyết áp nhạy cảm với muối (salt-sensitive hypertension). Chú ý trong cả hai trường hợp, các đường cong được dịch chuyển sang bên phải đến một mức áp suất cao hơn so với những người có áp suất động mạch bình thường. Trong trường hợp của người mắc tăng huyết áp vô căn không nhạy cảm với muối thì áp suất động mạch không tăng đáng kể khi thay đổi từ một lượng muối ăn vào bình thường đến một lượng muối ăn vào cao hơn. Tuy nhiên, ở những bệnh nhân mà mắc tăng huyết áp vô căn nhạy cảm với muối thì lượng muối ăn vào cao sẽ tăng cường đáng kể tăng huyết áp.
Hai điểm nữa cần được nhấn manh. Đầu tiên, tính nhạy cảm với muối của huyết áp không phải là một phát hiện tất cả hoặc không có gì (all-or-none) – nó có tính định lượng, với một số người trở nên nhạy cảm với muối hơn so với các người khác. Thứ hai, tính nhạy cảm với muối của huyết áp thì không phải là một đặc điểm hằng định, thay vào đó, huyết áp thường trở nên nhạy cảm với muối hơn theo tuổi tác của một người, đặc biệt là sau các tuổi 50 hoặc 60, khi số lượng các đơn vị chức năng (nephrons) trong các thận bắt đầu giảm dần.
Nguyên nhân cho sự khác biệt giữa tăng huyết áp vô căn không nhạy cảm với muối và tăng huyết áp nhạy cảm với muối chủ yếu liên quan với các sự khác biệt về cấu trúc và chức năng trong các thận của hai loại bệnh nhân tăng huyết áp này. Ví dụ, tăng huyết áp nhạy cảm với muối có thể xảy ra với các loại bệnh thận mạn tính khác nhau bởi vì sự mất dần của các nephrons hay bởi vì sự lão hóa bình thường như được bàn đến trong các bài viết tiếp theo của mình. Chức năng bất thường của hệ thống renin-angiotensin cũng có thể làm cho áp suất động mạch trở nên nhạy cảm với muối, như đã nói đến trong các bài viết trước.
Điều trị tăng huyết áp vô căn. Như là một bước đầu tiên, chỉ dẫn lâm sàng hiện tại để điều trị tăng huyết áp khuyến cáo thay đổi lối sống nhắm mục đích tăng hoạt động thể chất và giảm cân ở hầu hết các bệnh nhân. Không may thay, nhiều bệnh nhân thì không thể giảm cân và sự điều trị thuốc bằng các thuốc chống tăng huyết áp phải được thực hiện. Hai loại thuốc phổ biến được sử dụng để điều trị tăng huyết áp: (1) các thuốc giãn mạch (vasodilator drugs), làm tăng lưu lượng máu thận và tốc độ lọc cầu thận và (2) các thuốc lợi niệu natri hoặc lợi niệu (natriuretic or diuretic drugs), giúp làm giảm sự tái hấp thu muối và nước của ống thận.
Các thuốc giãn mạch thường gây giãn mạch trong nhiều mô khác nhau của cơ thể cũng như là trong các thận. Các thuốc giãn mạch khác nhau sẽ tác động theo các cách sau: (1) bằng cách ức chế các tín hiệu thần kinh giao cảm đến các thận hoặc bằng cách chặn hoạt động của chất dẫn truyền giao cảm lên hệ thống mạch máu thận và các ống thận; (2) bằng cách giãn một cách trực tiếp cơ trơn của hệ thống mạch máu thận; hay (3) bằng cách chặn hoạt động của hệ thống renin-angiotensin-aldosterone lên hệ thống mạch máu thận hay các ống thận.
Các thuốc mà làm giảm sự tái hấp thu của muối và nước bởi các ống thận bao gồm cụ thể là các thuốc mà chặn sự vận chuyển chủ động của natri qua thành ống; sự chặn vận chuyển này cuối cùng sẽ ngăn cản sự tái hấp thu của nước như đã được giải thích trước đó trong loạt bài viết này. Các thuốc lợi niệu natri và lợi niệu sẽ được bàn luận chi tiết hơn trong các bài viết sau.
Tóm tắt các hệ thống đa năng tích hợp trong điều hòa áp suất động mạch
Rõ ràng rằng là áp suất động mạch được điều hòa không chỉ bởi một hệ thống kiểm soát áp suất đơn mà thay vào đó là bởi nhiều hệ thống có liên hệ với nhau, mỗi trong số đó thực hiện một chức năng chuyên biệt. Ví dụ, khi một người chảy máu quá nặng đến nỗi áp suất giảm xuống một cách đột ngột, có 2 vấn đề thách thức đối với hệ thống kiểm soát áp suất. Đầu tiên là sự sống sót; áp suất động mạch phải quay trở lại một mức áp suất cao một cách nhanh chóng sao cho người đó có thể sống sót qua cơn mất máu cấp tính. Thứ hai là sự trở về cuối cùng của thể tích máu và áp suất động mạch đến các mức bình thường của chúng để cho hệ thống tuần hoàn có thể tái thiết lập tính bình thường một cách hoàn toàn, không chỉ đơn thuần là cần để sống sót.
Trong các bài viết trước, chúng ta đã thấy rằng lớp phòng thủ đầu tiên chống lại các sự thay đổi nhanh trong áp suất động mạch là hệ thống kiểm soát thần kinh. Trong loạt bài viết này, chúng ta sẽ nhấn mạnh đến một lớp phòng thủ thứ hai, đạt được chủ yếu bởi các cơ chế của thận trong kiểm soát áp suất động mạch dài hạn. Tuy nhiên, có thêm các cơ chế mảnh ghép khác cho vấn đề này. Hình 16 giúp đặt các cơ chế mảnh ghép này lại cùng với nhau.
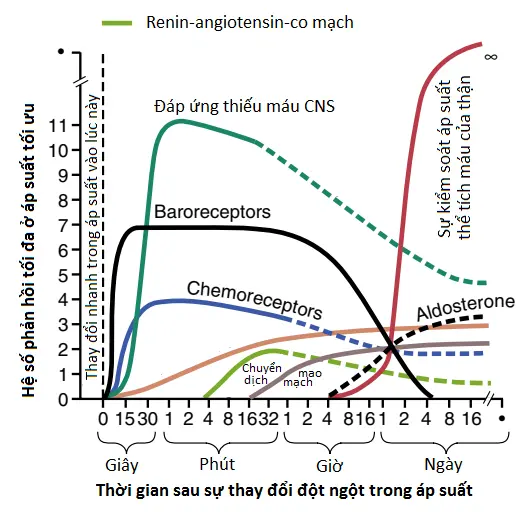
Hình 16 cho thấy các đáp ứng kiểm soát ngay lập tức (vài giây đến vài phút) và dài hạn (vài giờ đến vài ngày), trình bày dưới dạng các hệ số phản hồi (feedback gain), của 8 cơ chế kiểm soát áp suất động mạch. Các cơ chế này có thể được phân chia thành 3 nhóm: (1) các cơ chế phản hồi nhanh, trong vòng vài giây hay vài phút; (2) các cơ chế mà phản hồi trong một khoảng thời gian trung gian – nghĩa là, vài phút hay vài giờ; và (3) các cơ chế mà cung cấp sự kiểm soát áp suất động mạch dài hạn trong nhiều ngày, nhiều tháng và nhiều năm.
Các cơ chế kiểm soát áp suất động mạch mà tác động trong vòng vài giây hay vài phút. Các cơ chế kiểm soát áp suất tác động nhanh thì gần như hoàn toàn là các phản xạ thần kinh nhanh hay các đáp ứng của hệ thống thần kinh tự động khác. Chú ý trong Hình 16 có 3 cơ chế mà cho thấy các đáp ứng trong vòng vài giây: (1) cơ chế phản hồi baroreceptor; (2) cơ chế thiếu máu hệ thống thần kinh trung ương; và (3) cơ chế chemoreceptor. Các cơ chế này không chỉ bắt đầu phản ứng trong vòng vài giây mà chúng cũng rất mạnh mẽ. Sau bất cứ sự giảm xuống cấp trong áp suất, như được gây ra bởi mất máu nặng, các cơ chế thần kinh kết hợp lại để gây ra các tác động sau đây: (1) sự co các tĩnh mạch và sự chuyển máu vào trong tim; (2) tăng tần số tim và sức co cơ tim để cung cấp khả năng bơm máu lớn hơn bởi tim; và (3) sự co của hầu hết các tiểu động mạch ngoại vi. Tất cả các tác động này gần như xảy ra một cách tức thời để nâng áp suất động mạch quay trở lại vào trong khoảng sống sót.
Khi áp suất đột ngột tăng lên quá cao, như có thể xảy ra trong đáp ứng với sự truyền nhanh một lượng máu thêm thì cũng chính các cơ chế này vận hành theo hướng ngược lại, một lần nữa đưa áp suất quay trở về mức bình thường.
Các cơ chế kiểm soát áp suất động mạch mà tác động sau nhiều phút. Một vài cơ chế kiểm soát áp suất sẽ cho thấy các phản hồi đáng kể chỉ sau một vài phút sau một thay đổi áp suất động mạch nhanh. Ba trong số các cơ chế này, được thể hiện trong Hình 16, là như sau: (1) cơ chế co mạch renin-angiotensin; (2) sự giải tỏa sức căng của hệ thống mạch máu; và (3) sự dịch chuyển của dịch qua các thành mao mạch mô vào và ra khỏi hệ thống tuần hoàn để tái điều chỉnh thể tích máu khi cần.
Chúng ta đã mô tả sau cùng về vai trò của hệ thống co mạch renin-angiotensin trong việc cung cấp một phương tiện bán cấp để làm tăng áp suất động mạch khi cần thiết. Cơ chế giải tỏa sức căng (stress relaxation mechanism) được thể hiện bởi ví dụ sau đây. Khi áp suất trong các mạch máu trở nên quá cao, chúng trở nên giãn ra ngày càng nhiều trong vòng nhiều phút hoặc nhiều giờ; kết quả là áp suất trong các mạch máu giảm về giá trị bình thường. Sự giãn ra liên tục của các mạch máu được gọi là sự sự giải tỏa sức căng (stress relaxation), có thể đóng vai trò như là một “đệm” áp suất trung hạn.
Cơ chế dịch chuyển dịch mao mạch (capillary fluid shift mechanism) đơn giản có nghĩa là bất cứ khi nào áp suất mao mạch giảm xuống quá thấp, dịch được hấp thu từ các mô qua các màng mao mạch và vào trong hệ thống tuần hoàn, từ đó làm tăng thêm thể tích máu và tăng áp suất trong hệ thống tuần hoàn. Ngược lại, khi áp suất mao mạch tăng quá cao, dịch bị mất ra khỏi hệ thống tuần hoàn vào trong các mô, vì thế, làm giảm thể tích máu, cũng như là gần như tất cả các áp suất trên khắp hệ thống tuần hoàn.
Ba cơ chế trung gian này hầu như trở nên hoạt hóa trong vòng 30 phút đến vài giờ. Trong suốt thời gian này, các cơ chế thần kinh thường trở nên ngày càng ít hiệu quả, cho thấy tầm quan trọng của các phương thức kiểm soát áp suất trung hạn (intermediate-term pressure), không phải thần kinh này.
Các cơ chế điều hòa áp suất động mạch dài hạn. Mục tiêu của loạt bài viết này là giải thích vai trò của các thận trong sự kiểm soát áp suất động mạch dài hạn. Ở phía bên phải ngoài cùng của Hình 16 là cơ chế kiểm soát áp suất thể tích máu của thận, giống với cơ chế kiểm soát áp suất thận – dịch cơ thể, cho thấy rằng nó tốn một vài giờ để bắt đầu bắt đầu thực hiện đáp ứng đáng kể. Lúc này, nó sẽ phát triển một hệ số phản hồi kiểm soát áp suất động mạch mà gần như là vô cùng. Điều này có nghĩa là cơ chế này cuối cùng có thể đưa áp suất động mạch gần như hoàn toàn quay trở lại, mà không phải chỉ phần nào đó quay trở lại, mức áp suất mà cung cấp sự bài tiết muối và nước bình thường bởi các thận.
Nhiều yếu tố có thể ảnh hưởng đến mức điều hòa áp suất của cơ chế thận – dịch cơ thể. Một trong số này, được thể hiện trên Hình 16, là aldosterone. Một sự giảm trong áp suất động mạch dẫn đến một sự tăng lên trong sự bài tiết aldosterone trong vòng vài phút, qua vài giờ hoặc vài ngày tiếp theo, tác động này đóng một vai trò quan trọng trong việc điều chỉnh các đặc điểm kiểm soát áp suất của cơ chế thận – dịch cơ thể.
Đặc biệt quan trọng là sự tương tác của hệ thống renin-angiotensin với aldosterone và các cơ chế dịch của thận. Ví dụ, một lượng muối ăn vào của một người thay đổi nhiều từ ngày này đến ngày khác. Chúng ta đã thấy trong loạt bài viết này rằng là lượng muối ăn vào có thể giảm đến mức còn 1/10 so với bình thường hoặc có thể tăng đến 10 đến 15 lần so với bình thường và lúc này mức điều hòa của áp suất động mạch trung bình sẽ chỉ thay đổi một vài mm Hg nếu như hệ thống renin-angiotensin-aldosterone được vận hành một cách hoàn toàn. Tuy nhiên, nếu như không có một hệ thống renin-angiotensin-aldosterone thực hiện chức năng thì huyết áp sẽ trở nên rất nhạy cảm với các sự thay đổi trong lượng muối ăn vào.
Vì thế, sự kiểm soát áp suất động mạch bắt đầu với các phương thức cấp cứu của các sự kiểm soát áp suất thần kinh, sau đó tiếp tục với các đặc điểm duy trì của các sự kiểm soát áp suất trung gian và cuối cùng được ổn định ở mức áp suất dài hạn bởi cơ chế thận – dịch cơ thể. Cơ chế dài hạn này cuối cùng sẽ có nhiều sự tương tác với hệ thống renin-angiotensin-aldosterone, hệ thống thần kinh và một vài yếu tố khác mà cung cấp các khả năng kiểm soát huyết áp đặc biệt cho các mục đích chuyên biệt.
Cảm ơn các bạn đã theo dõi bài viết. Hẹn gặp lại các bạn trong các bài viết tiếp theo nhé !!!





































