Các cơ chế của sự kiểm soát lưu lượng máu
1. Sự kiểm soát nhanh của lưu lượng máu cục bộ
e. Sự kiểm soát lưu lượng máu mô: các yếu tố co và giãn mạch máu có nguồn gốc từ tế bào nội mô
Các tế bào nội mô lót các mạch máu tổng hợp một số chất mà khi giải phóng có thể tác động đến độ giãn hay co của thành mạch. Các vai trò sinh lý của nhiều yếu tố co hoặc giãn thành mạch có nguồn gốc từ tế bào nội mô này thì chỉ mới bắt đầu được hiểu.
Nitric oxide là một chất giãn mạch được giải phóng từ các tế bào nội mô khỏe mạnh. Quan trọng nhất trong các yếu tố giãn mạch có nguồn gốc từ tế bào nội mô là nitric oxide (NO), một khí ưa lipid được giải phóng từ các tế bào nội mô trong đáp ứng với nhiều kích thích hóa học và vật lý. Các enzyme nitric oxide synthase có nguồn gốc từ tế bào nội mô (eNOS) giúp tổng hợp NO từ arginine và oxygen và bằng sự khử nitrate vô cơ. Sau khi khuếch tán ra khỏi tế bào nội mô, NO có một thời gian bán hủy trong máu là chỉ khoảng 6 giây và đóng vai trò chủ yếu trong các mô cục bộ, nơi mà nó được giải phóng. NO hoạt hóa guanylate cyclase tan trong các tế bào cơ trơn mạch máu (Hình 1), tạo ra sự chuyển đổi guanosine triphosphate vòng (cGTP) thành guanosine monophosphate vòng (cGMP) và sự hoạt hóa protein kinase phụ thuộc cGMP, thành phần mà sẽ có một số tác động làm cho các mạch máu giãn ra.
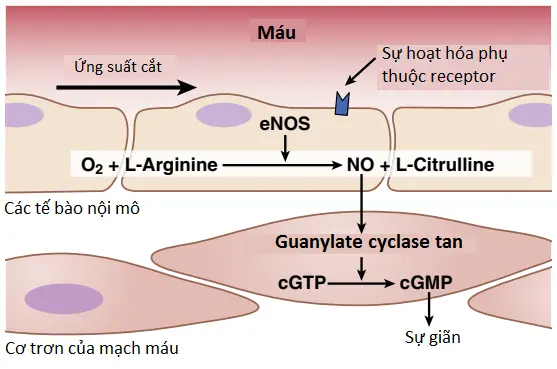
Lưu lượng máu qua các động mạch và các tiểu động mạch gây ra một ứng suất cắt (shear stress) trên các tế bào nội mô bởi lực kéo do độ nhớt của máu đối với thành mạch. Ứng suất cắt này làm biến dạng các tế bào nội mô theo hướng của dòng chảy và gây ra sự tăng lên đáng kể trong sự giải phóng NO. NO sau đó sẽ giúp làm giãn các mạch máu, may mắn thay, bởi vì các cơ chế chuyển hóa cục bộ trong kiểm soát lưu lượng máu mô chủ yếu làm giãn các động mạch rất nhỏ và các tiểu động mạch trong mỗi mô. Vì điều này, khi lưu lượng máu đi qua một phần vi mạch tăng lên thì điều này sẽ kích thích thứ phát sự giải phóng NO từ các mạch máu lớn hơn do sự tăng lên trong lưu lượng và ứng suất cắt trong các mạch máu này. NO giải phóng sẽ làm tăng đường kính của các mạch máu lớn hơn ở “thượng nguồn” (upstream) bất cứ khi nào mà lưu lượng máu vi mạch tăng ở “hạ nguồn” (downstream). Nếu không có một sự đáp ứng như vậy thì tính hiệu quả của sự kiểm soát lưu lượng máu cục bộ sẽ giảm bởi vì một phần sức cản đáng kể đối với dòng máu sẽ xuất hiện trong các động mạch nhỏ ở “thượng nguồn”.
Sự tổng hợp và giải phóng NO từ các tế bào nội mô thì cũng được kích thích bởi một số chất co mạch như angiotensin II, chất này kết hợp với các receptor đặc hiệu trên các tế bào nội mô. Sự tăng giải phóng NO giúp bảo vệ mạch máu khỏi sự co mạch quá mức.
Khi các tế bào nội mô bị phá hủy bởi tăng huyết áp mạn tính hay xơ vữa động mạch thì sự suy giảm tổng hợp NO có thể đóng góp vào sự co mạch quá mức và làm nặng thêm tình trạng tăng huyết áp và tổn thương nội mô. Nếu như không được điều trị, điều này cuối cùng có thể gây ra tổn thương mạch máu và phá hủy các mô dễ bị tổn thương như tim, thận và não.
Ngay cả trước khi NO được khám phá ra thì các bác sĩ lâm sàng cũng đã thường sử dụng nitroglycerin, amyl nitrate và các dẫn xuất nitrate khác để điều trị các bệnh nhân có cơn đau thắt ngực (angina pectoris) – nghĩa là, cơn đau ngực nặng gây ra bởi sự thiếu máu cơ tim. Các thuốc này, khi bị thoái hóa về mặt hóa học thì sẽ giải phóng NO và gây ra sự giãn các mạch máu trên khắp cơ thể, bao gồm cả các mạch máu vành.
Các ứng dụng quan trọng khác của NO trong sinh lý và dược lý là sự phát triển và sử dụng trên lâm sàng các thuốc (như sildenafil) giúp ức chế phosphodiesterase-5 đặc hiệu cGMP (PDE-5), một enzyme giúp thoái hóa cGMP. Bằng cách ngăn cản sự thoái hóa của cGMP, các chất ức chế PDE-5 sẽ kéo dài đáng kể hoạt động của NO để gây ra sự giãn mạch. Ứng dụng lâm sàng chủ yếu của các chất ức chế PDE-5 là điều trị rối loạn cương dương. Sự cương của dương vật được gây ra bởi các xung động của dây thần kinh giao cảm qua các dây thần kinh chậu đến dương vật, nơi mà các chất dẫn truyền thần kinh acetylcholine và NO được giải phóng. Bằng cách ngăn cản sự thoái hóa của NO, các chất ức chế PDE-5 làm tăng cường sự giãn của các mạch máu trong dương vật và giúp hỗ trợ trong sự cương dương, sẽ được bàn luận trong các bài viết tiếp theo của mình nhé.
Endothelin là một chất co mạch mạnh được giải phóng từ tế bào nội mô bị tổn thương. Các tế bào nội mô cũng sẽ giải phóng các chất co mạch . Quan trọng nhất trong số các chất này là endothelin, một peptide lớn gồm 27 amino acid mà chỉ cần một lượng nhỏ (tính bằng nanograms) để gây ra sự co mạch mạnh. Chất này xuất hiện trong các tế bào nội mô của tất cả hoặc hầu hết các mạch máu nhưng tăng nhiều khi các mạch máu bị tổn thương. Kích thích thông thường gây ra sự giải phóng chất này là tổn thương đối với các tế bào nội mô, như được gây ra bởi sự đè ép các mô hoặc sự tiêm một chất hóa học gây tổn thương vào trong mạch máu. Sau tổn thương mạch máu nặng, sự giải phóng endothelin cục bộ và sự co mạch kế tiếp giúp ngăn cản sự chảy máu diện rộng từ các động mạch có đường kính lớn khoảng 5 millimeters mà có thể có lỗ rách từ chấn thương do đè ép.
Tăng sự giải phóng endothelin thì cũng được cho là đóng góp vào sự co mạch khi mà tế bào nội mô bị tổn thương bởi tăng huyết áp. Các thuốc mà block các thụ cảm thể endothelin thì được sử dụng để điều trị tăng áp phổi (pulmonary hypertension) nhưng nhìn chung không được sử dụng để hạ huyết áp ở những bệnh nhân có tăng huyết áp động mạch hệ thống (systemic arterial hypertension).
2. Sự điều hòa lưu lượng máu dài hạn
Cho đến bây giờ thì hầu hết các cơ chế của sự điều hòa lưu lượng máu cục bộ mà chúng ta đã bàn thì sẽ được thực hiện vai trò trong vòng vài giây sau khi các điều kiện cục bộ của mô thay đổi. Tuy thế, ngay cả sự kích hoạt đầy đủ của các cơ chế nhanh này thì lưu lượng máu thường chỉ được điều chỉnh chỉ khoảng 3/4 lưu lượng máu được thêm vào của mô. Ví dụ, khi áp suất động mạch đột ngột tăng từ 100 đến 150 mm Hg thì lưu lượng máu tăng gần như ngay tức thời lên 100%. Sau đó, trong vòng 30 giây đến 2 phút, lưu lượng máu giảm quay trở về mức 10% đến 15% tăng hơn so với giá trị kiểm soát ban đầu. Ví dụ này cho thấy tính nhanh của các cơ chế điều hòa lưu lượng máu cục bộ nhanh nhưng vẫn cho thấy rằng sự điều hòa thì vẫn không hoàn toàn bởi vì một lưu lượng máu thêm 10% đến 15% vẫn ở trong một số mô.
Tuy nhiên, qua một khoảng thời gian vài giờ, vài ngày và vài tuần thì một loại điều hòa lưu lượng máu cục bộ dài hạn sẽ phát triển ngoài sự kiểm soát nhanh. Sự điều hòa dài hạn này sẽ thực hiện sự kiểm soát lưu lượng máu hoàn thiện hơn. Trong ví dụ đã đề cập trước đó, nếu như áp suất động mạch vẫn ở 150 mm Hg một cách không hạn định thì lưu lượng máu qua các mô sẽ dần dần tiệm cận đến mức gần như là bình thường trong vòng vài tuần. Hình 2 cho thấy (đường nét đứt màu xanh lá cây) tính cực kỳ hiệu quả của sự điều hòa lưu lượng máu cục bộ dài hạn này. Chú ý rằng một khi sự điều hòa dài hạn có thời gian để xảy ra thì các thay đổi dài hạn trong áp suất động mạch giữa 50 và 200 mm Hg sẽ có ít tác động lên lưu lượng máu cục bộ.

Sự điều hòa lưu lượng máu dài hạn thì đặc biệt quan trọng khi các nhu cầu chuyển hóa của một mô thay đổi. Vì thế, nếu như một mô trở nên hoạt động quá mức kéo dài và yêu cầu sự tăng lên trong lượng oxygen và các chất dinh dưỡng khác thì các tiểu động mạch và các mao mạch thường sẽ tăng cả số lượng và kích thước trong một vài tuần để đáp ứng với nhu cầu của mô trừ khi hệ thống tuần hoàn mắc bệnh lý hoặc quá già để đáp ứng với nhu cầu.
a. Sự điều hòa lưu lượng máu bằng các thay đổi trong hệ thống mạch máu của mô
Một cơ chế then chốt trong sự điều hòa lưu lượng máu cục bộ dài hạn là thay đổi số lượng mạch máu của mô. Ví dụ, nếu như sự chuyển hóa trong một mô tăng lên trong một khoảng thời gian dài thì mạch máu sẽ tăng lên, một quá trình được gọi là tân tạo mạch máu (angiogenesis), nếu như sự chuyển hóa giảm thì số lượng mạch máu sẽ giảm. Hình 3 cho thấy sự tăng lên nhiều của các mao mạch trong một cơ chày trước của chuột mà được kích thích điện để gây ra sự co cơ trong các khoảng thời gian ngắn trong vòng 30 ngày, so với cơ không được kích thích điện trong chân còn lại của chuột.
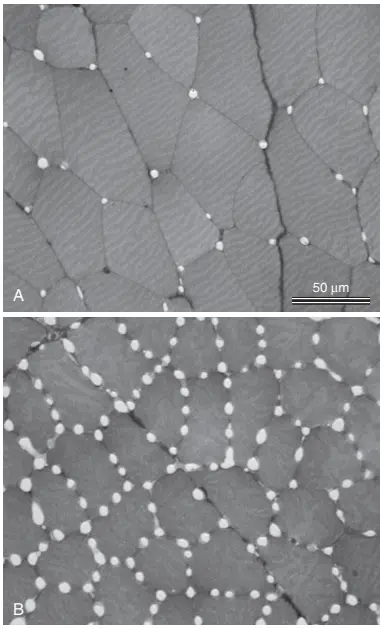
Vì thế, sự tái cấu trúc tự nhiên thực sự của hệ thống mạch máu mô xuất hiện để đáp ứng với các nhu cầu của các mô. Sự tái cấu trúc này xảy ra nhanh (trong vòng vài ngày) trong các động vật non. Nó cũng xảy ra nhanh trong mô mới phát triển như trong mô ung thư, nhưng xảy ra chậm hơn nhiều trong các mô già và tổ chức tốt. Vì thế, thời gian cần cho sự điều hòa dài hạn xảy ra có thể chỉ là vài ngày lúc mới sinh hoặc đến vài tháng ở những người già. Hơn thế nữa, mức độ đáp ứng cuối cùng thì tốt hơn nhiều ở những mô trẻ hơn so với các mô già; vì thế, ở trẻ sơ sinh, số lượng mạch máu sẽ điều chỉnh để đáp ứng gần như chính xác với nhu cầu của mô đối với lưu lượng máu, ngược lại ở những mô già hơn, số lượng mạch máu thường ít hơn nhiều so với nhu cầu của các mô.
Vai trò của oxygen trong sự điều hòa dài hạn. Oxygen thì quan trọng không chỉ cho sự kiểm soát nhanh lưu lượng máu cục bộ mà còn trong sự kiểm soát dài hạn lưu lượng máu cục bộ. Một ví dụ của điều này là sự tăng số lượng mạch máu trong các mô động vật mà sống ở các độ cao cao so với mực nước biển, nơi mà oxygen trong khí quyển thấp. Ở các đứa trẻ sinh non được đưa vào trong lều oxygen vì mục đích điều trị thì lượng oxygen thừa sẽ gây ra sự ngừng gần như ngay lập tức của sự phát triển mạch máu mới trong giác mạc của mắt đứa trẻ sinh non và thậm chí có thể gây ra sự thoái hóa của một số mạch máu nhỏ mà đã được hình thành. Khi đứa trẻ được đưa ra khỏi lều oxygen thì sự phát triển quá mức các mạch máu mới xảy ra để đáp ứng sự giảm đột ngột trong nhu cầu oxygen. Thông thường, sự phát triển quá mức xảy ra trong các mạch máu võng mạc sẽ phát triển ra ngoài võng mạc vào trong dịch thủy tinh, cuối cùng gây ra mù lòa, một tình trạng được gọi là “chứng tạo mô xơ sau thủy tinh thể” (retrolental fibroplasia).
Tầm quan trọng của các yếu tố tăng trưởng mạch máu trong sự hình thành các mạch máu lớn. Mười hai yếu tố hoặc nhiều hơn mà giúp làm tăng sự phát triển của các mạch máu mới đã được tìm thấy, gần như tất cả chúng là các peptide nhỏ. Bốn yếu tố mà được chỉ rõ đặc điểm là yếu tố tăng trưởng nội mạc mạch máu (vascular endothelial growth factor – VEGF), yếu tố tăng trưởng nguyên bào sợi (fibroblast growth factor), yếu tố tăng trưởng có nguồn gốc tiểu cầu (platelet-derived growth factor – PDGF) và angiogenin, mỗi trong số chúng được tách ra từ các mô mà có sự cung cấp oxygen không đầy đủ. Sự suy giảm oxygen mô sẽ làm thúc đẩy sự biểu hiện của các yếu tố cảm ứng khi hạ oxygen mô (hypoxia inducible factors – HIFs), các yếu tố phiên mã mà cuối cùng sẽ làm tăng điều hòa sự biểu hiện gene và sự hình thành các yếu tố tăng trưởng mạch máu (còn được gọi là các yếu tố tân tạo mạch máu).
Sự tân tạo mạch máu bắt đầu bằng các mạch máu mới mọc ra từ các mạch máu nhỏ khác. Bước đầu tiên là sự tiêu đi của màng đáy của tế bào nội mô tại điểm mọc của mạch máu. Bước này được theo sau bởi sự sản sinh nhanh các tế bào nội mô mới, sự sản sinh này sẽ đi ra phía ngoài qua thành mạch máu dưới dạng các dây mở rộng, hướng về phía nguồn của yếu tố tân tạo mạch máu. Các tế bào trong mỗi dây tiếp tục phân chia và gấp lên nhau một cách nhanh chóng để hình thành nên một ống. Tiếp theo, ống kết nối với một ống khác mọc ra từ một mạch nguồn khác (một tiểu động mạch hoặc tiểu tĩnh mạch) và hình thành nên một vòng mao mạch mà qua đó máu sẽ bắt đầu chảy. Nếu như dòng chảy đủ lớn thì các tế bào cơ trơn cuối cùng sẽ xâm lấn vào thành mạch, vì thế, một số mạch máu mới cuối cùng sẽ phát triển thành các tiêu động mạch hoặc các tiểu tĩnh mạch mới hoặc thậm chí là các mạch máu lớn hơn. Vì thế, sự tân tạo mạch máu giải thích việc làm thế nào mà các yếu tố chuyển hóa trong các mô cục bộ có thể gây ra sự phát triển của các mạch máu mới.
Một số chất nhất định khác như một số hormone steroid có tác động đối nghịch trên các mạch máu nhỏ, thậm chí đôi khi gây ra sự phân giải các tế bào mạch máu và sự biến mất của các mạch máu. Vì thế, các mạch máu cũng có thể bị làm cho biến mất khi chúng không được cần đến. Các peptide sản xuất trong các mô cũng có thể ngăn chặn sự phát triển của các mạch máu mới. Ví dụ, angiostatin, một phần của protein plasminogen, là một chất ức chế sự tân tạo mạch máu xuất hiện tự nhiên. Endostatin là một peptide chống tân tạo mạch máu khác có nguồn gốc từ sự thoái hóa của collagen type XVII. Mặc dù các chức năng sinh lý chính xác của các chất chống tân tạo mạch này thì vẫn chưa được biết đến nhưng có một điều rất thú vị trong công dụng tiềm năng của chúng là ngừng sự phát triển của mạch máu trong các khối ung thư và vì thế ngăn cản sự tăng lên mạnh trong lưu lượng máu cần để duy trì sự cung cấp dinh dưỡng cho các khối u đang phát triển nhanh.
Số lượng mạch máu được xác định bởi nhu cầu lưu lượng máu tối đa không phải bởi nhu cầu trung bình. Một đặc điểm đặc biệt có giá trị của sự kiểm soát mạch máu dài hạn là số lượng mạch máu được xác định chủ yếu bởi mức lưu lượng máu cần cho mô tối đa chứ không phải là nhu cầu trung bình. Ví dụ, trong suốt quá trình hoạt động mạnh, nhu cầu đối với lưu lượng máu cho toàn bộ cơ thể thường tăng từ 6 đến 8 lần so với lưu lượng máu khi nghỉ. Sự thừa quá nhiều lưu lượng máu này thì có thể không cần đến nhiều hơn vài phút mỗi ngày. Bất kể là thế nào đi nữa, ngay cả với khoảng thời gian nhu cầu ngắn này cũng có thể tạo ra đủ yếu tố tân tạo mạch máu bởi các cơ để tăng số lượng mạch máu cần thiết. Nếu như không có khả năng này thì mỗi lần một người cố gắng thực hiện hoạt động thể lực mạnh thì các cơ sẽ không thể nhận đủ các chất dinh dưỡng cần thiết, đặc biệt là oxygen và vì thế các cơ sẽ không thể co.
Tuy nhiên, sau khi một số lượng mạch máu thêm phát triển thì các mạch máu đã phát triển thêm bình thường sẽ vẫn co mạch, sự mở ra cho các lưu lượng máu thêm vào chỉ xuất hiện khi có sự kích thích cục bộ thích hợp như thiếu oxygen, các kích thích giãn mạch thần kinh hay các kích thích khác tạo ra các lưu lượng máu bổ sung cần thiết.
b. Sự điều hòa lưu lượng máu bởi sự phát triển của tuần hoàn bàng hệ
Trong hầu hết các mô của cơ thể, khi một động mạch hoặc một tĩnh mạch bị tắc lại thì một kênh mạch mới thường sẽ phát triển quanh chỗ tắc và cho phép ít nhất một phần sự tái cung cấp máu đến mô bị ảnh hưởng. Giai đoạn đầu tiên trong quá trình này là sự giãn của các vòng mao mạch nhỏ mà kết nối mạch máu ở phía trên của chỗ tắc mạch với mạch máu bên dưới. Sự giãn ra này xuất hiện trong vòng trong một hoặc hai phút đầu tiên, cho thấy rằng sự giãn dường như được điều hòa bởi các yếu tố chuyển hóa. Sau sự mở ban đầu này của các mạch máu bàng hệ thì lưu lượng máu thường vẫn ít hơn 25% so với nhu cầu cấp máu cho mô. Tuy nhiên, sự mở nhiều hơn nữa xảy ra trong nhiều giờ sau đó để sao cho trong vòng một ngày một nửa nhu cầu của mô phải được đáp ứng và trong vòng một vài ngày, lưu lượng máu thường là sẽ đủ để đáp ứng các nhu cầu của mô.
Các mạch máu bàng hệ tiếp tục phát triển trong nhiều tháng sau đó, thường hình thành nhiều kênh bàng hệ nhỏ chứ không phải là một kênh bàng hệ lớn. Dưới các điều kiện nghỉ ngơi, lưu lượng máu có thể trở về mức gần như bình thường, nhưng các kênh mới hiếm khi trở nên đủ lớn để cung cấp lưu lượng máu cần cho suốt quá trình hoạt động mạnh của mô. Vì thế, sự phát triển của các mạch máu bàng hệ tuân theo các sự nguyên lý thông thường của sự kiểm soát lưu lượng máu nhanh và dài hạn; sự kiểm soát nhanh là sự giãn nhanh do chuyển hóa, theo sau lâu dài bởi sự tăng trưởng và mở rộng của các mạch máu mới trong một khoảng thời gian nhiều tuần và nhiều tháng.
Một ví dụ quan trọng là sự phát triển của mạch máu bàng hệ xuất hiện sau huyết khối của một trong các động mạch vành. Ở những năm của tuổi 60, nhiều người trải qua sự đóng kín hoặc tắc một phần ở ít nhất một trong các nhánh của mạch máu vành nhưng họ thì không nhận thức được điều này bởi vì các mạch máu bàng hệ phát triển một cách nhanh chóng đủ đề ngăn chặn tổn thương cơ tim. Khi các mạch máu bàng hệ không thể phát triển một cách nhanh chóng để duy trì lưu lượng máu do sự nhanh hay mức độ nghiêm trọng của thiểu năng mạch vành thì các cơn đau tim nặng có thể xảy ra.
c. Sự tổ chức lại mạch máu trong đáp ứng với các sự thay đổi kéo dài trong lưu lượng máu hay áp suất máu
Sự tăng trưởng và tái tổ chức mạch máu là các vấn đề quan trọng của sự phát triển và tăng trưởng của mô và xảy ra như là một đáp ứng thích nghi với các sự thay đổi dài hạn trong huyết áp hay lưu lượng máu. Ví dụ, sau vài tháng rèn luyện thể thao thì số lượng mạch máu của các cơ được rèn luyện sẽ tăng lên để đáp ứng với nhu cầu lưu lượng máu cao hơn. Ngoài các sự thay đổi trong mật độ mao mạch thì cũng có các thay đổi trong cấu trúc của các mạch máu lớn để đáp ứng với các sự thay đổi dài hạn trong huyết áp và lưu lượng máu. Khi huyết áp tăng lên kéo dài trên mức bình thường, ví dụ, các động mạch lớn và nhỏ và các tiểu động mạch tái tổ chức để đáp ứng với sự tăng trong áp lực cơ học lên thành của huyết áp máu cao hơn. Trong hầu hết các mô, các động mạch nhỏ và các tiểu động mạch đáp ứng một cách nhanh chóng (trong vòng vài giây) với sự tăng lên của áp suất động mạch bằng sự co mạch, điều này giúp tự điều hòa lưu lượng máu mô, như đã được bàn luận trước đây nhé. Sự co mạch làm giảm đường kính lòng mạch, điều này cuối cùng sẽ có xu hướng làm bình thường hóa sức căng thành mạch (T), một yếu tố mà theo như phương trình Laplace là tích của bán kính mạch máu (r) và áp suất của nó (P): T = r x P.
Trong các mạch máu nhỏ mà co đáp ứng với sự tăng lên của huyết áp thì các tế bào cơ trơn và các tế bào nội mô sẽ dần dần – trong một khoảng thời gian vài ngày hoặc vài tuần – sắp xếp lại quanh đường kính lòng mạch nhỏ hơn, được gọi là sự tái tổ chức vào bên trong (inward eutrophic remodeling), mà không có sự thay đổi nào trong tổng tiết diện cắt ngang của mạch máu (Hình 4). Trong các động mạch lớn hơn mà không có sự co trong đáp ứng với sự tăng lên trong áp suất thì thành mạch sẽ rơi vào trạng thái tăng sức căng và kích thích một sự đáp ứng tái tổ chức kiểu phì đại (hypertrophic remodeling) và một sự tăng lên trong tiết diện cắt ngang của mạch máu. Đáp ứng phì đại làm tăng kích thước của các tế bào cơ trơn mạch máu và kích thích sự hình thành thêm các protein chất nền ngoại bào như collagen và fibronectin, các protein này giúp tăng cường sức mạnh thành mạch để đứng vững trước các huyết áp cao. Tuy nhiên, đáp ứng phì đại này cũng làm cho các mạch máu lớn cứng hơn, là một dấu hiệu của tăng huyết áp mạn tính.
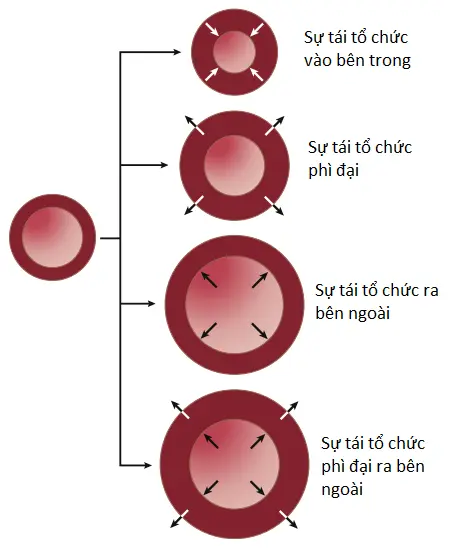
Một ví dụ khác của sự tái tổ chức mạch máu là sự thay đổi mà xảy ra khi một tĩnh mạch lớn (thường là tĩnh mạch hiển) được cấy vào trong một bệnh nhân cần thực hiện thủ thuật bắt cầu nối mạch vành. Các tĩnh mạch thường được tiếp xúc với các áp suất thấp hơn nhiều so với các động mạch và có các thành mỏng hơn nhiều, nhưng khi một tĩnh mạch được khâu vào động mạch chủ và kết nối với một động mạch vành thì nó được tiếp xúc với áp suất trong lòng mạch tăng lên và sức căng thành mạch tăng lên. Sự tăng lên trong sức căng thành mạch sẽ khởi động sự phì đại của các tế bào cơ trơn mạch máu và sự tăng hình thành chất nền ngoại bào, điều này sẽ làm dày và làm khỏe thành tĩnh mạch; kết quả, một vài tháng sau khi cấy vào trong hệ thống động mạch, tĩnh mạch thường sẽ có một sự dày thành tương tự với của một động mạch.
Sự tái tổ chức của mạch máu cũng xảy ra khi một mạch máu tiếp xúc lâu dài với sự tăng hay giảm của lưu lượng máu. Sự tạo thành một thông nối giúp kết nối một động mạch lớn với một tĩnh mạch lớn, bằng cách đó hoàn toàn bỏ qua các mạch máu nhỏ và các mao mạch có sức cản lớn, sẽ cung cấp một ví dụ đặc biệt thú vị về sự tái tổ chức trong động mạch và tĩnh mạch ảnh hưởng. Ở những bệnh nhân bị suy thận mà phải trải qua sự thẩm phân máu, một sự thông nối động-tĩnh mạch từ động mạch quay đến tĩnh mạch trước khuỷu của cánh tay được tạo ra, cho phép sự đi vào mạch máu để thực hiện thẩm phân. Tốc độ dòng máu trong động mạch quay có thể tăng lên 10 đến 50 lần so với tốc độ dòng máu bình thường, phụ thuộc vào sự thông thoáng của nối thông động-tĩnh mạch. Do tốc độ dòng máu cao và ứng suất cắt cao trên thành mạch nên đường kính lòng động mạch quay sẽ tăng dần (sự tái tổ chức ra bên ngoài (outward remodeling)), ngược lại thì độ dày thành mạch có thể vẫn không thay đổi, làm tăng tiết diện cắt ngang của mạch máu. Ngược lại, độ dày thành mạch, đường kính lòng mạch và tiết diện cắt ngang của mạch máu ở phía tĩnh mạch của thông nối sẽ tăng trong đáp ứng với sự tăng lên trong áp suất và lưu lượng máu (tái tổ chức kiểu phì đại ra bên ngoài (outward hypertrophic remodeling)). Kiểu tái tổ chức mạch máu này thì phù hợp với tiểu chuẩn về sự tăng lên dài hạn trong sức căng thành mạch sẽ làm phì đại và tăng độ dày thành mạch trong các mạch máu lớn, ngược lại, tăng tốc độ dòng máu và ứng suất cắt gây ra sự tái tổ chức ra bên ngoài và tăng đường kính lòng mạch để đáp ứng với sự tăng lên trong lưu lượng máu.
Sự giảm kéo dài của huyết áp và lưu lượng máu có các tác động trái ngược với những gì mà chúng ta đã mô tả trước đó. Khi lưu lượng máu bị giảm nhiều, đường kính của lòng mạch cũng bị giảm và khi huyết áp bị giảm thì độ dày của thành mạch cũng thường giảm. Vì thế, sự tái tổ chức của mạch máu là một đáp ứng thích nghi quan trọng đối với sự tăng trưởng và phát triển của mô cũng như là đối với các thay đổi sinh lý và bệnh lý quan trong trong huyết áp và lưu lượng máu đến các mô.
Sự kiểm soát dịch thể của hệ thống tuần hoàn
Sự kiểm soát dịch thể của hệ thống tuần hoàn có nghĩa là sự kiểm soát bởi các chất được tiết ra hay được hấp thu vào trong dịch cơ thể, như các hormones và các yếu tố được sản xuất cục bộ. Một số trong các chất này được hình thành bởi các tuyến chuyên biệt và được vận chuyển trong máu đi khắp toàn bộ cơ thể. Các chất khác được hình thành trong các mô cục bộ và chỉ gây ra các tác động tuần hoàn cục bộ. Các yếu tố dịch thể quan trọng nhất ảnh hưởng đến chức năng tuần hoàn sẽ được mô tả ngay bên dưới đây.
1. Các chất gây co mạch
Norepinephrine và epinephrine. Norepinephrine là một hormone gây co mạch cực kỳ mạnh, epinephrine là một chất gây co mạch ít mạnh hơn và trong một số mô, thậm chí nó còn gây ra sự giãn mạch nhẹ. (Một ví dụ đặc biệt về sự giãn mạch được gây ra bởi epinephrine là khi nó làm giãn mạch các động mạch vành trong suốt quá trình tăng hoạt động của tim).
Khi hệ thống thần kinh giao cảm được kích thích trong hầu hết các phần của cơ thể trong suốt quá trình căng thẳng hoặc hoạt động mạnh thì các đầu tận thần kinh giao cảm trong các mô riêng biệt giải phóng norepinephrine, chất này sẽ kích thích tim và co các tĩnh mạch và các tiểu động mạch. Ngoài ra, các dây thần kinh giao cảm đến tủy thượng thận sẽ làm cho các tuyến này tiết norepinephrine và epinephrine vào trong máu. Các hormone này sau đó tuần hoàn đến tất cả các khu vực trong cơ thể và gây ra các tác động trên hệ thống tuần hoàn gần như giống với sự kích thích giao cảm trực tiếp, vì thế, giúp cung cấp một hệ thống kiểm soát kép: (1) sự kích thích thần kinh trực tiếp; và (2) các tác động gián tiếp của norepinephrine và/hoặc epinephrine trong máu tuần hoàn.
Angiotensin II. Angiotensin II là một chất co mạch mạnh mẽ khác. Chỉ cần khoảng một phần triệu của một gram đã có thể tăng huyết áp của một người lên 50 mm Hg hoặc cao hơn.
Tác động của angiotensin II là co các tiểu động mạch nhỏ một cách mạnh mẽ. Nếu như sự co này xuất hiện trong một khu vực mô cục bộ thì lưu lượng máu đến khu vực đó có thể suy giảm nghiêm trọng. Tuy nhiên, tầm quan trọng thực sự của angiotensin II đó là bình thường nó có thể tác động lên nhiều tiểu động mạch của cơ thể cùng lúc để làm tăng tổng sức cản ngoại vi và làm giảm sự bài tiết natri và nước bởi các thận, bằng cách đó, làm tăng áp suất động mạch. Vì thế, hormone này đóng một vai trò không thể thiếu trong sự điều hòa áp suất động mạch, sẽ được nói đến trong các bài viết sau của mình nhé.
Vasopressin. Vasopressin còn được gọi là hormone chống bài niệu (antidiuretic hormone), thậm chí còn mạnh hơn angiotensin II ở khả năng gây co mạch, vì thế, làm cho nó trở thành một trong số các chất gây co mạch mạnh nhất cơ thể. Nó được hình thành trong các tế bào thần kinh ở vùng dưới đồi của não (xem các bài viết sau của mình nhé) nhưng sau đó được vận chuyển xuống dưới bởi các sợi trục thần kinh đến tuyến thùy sau tuyến yên, nơi mà nó cuối cùng sẽ được tiết vào trong máu.
Rõ ràng rằng là vasopressin có thể có các tác động to lớn lên chức năng tuần hoàn. Tuy nhiên, bởi vì chỉ các lượng nhỏ vasopressin được tiết trong hầu hết các điều kiện sinh lý nên hầu hết các nhà sinh lý học nghĩ rằng vasopressin đóng vai trò nhỏ trong sự kiểm soát mạch máu. Tuy nhiên, các thực nghiệm đã cho thấy rằng nồng độ vasopressin trong máu tuần hoàn sau mất máu nặng có thể tăng đủ lớn để giảm đi sự suy giảm trong huyết áp một cách đáng kể. Trong một số trường hợp, chính hoạt động này có thể đưa áp suất động mạch gần như quay trở về bình thường.
Vasopressin có chức năng chính trong việc tăng đáng kể khả năng tái hấp thu nước từ các ống thận quay trở về trong máu (sẽ được nói đến trong các bài viết sau) và vì thế giúp kiểm soát thể tích dịch cơ thể. Đó là lý do tại sao hormone này còn được gọi là hormone chống bài niệu.
2. Các chất giãn mạch
Bradykinin. Vài chất được gọi là các kinins gây ra sự giãn mạch mạnh khi được hình thành trong máu và trong dịch mô của một số cơ quan. Các kinins là các polypeptides nhỏ mà được tách ra bởi các enzyme phân giải protein từ α2-globulin trong huyết tương hay dịch mô. Một enzyme phân giải protein đặc biệt quan trọng cho mục đích này là kallikrein, xuất hiện trong máu và dịch mô ở dạng bất hoạt. Kallikrein bất hoạt này được hoạt hóa bởi sự phân hủy của máu, sự viêm của mô hoặc các tác động vật lý và hóa học khác lên máu và các mô. Khi kallikrein trở nên hoạt hóa, nó tác động ngay lập tức lên α2-globulin để giải phóng một kinin được gọi là kallidin, chất mà sau đó được chuyển bởi các enzyme mô thành bradykinin. Một khi được hình thành, bradykinin sẽ chỉ tồn tại trong khoảng vài phút bởi vì nó bị bất hoạt bởi enzyme carboxypeptidase hoặc bởi enzyme chuyển (converting enzyme), enzyme chuyển này cũng đóng một vai trò quan trọng trong hoạt hóa angiotensin, sẽ được bàn luận đến trong các bài viết tiếp theo của mình nhé. Enzyme kallikrein hoạt hóa bị phá hủy bởi một chất ức chế kallikrein mà cũng xuất hiện trong các dịch cơ thể.
Bradykinin gây ra cả tác động giãn mạch mạnh và tăng tính thấm mao mạch. Ví dụ, tiêm 1 microgram bradykinin vào trong động mạch cánh tay của một người sẽ làm tăng lưu lượng máu qua cánh tay đến 6 lần và thậm chí các liều lượng tiêm nhỏ hơn được tiêm cục bộ vào trong các mô có thể gây ra sự phù cục bộ rõ rệt do tăng kích thước lỗ mao mạch.
Các kinins đóng các vai trò đặc biệt quan trọng trong điều hòa lưu lượng máu và sự thoát dịch của mao mạch trong các mô viêm. Người ta cũng cho là bradykinin đóng một vai trò bình thường để giúp điều hòa lưu lượng máu trong da cũng như là trong các tuyến nước bọt và tiêu hóa.
Histamine. Histamine được giải phóng trong hầu hết mọi mô cơ thể nếu như mô trở nên tổn thương hoặc viêm hoặc là mục tiêu của một phản ứng dị ứng. Hầu hết histamine có nguồn gốc từ dưỡng bào (mast cells) trong các mô tổn thương và từ các bạch cầu ưa base (basophils) trong máu.
Histamine có một tác động giãn mạch mạnh lên các tiểu động mạch và giống như bradykinin, nó có khả năng tăng tình trạng xuất hiện lỗ của mao mạch một cách đáng kể, cho phép sự thoát dịch và protein huyết tương vào trong các mô. Trong nhiều điều kiện bệnh lý, sự giãn các tiểu động mạch mạnh và sự tăng tình trạng xuất hiện lỗ của mao mạch do histamine sẽ làm cho các lượng lớn dịch thoát khỏi hệ thống tuần hoàn để vào trong các mô, gây ra phù. Sự giãn mạch cục bộ và các tác động gây ra phù của histamine thì đặc biệt nổi bật trong suốt các phản ứng dị ứng và sẽ được nói đến trong các bài viết tiếp theo của mình nhé.
3. Sự kiểm soát mạch máu bởi các ion và các yếu tố hóa học khác
Nhiều ion khác nhau và các yếu tố hóa học khác có thể làm giãn hoặc co các mạch máu cục bộ. Danh sách sau đây sẽ nói chi tiết về một số tác động đặc hiệu của chúng:
1. Một sự tăng lên trong nồng độ ion canxi nội bào sẽ làm co mạch bởi vì tác động tổng quan của ion canxi là kích thích sự co cơ trơn, sẽ được nói đến trong các bài viết sau của mình nhé.
2. Một sự tăng lên trong nồng độ ion kali, trong khoảng sinh lý, sẽ gây ra sự giãn mạch. Tác động này là do khả năng của ion kali ức chế sự co cơ trơn.
3. Một sự tăng trong nồng độ ion magie sẽ gây ra sự giãn mạch mạnh bởi vì ion magie ức chế sự co cơ trơn.
4. Một sự tăng trong nồng độ ion hydrogen (sự giảm pH) sẽ làm giãn các tiểu động mạch. Ngược lại, một sự giảm nhẹ trong nồng độ ion hydrogen sẽ làm co tiểu động mạch.
5. Các anions mà có các tác động đáng kể lên các mạch máu là acetate và citrate, cả 2 ion này đều gây ra sự giãn mạch ở mức độ nhẹ.
6. Sự tăng lên trong nồng độ carbon dioxide sẽ gây ra sự giãn mạch trung bình trong hầu hết các mô nhưng sẽ gây ra sự giãn mạch đáng kể trong não. Ngoài ra, carbon dioxide trong máu, tác động lên trung tâm vận mạch của não, sẽ có một tác động gián tiếp cực kỳ mạnh, truyền qua hệ thống co mạch của thần kinh giao cảm gây ra sự co mạch lan rộng trên khắp cơ thể.
Hầu hết các chất giãn mạch hay co mạch sẽ có ít tác động lên lưu lượng máu dài hạn trừ khi chúng làm thay đổi tốc độ chuyển hóa của mô. Trong hầu hết các nghiên cứu thực nghiệm, lưu lượng máu mô và cung lượng tim (tổng lưu lượng máu đến tất cả các mô cơ thể) thì hầu như không thay đổi, trừ khi các lượng lớn chất co mạch mạnh như angiotensin II hay các chất giãn mạch mạnh như bradykinin thì được truyền kéo dài trong vòng 1 hoặc 2 ngày. Tại sao lưu lượng máu không thay đổi nhiều trong hầu hết các mô, ngay cả khi có mặt các lượng rất lớn các chất hoạt mạch này?
Để trả lời cho câu hỏi này, chúng ta phải nhớ lại một trong những nguyên lý nền tảng của chức năng tuần hoàn đã được bàn luận trước đó – khả năng của mỗi mô là sự tự điều hòa lưu lượng máu của chính nó theo các nhu cầu chuyển hóa và các chức năng khác nhau của mô. Sự sử dụng một chất co mạch mạnh, như angiotensin II có thể gây ra sự giảm tạm thời trong lưu lượng máu mô và cung lượng tim nhưng thường có ít tác động lâu dài nếu như không có sự thay đổi tốc độ chuyển hóa của mô. Tương tự, hầu hết các chất giãn mạch chỉ gây ra một sự thay đổi ngắn hạn trong lưu lượng máu mô và cung lượng tim nếu như chúng không làm thay đổi chuyển hóa mô. Vì thế, lưu lượng máu nhìn chung là được điều hòa theo các nhu cầu chuyên biệt của các mô, miễn là áp suất động mạch đủ để tưới máu các mô.
Cảm ơn các bạn đã theo dõi bài viết. Hẹn gặp lại các bạn trong các bài viết tiếp theo nhé !!!





































